Kobalt - Cobalt
 | |||||||||||||||||||||||||||||||
| Kobalt | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Wymowa |
/ K oʊ b ɒ L T / ( słuchania ) |
||||||||||||||||||||||||||||||
| Wygląd zewnętrzny | twardy błyszczący niebieskawo szary metal | ||||||||||||||||||||||||||||||
| Średnia masa atomowa R STD (Co) | 58,933 194 (3) | ||||||||||||||||||||||||||||||
| Kobalt w układzie okresowym | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Liczba atomowa ( Z ) | 27 | ||||||||||||||||||||||||||||||
| Grupa | grupa 9 | ||||||||||||||||||||||||||||||
| Okres | okres 4 | ||||||||||||||||||||||||||||||
| Blok | d-blok | ||||||||||||||||||||||||||||||
| Konfiguracja elektronów | [ Ar ] 3d 7 4s 2 | ||||||||||||||||||||||||||||||
| Elektrony na powłokę | 2, 8, 15, 2 | ||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||
| Faza w STP | solidny | ||||||||||||||||||||||||||||||
| Temperatura topnienia | 1768 K (1495 ° C, 2723 ° F) | ||||||||||||||||||||||||||||||
| Temperatura wrzenia | 3200 K (2927 °C, 5301 °F) | ||||||||||||||||||||||||||||||
| Gęstość (w pobliżu rt ) | 8,90 g / cm 3 | ||||||||||||||||||||||||||||||
| w stanie ciekłym (przy mp ) | 8,86 g / cm 3 | ||||||||||||||||||||||||||||||
| Ciepło stapiania | 16,06 kJ/mol | ||||||||||||||||||||||||||||||
| Ciepło parowania | 377 kJ/mol | ||||||||||||||||||||||||||||||
| Molowa pojemność cieplna | 24,81 J/(mol·K) | ||||||||||||||||||||||||||||||
Ciśnienie pary
| |||||||||||||||||||||||||||||||
| Właściwości atomowe | |||||||||||||||||||||||||||||||
| Stany utleniania | -3, -1, 0, +1, +2 , +3 , +4, +5 ( amfoteryczny tlenek) | ||||||||||||||||||||||||||||||
| Elektroujemność | Skala Paulinga: 1,88 | ||||||||||||||||||||||||||||||
| Energie jonizacji | |||||||||||||||||||||||||||||||
| Promień atomowy | empiryczny: 125 pm | ||||||||||||||||||||||||||||||
| Promień kowalencyjny | Niskie wirowanie: 126 ± 15:00 Wysokie wirowanie: 150 ± 7 pm |
||||||||||||||||||||||||||||||
| Linie widmowe kobaltu | |||||||||||||||||||||||||||||||
| Inne właściwości | |||||||||||||||||||||||||||||||
| Naturalne występowanie | pierwotny | ||||||||||||||||||||||||||||||
| Struktura krystaliczna | sześciokątny gęstego upakowania (HCP) | ||||||||||||||||||||||||||||||
| Prędkość dźwięku cienki pręt | 4720 m/s (przy 20 °C) | ||||||||||||||||||||||||||||||
| Rozszerzalność termiczna | 13,0 µm/(m⋅K) (przy 25 °C) | ||||||||||||||||||||||||||||||
| Przewodność cieplna | 100 W/(m⋅K) | ||||||||||||||||||||||||||||||
| Rezystancja | 62,4 nΩ⋅m (przy 20 °C) | ||||||||||||||||||||||||||||||
| Zamawianie magnetyczne | ferromagnetyczny | ||||||||||||||||||||||||||||||
| Moduł Younga | 209 GPa | ||||||||||||||||||||||||||||||
| Moduł ścinania | 75 GPa | ||||||||||||||||||||||||||||||
| Moduł objętościowy | 180 GPa | ||||||||||||||||||||||||||||||
| Współczynnik Poissona | 0,31 | ||||||||||||||||||||||||||||||
| Twardość Mohsa | 5.0 | ||||||||||||||||||||||||||||||
| Twardość Vickersa | 1043 MPa | ||||||||||||||||||||||||||||||
| Twardość Brinella | 470–3000 MPa | ||||||||||||||||||||||||||||||
| Numer CAS | 7440-48-4 | ||||||||||||||||||||||||||||||
| Historia | |||||||||||||||||||||||||||||||
| Odkrycie i pierwsza izolacja | Georg Brandt (1735) | ||||||||||||||||||||||||||||||
| Główne izotopy kobaltu | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
Kobalt to pierwiastek chemiczny o symbolu Co i liczbie atomowej 27. Podobnie jak nikiel , kobalt występuje w skorupie ziemskiej tylko w postaci połączonej chemicznie, z wyjątkiem niewielkich osadów występujących w stopach naturalnego żelaza meteorytowego . Wolny pierwiastek , wytwarzane przez redukcyjne wytapiania , jest twardym, błyszczącym, srebrzystoszare metalu .
Niebieskie pigmenty na bazie kobaltu ( błękit kobaltu ) były używane od czasów starożytnych w biżuterii i farbach, a także w celu nadania szkłu charakterystycznego niebieskiego odcienia, ale później sądzono, że kolor jest spowodowany znanym metalowym bizmutem . Górnicy od dawna używali nazwy kobold ore (po niemiecku ruda goblinów ) dla niektórych minerałów wytwarzających niebieski pigment ; zostały tak nazwane, ponieważ były ubogie w znane metale i dawały trujące opary zawierające arszenik podczas wytapiania. W 1735 r. okazało się, że takie rudy można zredukować do nowego metalu (pierwszego odkrytego od czasów starożytnych) i ostatecznie nazwano go koboldem .
Obecnie część kobaltu jest wytwarzana specjalnie z jednej z wielu rud metalicznych, takich jak kobalt (CoAsS). Pierwiastek ten jest jednak częściej wytwarzany jako produkt uboczny wydobycia miedzi i niklu . Copperbelt w Demokratycznej Republice Konga (DRK) i Zambii daje większość światowej produkcji kobaltu. Światowa produkcja w 2016 r. wyniosła 116 000 ton (114 000 długich ton; 128 000 krótkich ton) (według Natural Resources Canada ), a sama DRK stanowiła ponad 50%.
Kobalt jest używany głównie w akumulatorach litowo-jonowych oraz w produkcji stopów magnetycznych , odpornych na zużycie i o wysokiej wytrzymałości . Związki krzemianu kobaltu i glinianu kobaltu(II) (CoAl 2 O 4 , błękit kobaltowy) nadają charakterystyczny głęboki niebieski kolor szkłu , ceramice , tuszom , farbom i lakierom . Kobalt występuje naturalnie jako tylko jeden stabilny izotop , kobalt-59. Kobalt-60 jest ważnym komercyjnie radioizotopem, używanym jako znacznik radioaktywny i do produkcji wysokoenergetycznych promieni gamma .
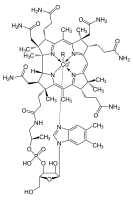
Kobalt jest aktywnym centrum grupy koenzymów zwanych kobalaminami . Witamina B 12 , najlepiej znanym przykładem takiego typu, jest istotnym witaminy dla wszystkich zwierząt. Kobalt w formie nieorganicznej jest również mikroelementem dla bakterii , alg i grzybów .
Charakterystyka

Kobalt to metal ferromagnetyczny o ciężarze właściwym 8,9. Temperatura Curie wynosi 1115 ° C (2039 ° F), a moment magnetyczny wynosi 1,6-1,7 magnetonów Bohra na atom . Kobalt ma względną przepuszczalność dwie trzecie przepuszczalności żelaza . Kobalt metaliczny występuje jako dwie struktury krystalograficzne : hcp i fcc . Idealna temperatura przejścia między strukturami hcp i fcc wynosi 450 °C (842°F), ale w praktyce różnica energii między nimi jest tak mała, że losowe przerastanie tych dwóch jest powszechne.
Kobalt to słabo redukujący metal, który jest chroniony przed utlenianiem przez pasywującą warstwę tlenku . Jest atakowany przez halogeny i siarkę . Ogrzewanie w tlen wytwarza Co 3 O 4 , który traci tlenu w temperaturze 900 ° C (1650 ° F) z wytworzeniem tlenku CoO. Metalowe reaguje z fluorem ( F 2 ) w temperaturze 520 K, w wyniku czego otrzymano COF 3 ; z chloru ( Cl 2 ), bromu ( Br 2 ) i jodu ( I 2 ) wytwarzania binarne odpowiadające halogenki . Nie reaguje z wodoru ( H 2 ), lub azot ( N 2 ), nawet podczas ogrzewania, ale nie reagują z boru , węgla , fosforu , arsenu i siarki. W zwykłych temperaturach reaguje powoli z kwasami mineralnymi , a bardzo powoli z wilgotnym, ale nie suchym powietrzem.
Związki
Typowe stany utlenienia kobaltu obejmują +2 i +3, chociaż znane są również związki o stopniu utlenienia w zakresie od -3 do +5 . Typowy stopień utlenienia prostych związków to +2 (kobalt(II)). Sole te tworzą różowy aquo kompleks metali [Co(H
2O)
6]2+
w wodzie. Dodatek chlorku daje intensywnie niebieski [CoCl
4]2-
. W teście płomienia boraksowego kobalt wykazuje głęboki błękit zarówno w płomieniach utleniających, jak i redukujących.
Związki tlenu i chalkogenu
Znanych jest kilka tlenków kobaltu. Zielony tlenek kobaltu(II) (CoO) ma strukturę soli kamiennej . Jest łatwo utleniany wodą i tlenem do brązowego wodorotlenku kobaltu(III) (Co(OH) 3 ). W temperaturze 600–700 °C CoO utlenia się do niebieskiego tlenku kobaltu(II,III) (Co 3 O 4 ), który ma strukturę spinelu . Znany jest również czarny tlenek kobaltu(III) (Co 2 O 3 ). Tlenki kobaltu są antyferromagnetyczne w niskich temperaturach : CoO ( temperatura Néela 291 K) i Co 3 O 4 (temperatura Néela: 40 K), co jest analogiczne do magnetytu (Fe 3 O 4 ), z mieszaniną utleniania +2 i +3 państw.
Główne tlenowców kobaltu zawierają czarne kobaltu (II), siarczki , COS 2 , który przyjmuje pirytu -jak struktury i kobaltu (III), siarczek (Co 2 S, 3 ).
Halogenki
Cztery dihalogenki kobaltu (II) są znane: kobaltu (II), fluorek (COF 2 różowy), (II), chlorek kobaltu (COCl 2 , niebieski), kobaltu (II), bromek (COBR 2 , zielony), kobaltu (II), jodek (CoI 2 , niebiesko-czarny). Halogenki te występują w postaci bezwodnej i uwodnionej. Podczas gdy bezwodny dichlorek jest niebieski, hydrat jest czerwony.
Potencjał redukcji dla reakcji Co3+
+ e − → Co2+
wynosi +1,92 V, powyżej chloru do chlorku, +1,36 V. W konsekwencji kobalt(III) i chlorek spowodowałyby redukcję kobaltu(III) do kobaltu(II). Ponieważ potencjał redukcji fluoru do fluoru jest tak wysoki, +2,87 V, fluorek kobaltu(III) jest jednym z niewielu prostych stabilnych związków kobaltu(III). Fluorek kobaltu(III), stosowany w niektórych reakcjach fluorowania, silnie reaguje z wodą.
Związki koordynacyjne
Podobnie jak w przypadku wszystkich metali, związki molekularne i wieloatomowe jony kobaltu są klasyfikowane jako kompleksy koordynacyjne , czyli cząsteczki lub jony, które zawierają kobalt połączony z kilkoma ligandami . Zasady elektroujemności i twardości-miękkości szeregu ligandów można wykorzystać do wyjaśnienia zwykłego stanu utlenienia kobaltu. Na przykład kompleksy Co3+ mają tendencję do posiadania ligandów aminowych . Ponieważ fosfor jest bardziej miękki niż azot, ligandy fosfinowe mają tendencję do bardziej miękkich Co 2+ i Co + , na przykład chlorek tris(trifenylofosfino)kobaltu(I) ( P(C
6h
5)
3)
3CoCl ). Bardziej elektroujemny (i twardszy) tlenek i fluorek może stabilizować pochodne Co 4+ i Co 5+ , np. heksafluorokobaltan cezu (Cs 2 CoF 6 ) i nadkobaltan potasu (K 3 CoO 4 ).
Alfred Werner , zdobywca nagrody Nobla pionier w dziedzinie chemii koordynacyjnej , pracował ze związkami o wzorze empirycznym [Co(NH
3)
6]3+
. Jednym z oznaczonych izomerów był chlorek heksaminy kobaltu(III) . Ten kompleks koordynacyjny, typowy kompleks typu Wernera, składa się z centralnego atomu kobaltu koordynowanego przez sześć aminowych ortogonalnych ligandów i trzy przeciwaniony chlorkowe . Zastosowanie chelatujących ligandów etylenodiaminy zamiast amoniaku daje tris(etylenodiamino)kobalt(III) ( [Co(en)
3]3+
), który był jednym z pierwszych kompleksów koordynacyjnych , które zostały rozłożone na izomery optyczne . Kompleks istnieje w prawo- i leworęcznych formach „trójłopatowego śmigła”. Ten kompleks został po raz pierwszy wyizolowany przez Wernera jako żółto-złote kryształy przypominające igły.
Związki metaloorganiczne
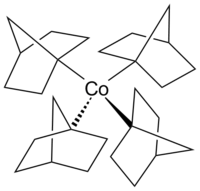
Cobaltocene jest analog strukturalny z ferrocenu , kobalt zamiast żelaza. Kobaltocen jest znacznie bardziej wrażliwy na utlenianie niż ferrocen. Karbonylową kobaltu ( Co 2 (CO) 8 ) jest katalizator do karbonylowania i hydrosililowania reakcji. Witaminy B 12 (patrz poniżej ) jest związek metaloorganiczny w naturze i jest jedyną witaminą , która zawiera atom metalu. Przykładem kompleksu alkilokobaltu na skądinąd rzadko spotykanym stopniu utlenienia +4 kobaltu jest homoleptyczny kompleks tetrakis(1-norbornylo)kobalt(IV) (Co(1-norb) 4 ), kompleks metal przejściowy-alkil, który wyróżnia się stabilnością w eliminacji β- wodoru . Kompleksy kobaltu(III) i kobaltu(V) [Li(THF)
4]+
[Co(1-norb)
4]−
i [Co(1-norb)
4]+
[BF
4]−
są również znane.
Izotopy
59 Co jest jedynym stabilnym izotopem kobaltu i jedynym izotopem naturalnie występującym na Ziemi. Scharakteryzowano dwadzieścia dwa radioizotopy : najbardziej stabilny, 60 Co , ma okres półtrwania 5,2714 lat; 57 Co ma okres półtrwania 271,8 dni; 56 Co ma okres półtrwania 77,27 dni; a 58 Co ma okres półtrwania 70,86 dni. Wszystkie inne radioaktywne izotopy kobaltu mają okres półtrwania krótszy niż 18 godzin, aw większości przypadków krótszy niż 1 sekunda. Ten pierwiastek ma również 4 stany meta , z których wszystkie mają okres półtrwania krótszy niż 15 minut.
Izotopy kobaltu mają masę atomową od 50 u ( 50 Co) do 73 u ( 73 Co). Podstawowym trybem rozpadu dla izotopów o wartościach masy atomowej mniejszej niż najbardziej rozpowszechniony stabilny izotop 59 Co, to wychwytywanie elektronów, a pierwotnym trybem rozpadu w izotopach o masie atomowej większej niż 59 jednostek masy atomowej jest rozpad beta . Głównymi produktami rozpadu poniżej 59 Co się element 26 ( żelazo ) izotopy; powyżej, że produktami rozpadu są izotopy pierwiastka 28 (niklu).
Historia
Związki kobaltu były używane od wieków do nadawania intensywnego niebieskiego koloru szkłu , glazurom i ceramice . Kobalt wykryto w egipskiej rzeźbie, perskiej biżuterii z III tysiąclecia p.n.e., w ruinach Pompejów zniszczonych w 79 r. n.e. oraz w Chinach, pochodzących z dynastii Tang (618–907 r. n.e.) i dynastii Ming (1368–1644 r.). OGŁOSZENIE).
Kobalt był używany do barwienia szkła od epoki brązu . Wykopaliska wraku statku Uluburun dostarczyły sztabki niebieskiego szkła, odlanej w XIV wieku p.n.e. Niebieskie szkło z Egiptu było barwione miedzią, żelazem lub kobaltem. Najstarsze szkło w kolorze kobaltu pochodzi z XVIII dynastii Egiptu (1550–1292 pne). Nie jest znane źródło kobaltu, którego używali Egipcjanie.
Słowo kobalt pochodzi od niemieckiego kobaltu , od kobold oznaczającego „goblin”, przesądnego terminu używanego przez górników dla rudy kobaltu. Pierwsze próby wytopu tych rud na miedź lub srebro nie powiodły się, zamiast tego uzyskano po prostu proszek (tlenek kobaltu(II)). Ponieważ pierwotne rudy kobaltu zawsze zawierają arsen, przetapianie rudy utleniało arsen do wysoce toksycznego i lotnego tlenku arsenu , zwiększając rozgłos rudy.
Szwedzkiemu chemikowi Georgowi Brandtowi (1694-1768) przypisuje się odkrycie kobaltu około 1735 roku, pokazując, że jest to nieznany wcześniej pierwiastek, różny od bizmutu i innych tradycyjnych metali. Brandt nazwał to nowym „semi-metalem”. Wykazał, że związki metalicznego kobaltu były źródłem niebieskiego koloru w szkle, co wcześniej przypisywano bizmutowi znalezionemu z kobaltem. Kobalt stał się pierwszym metalem odkrytym od czasów prehistorycznych. Wszystkie inne znane metale (żelazo, miedź, srebro, złoto, cynk, rtęć, cyna, ołów i bizmut) nie miały zarejestrowanych odkrywców.
W XIX wieku znaczna część światowej produkcji błękitu kobaltowego (pigmentu wytworzonego ze związków kobaltu i tlenku glinu) i smaltu ( szkło kobaltowe sproszkowane do użycia do celów pigmentowych w ceramice i malarstwie) była prowadzona w norweskim Blaafarveværket . Pierwsze kopalnie do produkcji smalty w XVI wieku znajdowały się w Norwegii, Szwecji, Saksonii i na Węgrzech. Wraz z odkryciem rudy kobaltu w Nowej Kaledonii w 1864 roku wydobycie kobaltu w Europie spadło. Wraz z odkryciem złóż rudy w Ontario w Kanadzie w 1904 r. i odkryciem jeszcze większych złóż w prowincji Katanga w Kongo w 1914 r. działalność wydobywcza uległa ponownemu przesunięciu. Kiedy w 1978 roku wybuchł konflikt Shaba , kopalnie miedzi w prowincji Katanga prawie wstrzymały produkcję. Wpływ tego konfliktu na światową gospodarkę kobaltową był mniejszy niż oczekiwano: kobalt jest rzadkim metalem, pigment jest wysoce toksyczny, a przemysł wypracował już skuteczne sposoby recyklingu materiałów kobaltowych. W niektórych przypadkach przemysł był w stanie przejść na alternatywy niezawierające kobaltu.
W 1938 roku John Livingood i Glenn T. Seaborg odkryli radioizotop kobalt-60 . Izotop ten był powszechnie używany na Uniwersytecie Columbia w latach 50. XX wieku w celu ustalenia naruszenia parzystości w radioaktywnym rozpadzie beta .
Po II wojnie światowej USA chciały zagwarantować dostawy rudy kobaltu do celów wojskowych (tak jak robili to Niemcy) i poszukiwać kobaltu w granicach USA. Odpowiednie zapasy rudy znaleziono w Idaho w pobliżu kanionu Blackbird na zboczu góry. Na miejscu rozpoczęła produkcję firma Calera Mining Company.
Argumentowano, że kobalt będzie jednym z głównych obiektów konkurencji geopolitycznej w świecie opartym na energii odnawialnej i zależnym od baterii, ale ta perspektywa była również krytykowana za niedocenianie siły bodźców ekonomicznych dla zwiększonej produkcji.
Występowanie
Stabilna forma kobaltu jest produkowana w supernowych w procesie r . Stanowi 0,0029% skorupy ziemskiej . Wolny kobalt ( metal rodzimy ) nie występuje na Ziemi z powodu tlenu w atmosferze i chloru w oceanie. Oba są wystarczająco obfite w górnych warstwach skorupy ziemskiej, aby zapobiec tworzeniu się rodzimego kobaltu. Z wyjątkiem niedawno dostarczonego w żelazie meteorytowym, czysty kobalt w postaci rodzimego metalu jest nieznany na Ziemi. Pierwiastek występuje średnio w obfitości, ale naturalne związki kobaltu są liczne, a niewielkie ilości związków kobaltu znajdują się w większości skał, gleb, roślin i zwierząt.
W naturze kobalt jest często kojarzony z niklem . Oba są charakterystycznymi składnikami żelaza meteorytowego , chociaż kobalt występuje w meteorytach żelaznych znacznie mniej niż nikiel. Podobnie jak w przypadku niklu, kobalt w stopach żelaza meteorytowego mógł być wystarczająco dobrze chroniony przed tlenem i wilgocią, aby pozostać jako wolny (ale stopowy) metal, chociaż żaden pierwiastek nie jest widoczny w tej postaci w starożytnej skorupie ziemskiej.
Kobalt w postaci związku występuje w minerałach miedzi i niklu. Jest to główny składnik metaliczny, który łączy się z siarką i arsenem w minerałach siarczkowego kobaltytu (CoAsS), szaflorytu ( CoAs 2 ), glaucodotu ( (Co,Fe)AsS ) i skutterudytu ( CoAs 3 ). Mineralny cattierite jest podobny do pirytu i występuje razem z waezytem w złożach miedzi w prowincji Katanga . Kiedy dociera do atmosfery, następuje wietrzenie ; minerały siarczku utleniają, tworząc różowy erytryn ( "oka": kobalt Co 3 (ASO 4 ) 2 · 8H 2 O ) i spherocobaltite (COCO 3 ).
Kobalt jest również składnikiem dymu tytoniowego . Tytoń łatwo wchłania i gromadzi metali ciężkich , jak kobalt z otaczającej ziemi w swoich liściach. Są one następnie wdychane podczas palenia tytoniu .
W oceanie
Kobalt jest metalem śladowym biorącym udział w fotosyntezie i wiązaniu azotu wykrywanym w większości basenów oceanicznych i jest mikroelementem ograniczającym fitoplankton i cyjanobakterie. Kompleks kobalaminy zawierający Co jest syntetyzowany tylko przez cyjanobakterie i kilka archeonów , więc stężenie rozpuszczonego kobaltu w górnym oceanie jest niskie. Podobnie jak Mn i Fe, Co ma hybrydowy profil wychwytywania biologicznego przez fitoplankton poprzez fotosyntezę w górnych warstwach oceanu i wychwytywanie w głębinach oceanicznych, chociaż większość wychwytywania jest ograniczona przez złożone ligandy organiczne. Co podlega recyklingowi w oceanie, rozkładając materię organiczną, która opada poniżej górnego poziomu oceanu, chociaż większość z nich jest oczyszczana przez bakterie utleniające.
Źródła kobaltu dla wielu zbiorników oceanicznych obejmują rzeki i spływy lądowe z pewnym wkładem z kominów hydrotermalnych. W głębokim oceanie źródła kobaltu znajdują się na szczytach gór podwodnych (które mogą być duże lub małe), gdzie prądy oceaniczne omiatają dno oceanu, usuwając osady na przestrzeni milionów lat, umożliwiając im tworzenie się skorup żelazomanganu. Chociaż wykonano ograniczone mapowanie dna morskiego, wstępne badania wskazują, że duża ilość tych bogatych w kobalt skorup znajduje się w Strefie Clarion Clipperton , obszarze, który cieszy się coraz większym zainteresowaniem dla przedsięwzięć górniczych jego domena. Wkład antropogeniczny jest źródłem nienaturalnym, ale w bardzo małych ilościach. Stężenia rozpuszczonego kobaltu (dCo) w oceanach są kontrolowane głównie przez zbiorniki, w których stężenie rozpuszczonego tlenu jest niskie. Złożony biochemiczny obieg kobaltu w oceanie jest nadal nieco błędnie rozumiany, ale wzorce wyższych stężeń odkryto w obszarach o niskiej zawartości tlenu, takich jak strefa minimum tlenu (OMZ) na południowym Oceanie Atlantyckim.
Kobalt jest uważany za toksyczny dla środowiska morskiego w wysokich stężeniach. W przypadku planktonu, takiego jak okrzemki, bezpieczne stężenia w wodach morskich spadają do około 18 μg/l . Na większość poziomów toksyczności przybrzeżnej wpływ mają czynniki antropogeniczne, takie jak spływ ścieków i spalanie paliw kopalnych. Wysokie poziomy Co i Se zostały zarejestrowane w owocach morza pochodzących z obszarów przybrzeżnych z wyższymi poziomami metali śladowych. Chociaż naukowcy są świadomi groźnej toksyczności, mniej uwagi poświęcono w porównaniu z innymi metalami śladowymi, takimi jak rtęć i ołów, w zanieczyszczonych systemach wodnych.
Produkcja
| Kraj | Produkcja | Rezerwy |
|---|---|---|
|
|
64 000 | 3 500 000 |
|
|
5600 | 250 000 |
|
|
5000 | 1 200 000 |
|
|
4300 | 250 000 |
|
|
4200 | 500 000 |
|
|
4000 | 280 000 |
|
|
3800 | 150 000 |
|
|
3200 | 51 000 |
|
|
2900 | 270 000 |
|
|
2800 | - |
|
|
2500 | 29 000 |
|
|
1500 | |
|
|
650 | 23 000 |
| Inne kraje | 5900 | 560 000 |
| Suma na świecie | 110 000 | 7 100 000 |
Głównymi rudami kobaltu są kobaltyt , erytryt , glaucodot i skutterudite (patrz wyżej), ale większość kobaltu otrzymuje się poprzez redukcję kobaltu jako produktów ubocznych wydobycia i wytopu niklu i miedzi .
Ponieważ kobalt jest generalnie wytwarzany jako produkt uboczny, podaż kobaltu zależy w dużej mierze od opłacalności wydobycia miedzi i niklu na danym rynku. Przewiduje się, że w 2017 r. popyt na kobalt wzrośnie o 6%.
Pierwotne złoża kobaltu są rzadkie, takie jak te występujące w złożach hydrotermalnych , związanych ze skałami ultramaficznymi , typowymi dla dystryktu Bou-Azzer w Maroku . W takich lokalizacjach wydobywa się wyłącznie rudy kobaltu, aczkolwiek w mniejszym stężeniu, a zatem wymagają dalszego przetwarzania w celu wydobycia kobaltu.
Istnieje kilka metod oddzielania kobaltu od miedzi i niklu, w zależności od stężenia kobaltu i dokładnego składu użytej rudy . Jedną z metod jest flotacja pianowa , w której środki powierzchniowo czynne wiążą się ze składnikami rudy, co prowadzi do wzbogacenia rud kobaltu. Późniejsze prażenie przekształca rudy w siarczan kobaltu , a miedź i żelazo utleniają się do tlenku. Wymywanie wodą powoduje ekstrakcję siarczanu wraz z arsenianami . Pozostałości są dalej ługowane kwasem siarkowym , otrzymując roztwór siarczanu miedzi. Kobalt może być również ługowany z żużla po wytopie miedzi.
Produkty powyższych procesów przekształcane są w tlenek kobaltu (Co 3 O 4 ). Tlenek ten jest redukowany do metalu w reakcji aluminotermicznej lub redukcji węglem w wielkim piecu .
Ekstrakcja
The United States Geological Survey szacuje światowe rezerwy kobaltu na 7 100 000 ton metrycznych. Demokratyczna Republika Konga (DRK), obecnie produkuje 63% światowej kobaltu. Ten udział w rynku może osiągnąć 73% do 2025 r., jeśli planowana ekspansja producentów górniczych, takich jak Glencore Plc, odbędzie się zgodnie z oczekiwaniami. Jednak do 2030 r. globalny popyt może być 47 razy większy niż w 2017 r., szacuje Bloomberg New Energy Finance.
Zmiany wprowadzone przez Kongo do prawa górniczego w 2002 roku przyciągnęły nowe inwestycje w kongijskie projekty dotyczące miedzi i kobaltu. W 2016 r. kopalnia Mutanda w Glencore dostarczyła 24 500 ton kobaltu , co stanowiło 40% wydobycia w Kongo DRK i prawie jedną czwartą światowej produkcji. Po nadpodaży Glencore zamknął Mutandę na dwa lata pod koniec 2019 roku. Projekt Katanga Mining Glencore również jest wznawiany i powinien wyprodukować 300 000 ton miedzi i 20 000 ton kobaltu do 2019 roku, według Glencore.
Po osiągnięciu niemal dekadowego rekordu na początku 2018 r. powyżej 100 000 USD za tonę, ceny kobaltu używanego w globalnym łańcuchu dostaw baterii elektrycznych spadły o 45% w ciągu następnych 2 lat. Wraz ze wzrostem popytu na pojazdy elektryczne (EV) w 2020 r. i w 2021 r. ceny kobaltu wzrosły w styczniu 2021 r. Wskaźnik cen kobaltu z marca 2021 r. pokazuje, że ceny rosną z miesiąca na miesiąc do 54 000 USD za tonę w dniu 19 marca 2021 r., co oznacza wzrost o 35% ponad 2 miesiące.
Kobalt jest uznawany za minerał krytyczny przez Stany Zjednoczone, Japonię, Republikę Korei, Wielką Brytanię i Unię Europejską.
Demokratyczna Republika Konga
W 2005 roku, top producent kobaltu było złoża miedzi w Demokratycznej Republice Konga „s Katanga . Dawna prowincja Shaba, obszar ten posiadał prawie 40% światowych zasobów, poinformował British Geological Survey w 2009 r. Do 2015 r. Demokratyczna Republika Konga (DRK) dostarczyła 60% światowej produkcji kobaltu, 32 000 ton po 20 000 do 26 000 USD za tonę. Niedawny wzrost produkcji mógł przynajmniej częściowo wynikać z tego, jak niska produkcja górnicza spadła podczas bardzo gwałtownych wojen domowych w Demokratycznej Republice Konga na początku 2000 roku, lub ze zmian wprowadzonych przez ten kraj do swojego Kodeksu Górniczego w 2002 roku, aby zachęcić do zagranicznych i międzynarodowych inwestycji. pozyskać wielu inwestorów, w tym Glencore .
Górnictwo rzemieślnicze dostarczało od 17% do 40% produkcji DRK. Około 100 000 górników kobaltu w Kongo DRK używa narzędzi ręcznych do kopania setek stóp, przy niewielkim planowaniu i mniejszych środkach bezpieczeństwa, mówią pracownicy, urzędnicy rządowi i organizacje pozarządowe, a także obserwacje reporterów The Washington Post dotyczące wizyt w odizolowanych kopalniach. Brak środków ostrożności często powoduje obrażenia lub śmierć. Według urzędników służby zdrowia, górnictwo zanieczyszcza okolicę i naraża lokalną przyrodę i rdzenną społeczność na działanie metali toksycznych, które mogą powodować wady wrodzone i problemy z oddychaniem.
Obrońcy praw człowieka twierdzili, a dziennikarstwo śledcze potwierdziło, że praca dzieci jest wykorzystywana do wydobywania kobaltu z afrykańskich kopalni rzemieślniczych . To odkrycie skłoniło producenta telefonów komórkowych Apple Inc. , 3 marca 2017 r., do zaprzestania kupowania rudy od dostawców takich jak Zhejiang Huayou Cobalt, którzy zaopatrują się w kopalnie rzemieślnicze w DRK, i zaczął korzystać tylko z dostawców zweryfikowanych pod kątem spełniania standardów w miejscu pracy.
Istnieje globalny nacisk ze strony UE i głównych producentów samochodów (OEM), aby globalna produkcja kobaltu była pozyskiwana i produkowana w sposób zrównoważony, odpowiedzialny i identyfikowalny w łańcuchu dostaw. Przedsiębiorstwa górnicze przyjmują i stosują inicjatywy ESG zgodnie z wytycznymi OECD i przedstawiają dowody świadczące o zerowym lub niskim śladzie węglowym w łańcuchu dostaw produkcji akumulatorów litowo-jonowych . Inicjatywy te są już realizowane z dużymi firmami górniczymi, rzemieślniczymi i małymi przedsiębiorstwami wydobywczymi (ASM). Producenci samochodów i łańcuchy dostaw producentów akumulatorów Tesla, VW, BMW, BASF, Glencore biorą udział w kilku inicjatywach, takich jak Responsible Cobalt Initiative i Cobalt for Development. W 2018 r. BMW Group we współpracy z BASF, Samsung SDI i Samsung Electronics uruchomiły projekt pilotażowy w DRK nad jedną kopalnią pilotażową, aby poprawić warunki i sprostać wyzwaniom dla górników rzemieślniczych i okolicznych społeczności.
Dynamika polityczna i etniczna regionu spowodowała w przeszłości wybuchy przemocy i lata konfliktów zbrojnych oraz przesiedlenia ludności. Ta niestabilność wpłynęła na cenę kobaltu, a także stworzyła przewrotne zachęty dla walczących w pierwszej i drugiej wojnie w Kongu, aby przedłużyć walki, ponieważ dostęp do kopalni diamentów i innych cennych zasobów pomógł sfinansować ich cele wojskowe – które często sprowadzały się do ludobójstwa – i wzbogacił także samych bojowników. Podczas gdy DR Kongo w 2010 roku nie było ostatnio najeżdżane przez sąsiednie siły zbrojne, niektóre z najbogatszych złóż minerałów sąsiadują z obszarami, gdzie Tutsi i Hutu wciąż często się ścierają, niepokoje trwają, chociaż na mniejszą skalę, a uchodźcy wciąż uciekają przed wybuchami przemocy.
Kobalt wydobyty z małych kongijskich rzemieślniczych przedsięwzięć wydobywczych w 2007 roku zaopatrywał jedną chińską firmę Congo DongFang International Mining. Spółka zależna Zhejiang Huayou Cobalt , jednego z największych światowych producentów kobaltu, Congo DongFang dostarczała kobalt niektórym z największych światowych producentów baterii, którzy produkowali baterie do wszechobecnych produktów, takich jak iPhone'y Apple . Ze względu na oskarżenia dotyczące naruszeń prawa pracy i troski o środowisko firma LG Chem przeprowadziła następnie audyt Congo DongFang zgodnie z wytycznymi OECD . Firma LG Chem, która produkuje również materiały akumulatorowe dla firm samochodowych, nałożyła kodeks postępowania na wszystkich kontrolowanych dostawców.
Projekt Mukondo Mountain , prowadzony przez Central African Mining and Exploration Company (CAMEC) w prowincji Katanga , może być najbogatszym rezerwatem kobaltu na świecie. Szacuje się, że wyprodukował jedną trzecią całkowitej światowej produkcji kobaltu w 2008 roku. W lipcu 2009 roku CAMEC ogłosił długoterminową umowę na dostawę całej rocznej produkcji koncentratu kobaltu z Mukondo Mountain do Zhejiang Galico Cobalt & Nickel Materials w Chinach.
W lutym 2018 r. globalna firma zarządzająca aktywami AllianceBernstein określiła DRK jako ekonomicznie „ Arabię Saudyjską ery pojazdów elektrycznych”, ze względu na jej zasoby kobaltu, niezbędne dla akumulatorów litowo-jonowych napędzających pojazdy elektryczne .
9 marca 2018 r. prezydent Joseph Kabila zaktualizował kodeks górniczy z 2002 r., zwiększając opłaty licencyjne i ogłaszając kobalt i koltan „metalami strategicznymi”.
Kodeks górniczy z 2002 r. został skutecznie zaktualizowany 4 grudnia 2018 r.
W grudniu 2019 r. International Rights Advocates, organizacja pozarządowa zajmująca się prawami człowieka, złożyła przełomowy pozew przeciwko Apple , Tesli , Dellowi , Microsoftowi i firmie Google Alphabet za „świadome czerpanie korzyści i pomoc w okrutnym i brutalnym wykorzystywaniu małych dzieci” w wydobyciu kobaltu . Firmy, o których mowa, zaprzeczyły swojemu udziałowi w pracy dzieci .
Kanada
W 2017 r. niektóre firmy poszukiwawcze planowały zbadać stare kopalnie srebra i kobaltu w rejonie Cobalt w Ontario, gdzie uważa się, że znajdują się znaczne złoża.
Kanadyjska firma Sherritt International przetwarza rudy kobaltu w złożach niklu z kopalni Moa na Kubie , a na wyspie znajduje się kilka innych kopalń w Mayari , Camaguey i Pinar del Rio . Kontynuacja inwestycji Sherritt International w kubańską produkcję niklu i kobaltu przy jednoczesnym nabyciu praw wydobywczych na 17-20 lat sprawiła, że w 2019 roku komunistyczny kraj był trzeci pod względem rezerw kobaltu, przed samą Kanadą.
Aplikacje
W 2016 roku zużyto 116 000 ton kobaltu. Kobalt został wykorzystany do produkcji stopów o wysokich parametrach użytkowych. Można go również wykorzystać do produkcji akumulatorów, a pojawienie się pojazdów elektrycznych i ich sukces wśród konsumentów prawdopodobnie ma wiele wspólnego z gwałtownie rosnącą produkcją w DRK. Innymi ważnymi czynnikami były Kodeks Górniczy z 2002 r., który zachęcał do inwestycji zagranicznych i transnarodowych korporacji, takich jak Glencore, oraz zakończenie I i II wojny w Kongo.
Stopy
Na bazie kobaltu nietypowe historycznie spożywane większość kobaltu produkowane. Stabilność temperaturowa tych stopów sprawia, że nadają się one na łopatki turbin do turbin gazowych i silników odrzutowych samolotów , chociaż stopy monokrystaliczne na bazie niklu przewyższają je pod względem wydajności. Stopy na bazie kobaltu są również odporne na korozję i zużycie, dzięki czemu, podobnie jak tytan , są przydatne do wytwarzania implantów ortopedycznych , które nie zużywają się z czasem. Rozwój odpornych na ścieranie stopów kobaltu rozpoczął się w pierwszej dekadzie XX wieku od stopów stellitowych , zawierających chrom z różnymi ilościami wolframu i węgla. Stopy z węglikami chromu i wolframu są bardzo twarde i odporne na zużycie. Specjalne stopy kobaltowo-chromowo- molibdenowe , takie jak Vitallium, są używane do wykonywania części protetycznych ( uzupełnienia stawu biodrowego i kolanowego). Stopy kobaltu są również stosowane w protetyce dentystycznej jako użyteczny substytut niklu, który może powodować alergie. Niektóre stale szybkotnące zawierają również kobalt zwiększający odporność na ciepło i zużycie. W magnesach trwałych stosowane są specjalne stopy aluminium, niklu, kobaltu i żelaza, znane jako Alnico oraz samaru i kobaltu ( magnes samarowo-kobaltowy ) . Jest również stopiony z 95% platyną do produkcji biżuterii, dając stop odpowiedni do precyzyjnego odlewania, który jest również lekko magnetyczny.
Baterie
Tlenek litowo-kobaltowy (LiCoO 2 ) jest szeroko stosowany w katodach akumulatorów litowo-jonowych . Materiał składa się z warstw tlenku kobaltu z interkalacją litu . Podczas rozładowania ( tj. gdy nie jest aktywnie ładowany), lit jest uwalniany jako jony litu. Akumulatory niklowo-kadmowe (NiCd) i niklowo-wodorkowe (NiMH) zawierają również kobalt, który poprawia utlenianie niklu w akumulatorze. Transparency Market Research oszacował światowy rynek akumulatorów litowo-jonowych na 30 miliardów dolarów w 2015 roku i przewidywał wzrost do ponad 75 miliardów dolarów do 2024 roku.
Chociaż w 2018 r. większość kobaltu w bateriach była używana w urządzeniu mobilnym, nowszym zastosowaniem kobaltu są akumulatory do samochodów elektrycznych. Przemysł ten pięciokrotnie zwiększył zapotrzebowanie na kobalt, co sprawia, że pilne jest znalezienie nowych surowców w bardziej stabilnych obszarach świata. Oczekuje się, że popyt utrzyma się lub wzrośnie wraz ze wzrostem rozpowszechnienia pojazdów elektrycznych. Eksploracja w latach 2016–2017 objęła obszar wokół Cobalt w prowincji Ontario , gdzie wiele kopalni srebra przestało działać kilkadziesiąt lat temu. Kobalt dla pojazdów elektrycznych wzrósł o 81% od I półrocza 2018 r. do 7200 ton w I półroczu 2019 r., przy pojemności baterii 46,3 GWh. Przyszłość samochodów elektrycznych może zależeć od górnictwa głębinowego, ponieważ kobalt jest bogaty w skały na dnie morskim.
Ponieważ w wydobyciu kobaltu, głównie w kopalniach rzemieślniczych w DR Konga, wielokrotnie odnotowywano pracę dzieci i niewolników, firmy technologiczne poszukujące etycznego łańcucha dostaw stanęły w obliczu niedoborów tego surowca, a cena kobaltu w październiku osiągnęła najwyższy poziom od dziewięciu lat. 2017 r., ponad 30 USD za funt, w porównaniu z 10 USD pod koniec 2015 r. Po nadpodaży cena spadła do bardziej normalnego poziomu 15 USD w 2019 r. W odpowiedzi na problemy z rzemieślniczym wydobyciem kobaltu w DR Kongo wielu dostawców kobaltu i ich klienci utworzyli Fair Cobalt Alliance (FCA), którego celem jest położenie kresu pracy dzieci i poprawa warunków pracy przy wydobyciu i przetwarzaniu kobaltu w Demokratycznej Republice Konga. Członkowie FCA to m.in. Zhejiang Huayou Cobalt , Sono Motors , Responsible Cobalt Initiative , Fairphone , Glencore i Tesla, Inc.
Unia Europejska prowadzi badania nad możliwością wyeliminowania wymagań dotyczących kobaltu w produkcji akumulatorów litowo-jonowych. Od sierpnia 2020 r. producenci baterii stopniowo zmniejszali zawartość kobaltu w katodzie z 1/3 ( NMC 111) do 2/10 (NMC 442) do 1/10 (NMC 811), a także wprowadzili do baterii bezkobaltową katodę LFP paczki samochodów elektrycznych, takich jak Tesla Model 3 . We wrześniu 2020 r. Tesla przedstawił swoje plany stworzenia własnych, wolnych od kobaltu ogniw baterii.
Katalizatory
Kilka związków kobaltu to katalizatory utleniania. Octan kobaltu jest używany do konwersji ksylenu do kwasu tereftalowego , prekursora politereftalanu etylenu w masie . Typowymi katalizatorami są karboksylany kobaltu (znane jako mydła kobaltowe). Stosowane są również w farbach, lakierach i tuszach jako „środki suszące” poprzez utlenianie schnących olejów . Te same karboksylany są używane do poprawy przyczepności między stalą a gumą w oponach radialnych z opasaniem stalowym. Ponadto są stosowane jako przyspieszacze w systemach żywic poliestrowych .
Katalizatory na bazie kobaltu są stosowane w reakcjach z udziałem tlenku węgla . Kobalt jest również katalizatorem w procesie Fischera-Tropscha do uwodorniania tlenku węgla do paliw płynnych. Hydroformylowanie z alkenów często wykorzystuje kobaltu octacarbonyl jako katalizatora, ale często jest zastąpiony przez bardziej efektywne iridium- i rodowych katalizatorów opartych, na przykład w procesie Cativa .
Hydroodsiarczania z ropy naftowej wykorzystuje katalizator pochodzi z kobaltu i molibdenu. Proces ten pomaga w oczyszczeniu ropy naftowej z zanieczyszczeń siarkowych, które przeszkadzają w rafinacji paliw płynnych.
Pigmenty i barwniki
Przed XIX wiekiem kobalt był używany głównie jako pigment. Jest używany od średniowiecza do produkcji smalta , niebieskiego szkła. Smalt jest wytwarzany przez stopienie mieszanki palonego mineralnego smaltytu , kwarcu i węglanu potasu , co daje ciemnoniebieskie szkło krzemianowe, które po wytworzeniu jest drobno zmielone. Smalt był szeroko stosowany do barwienia szkła i jako pigment do obrazów. W 1780 roku Sven Rinman odkrył zieleń kobaltową , aw 1802 Louis Jacques Thénard odkrył błękit kobaltowy. Pigmenty kobaltowe, takie jak błękit kobaltowy (glinian kobaltu), błękit cerulowy ( cynian kobaltu(II), różne odcienie zieleni kobaltowej (mieszanina tlenku kobaltu(II) i tlenku cynku ) oraz fiolet kobaltowy ( fosforan kobaltu ) są stosowane jako pigmenty artystyczne ze względu na ich doskonałą stabilność chromatyczną. Aureolin ( żółcień kobaltowy) jest obecnie w dużej mierze zastępowany przez bardziej odporne na światło żółte pigmenty.
Radioizotopy
Kobalt-60 (Co-60 lub 60 Co) jest użyteczny jako źródło promieniowania gamma, ponieważ może być wytwarzany w przewidywalnych ilościach z wysoką aktywnością przez bombardowanie kobaltu neutronami . Wytwarza promienie gamma o energiach 1,17 i 1,33 MeV .
Kobalt jest stosowany w radioterapii wiązką zewnętrzną , sterylizacji materiałów medycznych i odpadów medycznych, napromieniowaniu żywności do sterylizacji (zimna pasteryzacja ), radiografii przemysłowej (np. zdjęcia rentgenowskie integralności spoin), pomiarach gęstości (np. pomiary gęstości betonu) oraz przełącznikach wysokości napełnienia zbiornika . Metal ma niefortunną właściwość tworzenia drobnego pyłu, co powoduje problemy z ochroną przed promieniowaniem . Kobalt z urządzeń do radioterapii stanowił poważne zagrożenie, gdy nie był właściwie usuwany, a jeden z najgorszych wypadków skażenia promieniowaniem w Ameryce Północnej miał miejsce w 1984 r., kiedy wyrzucona jednostka do radioterapii zawierająca kobalt-60 została omyłkowo zdemontowana na złomowisku w Juarez w Meksyku.
Cobalt-60 ma radioaktywny okres półtrwania 5,27 lat. Utrata siły działania wymaga okresowej wymiany źródła w radioterapii i jest jednym z powodów, dla których maszyny kobaltowe zostały w dużej mierze zastąpione akceleratorami liniowymi w nowoczesnej radioterapii. Kobalt-57 (Co-57 albo 57 CO) radioizotopem kobalt najczęściej stosowane w badaniach medycznych, jako znacznik radioaktywny do witaminy B 12 wychwytu, oraz do badania Schilling . Kobalt-57 jest używany jako źródło w spektroskopii Mössbauera i jest jednym z kilku możliwych źródeł w urządzeniach do fluorescencji rentgenowskiej .
Projekty broni jądrowej mogłyby celowo zawierać 59 Co, z których część byłaby aktywowana podczas eksplozji nuklearnej w celu wytworzenia 60 Co. 60 Co, rozproszone jako opad jądrowy , jest czasami nazywane bombą kobaltową .
Inne zastosowania
- Kobalt jest używany w galwanotechnice ze względu na atrakcyjny wygląd, twardość i odporność na utlenianie .
- Stosowany jest również jako podkład podkładowy pod emalie porcelanowe .
Rola biologiczna
Kobalt jest niezbędny do metabolizmu wszystkich zwierząt . Jest głównym składnikiem kobalaminy , znana także jako witamina B 12 , głównym zbiorniku biologicznym kobaltu jako elementu ultraśladów . Bakterie w żołądkach przeżuwaczy zwierząt konwersji sole kobaltu w witaminę B 12 , związek, który może być wytwarzany przez bakterie lub archeowce . Dlatego minimalnej obecności kobaltu w glebie znacząco poprawia stan zdrowia wypasu zwierząt i wychwyceniu 0,20 mg / kg na dzień jest zalecana, ponieważ nie mają one inne źródło witaminy B 12 .
Białka na bazie kobalaminy wykorzystują corrin do przechowywania kobaltu. Koenzym B 12 zawiera reaktywne wiązanie C-Co, które uczestniczy w reakcjach. U ludzi, B 12 ma dwa rodzaje alkilową ligand : metyl i adenozylometioniny. Meb 12 promuje metylu (CH 3 transferów) grupy. Wersja adenozylo: B 12 katalizuje przegrupowania, w którym atom wodoru jest bezpośrednio przesyłany pomiędzy dwoma sąsiednimi atomami z jednoczesną wymianę drugim podstawnikiem, X, który może być atomem węgla z podstawnikami, atom tlenu alkoholem lub aminą. Mutaza koenzymu A metylomalonylu (MUT) przekształca MM1-CoA w Su-CoA , co jest ważnym krokiem w ekstrakcji energii z białek i tłuszczów.
Chociaż znacznie rzadziej niż inne metaloprotein (na przykład tych, cynku i żelaza), inne cobaltoproteins znane są poza B 12 . Te białka obejmują Aminopeptydaza metioniny 2 , enzymu który występuje u ludzi i innych ssaków, które nie wykorzystują pierścień koryny związku B 12 , ale wiąże się bezpośrednio kobaltu. Innym nie-corrinowym enzymem kobaltowym jest hydrataza nitrylowa , enzym występujący w bakteriach, który metabolizuje nitryle .
Niedobór kobaltu
U ludzi, spożywanie zawierający kobalt witaminy B 12 spełnia wszystkie potrzeby związane z kobaltem. Dla bydła i owiec, które spełniają witaminy B 12 potrzeb na drodze syntezy przez bakterie stale występującej w żwaczu, jest funkcją nieorganicznej kobaltu. Na początku XX wieku, podczas rozwoju rolnictwa na Wyspie Wulkanicznej Wyspy Północnej Nowej Zelandii, bydło cierpiało na tzw. chorobę krzewów. Odkryto, że w glebach wulkanicznych brakowało soli kobaltu niezbędnych w łańcuchu pokarmowym bydła. „Choroby wybrzeże” owiec w Ninety Mile pustyni w południowo-wschodniej z Południowej Australii w 1930 roku stwierdzono, że pochodzą z niedoborów żywieniowych pierwiastków śladowych, kobaltu i miedzi. Niedobór kobaltu został przezwyciężony przez opracowanie „kul kobaltowych”, gęstych granulek tlenku kobaltu zmieszanych z gliną podawanych doustnie w celu wylegania w żwaczu zwierzęcia .
Problemy zdrowotne
| Zagrożenia | |
|---|---|
| Piktogramy GHS |

|
| Hasło ostrzegawcze GHS | Zagrożenie |
| H317 , H334 , H413 | |
| P261 , P272 , P273 , P280 , P285 , P302+352 , P304+341 , P333+313 , P342+311 , P363 , P405 , P501 | |
| NFPA 704 (ognisty diament) | |
LD 50 wartości dla rozpuszczalnych soli kobaltu Ocenia się między 150 a 500 mg / kg. W Stanach Zjednoczonych Urząd Bezpieczeństwa i Higieny Pracy (OSHA) wyznaczył dopuszczalny limit narażenia (PEL) w miejscu pracy jako średnią ważoną w czasie (TWA) na poziomie 0,1 mg/m 3 . Narodowy Instytut Zdrowia i Bezpieczeństwa Pracy (NIOSH) ustalił granicę zalecanej ekspozycji (REL) 0,05 mg / m 3 , średnia ważona czasowo. Wartość IDLH (bezpośrednio zagrażająca życiu i zdrowiu) wynosi 20 mg/m 3 .
Jednak przewlekłe spożywanie kobaltu spowodowało poważne problemy zdrowotne przy dawkach znacznie mniejszych niż dawka śmiertelna. W 1966 roku dodanie związków kobaltu w celu stabilizacji piany piwa w Kanadzie doprowadziło do szczególnej formy kardiomiopatii wywołanej toksynami , która stała się znana jako kardiomiopatia pijących piwo .
Ponadto, kobalt metal podejrzewa się, że powoduje raka (tzn ewentualnie rakotwórczych , IARC grupa 2B ), zgodnie z Międzynarodowa Agencja Badań nad Rakiem (IARC) monografii. [PDF]
Wdychanie powoduje problemy z oddychaniem. Powoduje również problemy skórne po dotknięciu; Kobalt jest po niklu i chromie główną przyczyną kontaktowego zapalenia skóry . Na te zagrożenia stoją górnicy kobaltu.
Zobacz też
- Coltan
- Minerał konfliktu
- Gospodarka Demokratycznej Republiki Konga
- Przemysł wydobywczy Demokratycznej Republiki Konga
Bibliografia
Dalsza lektura
- Harper, EM; Kavlak, G.; Graedel, TE (2012). „Śledzenie metalu goblinów: cykl użytkowania kobaltu”. Nauka o środowisku i technologia . 46 (2): 1079–86. Kod Bib : 2012EnST...46.1079H . doi : 10.1021/es201874e . PMID 22142288 .
- Narendrula, R.; Nkongolo, KK; Beckett, P. (2012). „Porównawcze analizy metali w glebie w Sudbury (Ontario, Kanada) i Lubumbashi (Ktanga, DR-Kongo)”. Biuletyn Skażenia Środowiska i Toksykologii . 88 (2): 187-92. doi : 10.1007/s00128-011-0485-7 . PMID 22139330 . S2CID 34070357 .
- Pauwels, H.; Pettenati, M.; Greffié, C. (2010). „Połączony wpływ opuszczonych kopalń i rolnictwa na chemię wód podziemnych”. Journal of Contaminant Hydrology . 115 (1–4): 64–78. Kod bib : 2010JCHyd.115...64P . doi : 10.1016/j.jconhyd.2010.04.003 . PMID 20466452 .
- Bulut, G. (2006). „Odzyskiwanie miedzi i kobaltu ze starożytnego żużla”. Gospodarka odpadami i badania . 24 (2): 118-24. doi : 10.1177/0734242X06063350 . PMID 16634226 . S2CID 24931095 .
- Jefferson, JA; Escudero, E.; Hurtado, ME; Pando, J.; Tapia, R.; Swenson, ER; Prchal, J.; Schreinera, GF; Schöne, RB; Hurtado, A.; Johnson, RJ (2002). „Nadmierna erytrocytoza, przewlekła choroba górska i poziom kobaltu w surowicy”. Lancet . 359 (9304): 407-8. doi : 10.1016/s0140-6736(02)07594-3 . PMID 11844517 . S2CID 12319751 .
- Løvold, telewizja; Haugsbø, L. (1999). „Fabryka wydobycia kobaltu – diagnozy 1822-32”. Tidsskrift dla den Norske Laegeforening . 119 (30): 4544-6. PMID 10827501 .
- Ptak, GA; Hesslein, RH; Młyny, KH; Schwartz, WJ; Turner, mgr (1998). „Bioakumulacja radionuklidów w nawożonych basenach kanadyjskich jezior Shield”. Nauka o całkowitym środowisku . 218 (1): 67-83. Kod Bib : 1998ScTEn.218...67B . doi : 10.1016/s0048-9697(98)00179-x . PMID 9718743 .
- Nemery B. (1990). „Toksyczność metali a drogi oddechowe”. European Respiratory Journal . 3 (2): 202–19. PMID 2178966 .
- Kazantzis, G. (1981). „Rola kobaltu, żelaza, ołowiu, manganu, rtęci, platyny, selenu i tytanu w karcynogenezie” . Perspektywy ochrony środowiska . 40 : 143-61. doi : 10.1289/ehp.8140143 . PMC 1568837 . PMID 7023929 .
- Kerfoot, EJ; Fredrick, WG; Domeier, E. (1975). „Badania inhalacji metali kobaltowych na miniaturowych świniach”. Dziennik Amerykańskiego Stowarzyszenia Higieny Przemysłowej . 36 (1): 17–25. doi : 10.1080/0002889758507202 . PMID 1111264 .
Zewnętrzne linki
- Kobalt w układzie okresowym filmów wideo (University of Nottingham)
- Centra Chorób i Prewencji – Kobalt
- Instytut Kobaltu
- Odpowiedzialny Instytut Kobaltu