Poliketyd - Polyketide
Poliketydy duża grupy metabolitów wtórnych , które albo zawierają naprzemienne grupy karbonylowe i grupy metylenowe (-CO-CH 2 -), lub które pochodzą z prekursorów, które zawierają takie grupy zmienny. Wiele poliketydów ma właściwości lecznicze lub wykazuje ostrą toksyczność.
- Poliketydy
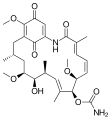
Geldanamycin , użyteczny antybiotyk.
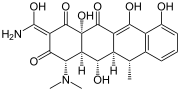
Doksycyklina , kolejny ważny antybiotyk.
Erytromycyna , antybiotyk.
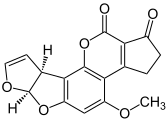
Aflatoksyna B1 jeden z najbardziej znanych związków rakotwórczych .
Biosynteza
Poliketydy są produkowane w bakteriach, grzybach, roślinach i niektórych zwierzętach morskich. Biosynteza obejmuje stopniową kondensację acetylo-CoA lub propionylo-CoA z malonylo-CoA lub metylomalonylo-CoA. Reakcji kondensacji towarzyszy dekarboksylacja jednostki przedłużającej i daje grupę funkcyjną beta-keto. Pierwsza kondensacja daje grupę acetoacetylową, diketyd . Kolejne kondensacje dają triketydy , tetraketydy itp.

Łańcuchy poliketydowe wytwarzane przez minimalną syntazę poliketydową są prawie niezmiennie modyfikowane. Modyfikacje obejmują redukcję grup ketonowych do metylenu i cyklizację. Wiele z tych konwersji zachodzi przez tautomery enolowe poliketydu. Poliketydy to rodzina zróżnicowana strukturalnie. Są one ogólnie podzielone na trzy klasy: poliketydy typu I (często makrolidy wytwarzane przez multimodularne megasyntazy ), poliketydy typu II (często aromatyczne cząsteczki wytwarzane przez iteracyjne działanie zdysocjowanych enzymów ) oraz poliketydy typu III (często małe cząsteczki aromatyczne wytwarzane przez gatunki grzybów ).
Poliketydy są syntetyzowane przez polipeptydy wieloenzymatyczne, które przypominają syntazę eukariotycznych kwasów tłuszczowych, ale często są znacznie większe. Obejmują one domeny nośnika acylowego oraz zestaw jednostek enzymatycznych, które mogą funkcjonować w sposób iteracyjny, powtarzając te same etapy wydłużania/modyfikacji (jak w syntezie kwasów tłuszczowych) lub w sposób sekwencyjny, aby wygenerować bardziej heterogeniczne typy poliketydów.
Aplikacje
Antybiotyki poliketydowe , przeciwgrzybicze , cytostatyki , przeciwcholesterolowe , przeciwpasożytnicze , kokcydiostatyki , stymulatory wzrostu zwierząt i naturalne insektycydy są w użyciu komercyjnym .
Przykłady
-
Makrolidy
- Pikromycyna , pierwszy wyizolowany makrolid (1951)
- Te antybiotyki erytromycyny A , klarytromycyna i azytromycyny
- Środki przeciw robakom awermektyna i iwermektyna
- Owadobójczy spinosad (spinozyn)
-
Ansamycyny
- W przeciwnowotworowe środki geldanamycyna i macbecin ,
- Antybiotyk ryfamycyną
- Polieny
- Polietery
-
Tetracykliny
- Antybiotyk doksycyklina
- Acetogeniny
- Inni
- Immunosupresyjne, takrolimus (FK-506) (a kalcyneuryny, inhibitor) i sirolimus (rapamycyna) (A mTOR inhibitora)
- Radicicol i rodzina pochonin ( inhibitory HSP90 )
- Cholesterolu, obniżając środek lowastatyna
- Dyskodermolid
- Aflatoksyna
- kwas usninowy
- antracimycyna
- antramycyna
Zobacz też
Bibliografia
- ^ IUPAC , Kompendium Terminologii Chemicznej , wyd. ("Złota Księga") (1997). Wersja poprawiona online: (2006-) „ Poliketydy ”. doi : 10.1351/goldbook.P04734
- ^ a b Voet Donald ; Voet, Judith G. ; Pratt, Charlotte W. (2013). Podstawy biochemii: Życie na poziomie molekularnym (4 wyd.). John Wiley i Synowie . P. 688. ISBN 9780470547847.
- ^ Staunton, James; Weissman, Kira J. (2001). „Biosynteza poliketydów: przegląd milenijny”. Raporty o produktach naturalnych . 18 (4): 380–416. doi : 10.1039/a909079g . PMID 11548049 .
- ^ Robinson, John A.; Fersht, Alan Roy ; Gani, D. (1991). „Kompleksy syntazy poliketydowej: ich struktura i funkcja w biosyntezie antybiotyków”. Filos. Przeł. R. Soc. Londyn. B Biol. Nauka. 332 (1263): 107-114. Kod Bib : 1991RSPTB.332..107R . doi : 10.1098/rstb.1991.0038 . PMID 1678529 .
- ^ Katz Leonard (1997). „Manipulacja modułowymi syntezami poliketydowymi”. Chem. Obj. 97 (7): 2557-2576. doi : 10.1021/cr960025+ . PMID 11851471 .
- ^ „5.13E: Antybiotyki poliketydowe” . LibreTexts biologii . 2017-05-09 . Pobrano 2021-07-05 .
- ^ B Ross Claudia; Opla, Wiktorii; Scherlach, Kirstin; Hertweck, Chrześcijanin (2014). „Biosynteza poliketydów przeciwgrzybiczych i przeciwbakteryjnych przez Burkholderia gladioli we współhodowli z Rhizopus microsporus” . Grzybice . 57 Suplement 3: 48–55. doi : 10.1111/myc.12246 . ISSN 1439-0507 . PMID 25250879 .
- ^ Jiang, Lin; Pu, Hong; Xiang, Jingxi; Su, Meng; Yan, Xiaohui; Yang, Dong; Zhu, Xiangcheng; Shen, Ben; Duan, Yanwen; Huang, Yong (2018). „Huanglongmycyna AC, cytotoksyczne poliketydy biosyntetyzowane przez przypuszczalną syntazę poliketydową typu II ze Streptomyces sp. CB09001” . Granice w chemii . 6 : 254. Kod bib : 2018FrCh ....6..254J . doi : 10.3389/fchem.2018.00254 . ISSN 2296-2646 . PMC 6036704 . PMID 30013965 .
- ^ Chan, Yolande A .; Podevels, Angela M.; Kevany, Brian M.; Tomasz, Michael G. (2009). „Biosynteza jednostek przedłużających syntazę poliketydową” . Raporty o produktach naturalnych . 26 (1): 90–114. doi : 10.1039/b801658p . ISSN 0265-0568 . PMC 2766543 . PMID 19374124 .
- ^ Kim, Hak Joong; Choi, Sei-hyun; Jeon, Byung-sun; Kim, Namho; Pongdee, Rongson; Wu, Qingquan; Liu, Hung-wen (01.12.2014). „Chemoenzymatyczna synteza spinozyny A” . Angewandte Chemie International Edition w języku angielskim . 53 (49): 13553-13557. doi : 10.1002/anie.201407806 . ISSN 1521-3773 . PMC 4266379 . PMID 25287333 .
- ^ Brockmann, Hans; Henkel, Willfried (1951). „Pikromycyna, ein bitter schmeckendes Antibioticum aus Actinomyceten” [Pikromycyna, antybiotyk o gorzkim smaku z promieniowców]. Chem. Ber. (po niemiecku). 84 (3): 284–288. doi : 10.1002/cber.19510840306 .