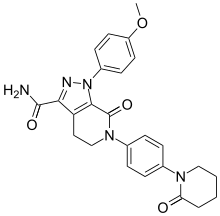
Apiksaban - Apixaban
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Eliquis, inni |
| Inne nazwy | BMS-562247-01 |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a613032 |
| Dane licencyjne | |
Kategoria ciąży |
|
| Drogi administracji |
Ustami |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | ~50% |
| Wiązanie białek | ~87% |
| Metabolizm | CYP3A4 , CYP3A5 , CYP1A2 i inne |
| Okres półtrwania eliminacji | 9-14 godz |
| Wydalanie | Żółć (75%), nerki (25%) |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.167,332 |
| Dane chemiczne i fizyczne | |
| Formuła | C 25 H 25 N 5 O 4 |
| Masa cząsteczkowa | 459,506 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Apixaban , sprzedawany pod marką Eliquis , jest lekiem przeciwzakrzepowym stosowanym w leczeniu i zapobieganiu zakrzepom krwi oraz w zapobieganiu udarom mózgu u osób z niezastawkowym migotaniem przedsionków . W szczególności stosuje się go w celu zapobiegania powstawaniu zakrzepów krwi po wymianie stawu biodrowego lub kolanowego oraz u osób z historią zakrzepów. Jest stosowany jako alternatywa dla warfaryny i nie wymaga monitorowania za pomocą badań krwi ani ograniczeń dietetycznych. Jest przyjmowany doustnie .
Częste działania niepożądane to krwawienie i nudności. Inne działania niepożądane mogą obejmować krwawienie wokół kręgosłupa i reakcje alergiczne. Nie zaleca się stosowania w okresie ciąży lub karmienia piersią . Stosowanie wydaje się być stosunkowo bezpieczne u osób z łagodnymi problemami z nerkami . W porównaniu do warfaryny ma mniej interakcji z innymi lekami . Jest bezpośrednim inhibitorem czynnika Xa .
Apiksaban został dopuszczony do użytku medycznego w Unii Europejskiej w maju 2011 r., aw Stanach Zjednoczonych w grudniu 2012 r. Znajduje się na liście podstawowych leków Światowej Organizacji Zdrowia . W 2019 roku był to 52. najczęściej przepisywany lek w Stanach Zjednoczonych z ponad 14 milionami recept. W grudniu 2019 r. w Stanach Zjednoczonych zatwierdzono wersje generyczne.
Mechanizm akcji
Apiksaban jest wysoce selektywnym, biodostępnym po podaniu doustnym i odwracalnym bezpośrednim inhibitorem wolnego i związanego z skrzepem czynnika Xa . Czynnik Xa katalizuje konwersję protrombiny do trombiny, ostatniego enzymu w kaskadzie krzepnięcia, który jest odpowiedzialny za tworzenie skrzepu fibryny . Apiksaban nie ma bezpośredniego wpływu na agregację płytek krwi , ale poprzez hamowanie czynnika Xa pośrednio zmniejsza tworzenie skrzepów indukowane przez trombinę.
Zastosowania medyczne
Apiksaban jest wskazany w następujących przypadkach:
- Obniżenie ryzyka udaru i zatorowości u osób z niezastawkowym migotaniem przedsionków .
- Zapobieganie zakrzepicy żył głębokich (ZŻG). ZŻG może prowadzić do zatorowości płucnej (PE) u pacjentów po operacji wymiany stawu kolanowego lub biodrowego.
- Leczenie zarówno ZŻG, jak i ZP.
- Zmniejszenie ryzyka nawrotu ZŻG i ZP po początkowym leczeniu.
W UE apiksaban jest wskazany w zapobieganiu żylnym incydentom zakrzepowo-zatorowym (ŻChZZ) u osób dorosłych po przebytej planowej alloplastyce stawu biodrowego lub kolanowego, zapobieganiu udarowi i zatorowości systemowej u dorosłych z niezastawkowym migotaniem przedsionków (NVAF) z jednym lub więcej czynników ryzyka, w leczeniu zakrzepicy żył głębokich (ZŻG) i zatorowości płucnej (ZP) u dorosłych oraz w zapobieganiu nawrotowej ZŻG i ZP u dorosłych.
Migotanie przedsionków
Apiksaban jest zalecany przez Narodowy Instytut Zdrowia i Doskonałości Klinicznej w profilaktyce udaru mózgu i zatorowości systemowej u osób z niezastawkowym migotaniem przedsionków i co najmniej jednym z następujących czynników ryzyka: przebyty udar lub przemijający napad niedokrwienny, wiek 75 lat lub więcej , cukrzyca , lub objawowa niewydolność serca .
Apiksaban i inne antykoagulanty ( dabigatran , edoksaban i rywaroksaban ) wydają się równie skuteczne jak warfaryna w zapobieganiu udarom niekrwotocznym u osób z migotaniem przedsionków i wiążą się z mniejszym ryzykiem krwawienia śródczaszkowego.
Chociaż apiksaban może być stosowany u osób z poważnie obniżoną czynnością nerek i osób poddawanych hemodializie, nie badano go w tych grupach. Można zastosować pełną dawkę apiksabanu (5 mg [bid]), chyba że występują co najmniej dwie z następujących cech: wiek pacjenta wynosi 80 lat lub więcej, masa ciała wynosi 60 kg lub mniej, a stężenie kreatyniny w surowicy wynosi 1,5 mg/dl lub więcej , w takim przypadku wskazane jest zmniejszenie dawki do 2,5 mg dwa razy na dobę.
Skutki uboczne
Krwawienie
Apiksaban może zwiększać ryzyko krwawienia, które może być poważne i potencjalnie śmiertelne. Jednoczesne stosowanie z innymi lekami wpływającymi na krzepliwość krwi może dodatkowo zwiększyć to ryzyko. Obejmuje to leki takie jak inne antykoagulanty, heparyna, aspiryna, leki przeciwpłytkowe, selektywne inhibitory wychwytu zwrotnego serotoniny , inhibitory wychwytu zwrotnego serotoniny i noradrenaliny oraz niesteroidowe leki przeciwzapalne (NLPZ).
Andeksanet alfa to antidotum zatwierdzone przez Agencję ds. Żywności i Leków (FDA) dla apiksabanu u osób z niekontrolowanymi i zagrażającymi życiu krwawieniami.
Nakłucie kręgosłupa
Po znieczuleniu podpajęczynówkowym lub nakłuciu osoby leczone środkami przeciwzakrzepowymi są bardziej narażone na rozwój krwiaka , który może powodować długotrwały lub trwały paraliż. Ryzyko tego można zwiększyć, stosując cewniki nadtwardówkowe lub dooponowe po operacji chirurgicznej lub stosując jednocześnie środki lecznicze, które wpływają na hemostazę .
Historia
Apiksaban został dopuszczony do użytku medycznego w Unii Europejskiej w maju 2011 roku.
Nowa aplikacja leku (NDA) dla zatwierdzenia apiksaban został przekazany do US Food and Drug Administration (FDA) przez Bristol-Myers Squibb (BMS) oraz Pfizer wspólnie po zawarciu Arystoteles badaniu klinicznym w 2011. apiksaban został zatwierdzony do profilaktyka udaru mózgu u osób z migotaniem przedsionków w dniu 28 grudnia 2012 r. W dniu 13 marca 2014 r. została zatwierdzona jako dodatkowe wskazanie profilaktyki zakrzepicy żył głębokich i zatorowości płucnej u osób po przebytej niedawno alloplastyce stawu kolanowego lub biodrowego. 21 sierpnia 2014 r. FDA zatwierdziła apiksaban jako dodatkowe wskazanie w leczeniu nawracającej zakrzepicy żył głębokich i zatorowości płucnej. W trakcie rozwoju lek był znany jako BMS-562247-01. Pod koniec 2019 roku sprzedaż produktu przez BMS stanowiła trzydzieści procent ich kwartalnych przychodów. W grudniu 2019 r. amerykańska FDA zatwierdziła wersję generyczną produkowaną wspólnie przez Mylan i Micro Labs .
Użyj w pandemii COVID-19
NHS jest obecnie trialling użycie apiksaban w leczeniu po odzyskiwania COVID-19 pacjentów.
Bibliografia
Zewnętrzne linki
- „Apiksaban” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
