Alfa-amylaza - Alpha-amylase
| alfa-amylaza | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Identyfikatory | |||||||||
| Nr WE | 3.2.1.0 | ||||||||
| Nr CAS | 9000-90-2 | ||||||||
| Bazy danych | |||||||||
| IntEnz | Widok IntEnz | ||||||||
| BRENDA | Wpis BRENDY | ||||||||
| ExPASy | Widok NiceZyme | ||||||||
| KEGG | Wpis KEGG | ||||||||
| MetaCyc | szlak metaboliczny | ||||||||
| PRIAM | profil | ||||||||
| Struktury WPB | RCSB PDB PDBe Suma PDB | ||||||||
| |||||||||
| Domena katalityczna GH13 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Glukanotransferaza cyklodekstryny (ec2.4.1.19) (cgtase)
| |||||||||
| Identyfikatory | |||||||||
| Symbol | alfa-amylaza | ||||||||
| Pfam | PF00128 | ||||||||
| Klan Pfam | CL0058 | ||||||||
| InterPro | IPR006047 | ||||||||
| SCOP2 | 1ppi / zakres / SUPFAM | ||||||||
| Nadrodzina OPM | 117 | ||||||||
| Białko OPM | 1wza | ||||||||
| CAZy | GH13 | ||||||||
| CDD | cd11338 | ||||||||
| |||||||||
| C-końcowa domena beta-kartki alfa-amylazy | |||||||||
|---|---|---|---|---|---|---|---|---|---|
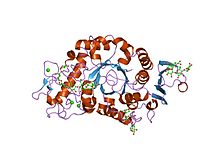 Struktura krystaliczna izozymu 1 alfa-amylazy jęczmienia (amy1) nieaktywnego mutanta d180a w kompleksie z maltoheptaozą
| |||||||||
| Identyfikatory | |||||||||
| Symbol | Alfa-amyl_C2 | ||||||||
| Pfam | PF07821 | ||||||||
| InterPro | IPR012850 | ||||||||
| |||||||||
| Alfa-amylaza, C-końcowa domena all-beta | |||||||||
|---|---|---|---|---|---|---|---|---|---|
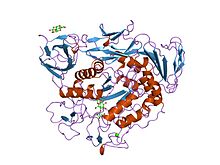 kompleks maltotriozy wstępnie kondycjonowanego mutanta glikozylotransferazy cyklodekstrynowej
| |||||||||
| Identyfikatory | |||||||||
| Symbol | Alfa-amylaza_C | ||||||||
| Pfam | PF02806 | ||||||||
| Klan Pfam | CL0369 | ||||||||
| InterPro | IPR006048 | ||||||||
| SCOP2 | 1ppi / zakres / SUPFAM | ||||||||
| |||||||||
Alfa-amylaza , (α-amylazy) jest enzymem EC 3.2.1.1 który hydrolizuje wiązania alfa wiązania dużych, alfa-linked polisacharydów , takich jak skrobia i glikogenu , uzyskując krótsze łańcuchy jego dekstryny i maltoza . Jest to główna forma amylazy występująca u ludzi i innych ssaków. Jest również obecny w nasionach zawierających skrobię jako zapas pokarmowy i jest wydzielany przez wiele grzybów. Należy do rodziny hydrolaz glikozydowych 13 .
W biologii człowieka
Chociaż znajduje się w wielu tkankach, amylaza jest najbardziej widoczna w soku trzustkowym i ślinie , z których każda ma swoją własną izoformę ludzkiej α-amylazy. Zachowują się różnie przy ogniskowaniu izoelektrycznym i można je również rozdzielić w testach przy użyciu specyficznych przeciwciał monoklonalnych . U ludzi wszystkie izoformy amylazy łączą się z chromosomem 1p21 (patrz AMY1A ).
Amylaza ślinowa (ptyalina)
Amylaza znajduje się w ślinie i rozkłada skrobię na maltozę i dekstrynę . Ta forma amylazy jest nazywany także „ptyalin” / t aɪ əl ɪ n / , który został wybrany przez szwedzkiego chemika Jöns Jacob Berzelius . Nazwa wywodzi się od greckiego słowa πτυω (pluję), ponieważ substancja została uzyskana ze śliny. Rozbija duże, nierozpuszczalne cząsteczki skrobi na skrobie rozpuszczalne ( amylodekstrynę , erytrodekstrynę i akrodekstrynę ), wytwarzając kolejno mniejsze skrobie i ostatecznie maltozę . Ptyalin działa na liniowe wiązania α(1,4) glikozydowe , ale hydroliza związków wymaga enzymu, który działa na produkty rozgałęzione. Amylaza ślinowa jest inaktywowana w żołądku przez kwas żołądkowy . W soku żołądkowym doprowadzonym do pH 3,3 ptialina została całkowicie zdezaktywowana w ciągu 20 minut w temperaturze 37°C. Natomiast 50% aktywności amylazy pozostało po 150 minutach ekspozycji na sok żołądkowy o pH 4,3. Zarówno skrobia będąca substratem dla ptialiny, jak i produkt (krótkie łańcuchy glukozy) są w stanie częściowo chronić ją przed inaktywacją przez kwas żołądkowy. Ptyalina dodana do buforu o pH 3,0 uległa całkowitej inaktywacji w ciągu 120 minut; jednakże dodanie skrobi na poziomie 0,1% skutkowało pozostawaniem 10% aktywności, a podobne dodanie skrobi do poziomu 1,0% skutkowało pozostawieniem około 40% aktywności po 120 minutach.
Optymalne warunki dla ptialiny
- Optymalne pH – 7,0
- Temperatura ciała ludzkiego
- Obecność niektórych anionów i aktywatorów:
Zmienność genetyczna ludzkiej amylazy ślinowej
Gen amylazy ślinowej przeszedł duplikację podczas ewolucji, a badania hybrydyzacji DNA wskazują, że wiele osób ma wiele powtórzeń tandemowych genu. Liczba kopii genów koreluje z poziomami amylazy ślinowej, mierzonymi w testach blottingu białkowego z użyciem przeciwciał przeciwko ludzkiej amylazie. Liczba kopii genów jest związana z widoczną ewolucyjną ekspozycją na diety wysokoskrobiowe. Na przykład Japończyk miał 14 kopii genu amylazy (jeden allel z 10 kopiami i drugi allel z czterema kopiami). Japońska dieta tradycyjnie zawierała duże ilości skrobi ryżowej . W przeciwieństwie do tego, osoba Biaka nosiła sześć kopii (trzy kopie na każdy allel). Biaka są Rainforest myśliwi i zbieracze, którzy tradycyjnie spożywane dietę o niskiej zawartości skrobi. Perry i współpracownicy spekulowali, że zwiększona liczba kopii genu amylazy ślinowej może wpłynąć na poprawę przeżywalności zbiegającą się z przejściem na dietę skrobiową podczas ewolucji człowieka.
Amylaza trzustkowa
Α-amylazy trzustkowej losowo rozszczepia a (1-4), wiązania glikozydowe z amylozy otrzymując dekstryny , maltozy lub maltotriozy . Przyjmuje mechanizm podwójnego przemieszczenia z zachowaniem konfiguracji anomerycznej . U ludzi amylaza ślinowa wyewoluowała z jej kopii.
W patologii
Test na amylazę jest łatwiejszy do wykonania niż test na lipazę , co czyni go podstawowym testem używanym do wykrywania i monitorowania zapalenia trzustki . Laboratoria medyczne zwykle mierzą amylazę trzustkową lub amylazę całkowitą. Jeśli mierzy się tylko amylazę trzustkową, wzrost nie zostanie odnotowany w przypadku świnki lub innych urazów gruczołów ślinowych.
Jednak ze względu na niewielką obecną ilość, czas ma kluczowe znaczenie podczas pobierania krwi do tego pomiaru. Krew należy pobrać wkrótce po ataku bólu związanego z zapaleniem trzustki, w przeciwnym razie jest szybko wydalana przez nerki .
Śliny α-amylaza jest używany jako marker biologiczny dla naprężeń i jako zastępczy marker współczulnego układu nerwowego (SNS) aktywności, który nie wymaga pobierania krwi.
Interpretacja
Podwyższone poziomy w osoczu u ludzi występują w:
- Uraz śliny (w tym intubacja znieczulająca )
- Świnka - z powodu stanu zapalnego z gruczołów ślinowych
- Zapalenie trzustki – z powodu uszkodzenia komórek wytwarzających amylazę
- Niewydolność nerek – z powodu zmniejszonego wydalania
Całkowite odczyty amylazy przekraczające 10 razy górną granicę normy (ULN) sugerują zapalenie trzustki. Od pięciu do dziesięciu razy GGN może wskazywać na niedrożność jelit lub dwunastnicy lub niewydolność nerek, a niższe wartości często występują w chorobie gruczołów ślinowych.
Geny
W ziarnie
Aktywność α-amylazy w ziarnie mierzy się np. za pomocą wskaźnika opadania Hagberga-Pertena , testu do oceny uszkodzeń kiełków lub metody Phadebas . Występuje w pszenicy .
Użytek przemysłowy
α-amylaza jest stosowana w produkcji etanolu do rozbijania skrobi w ziarnach na cukry fermentujące.
Pierwszym etapem produkcji wysokofruktozowego syropu kukurydzianego jest traktowanie skrobi kukurydzianej α-amylazą, wytwarzającą krótsze łańcuchy cukrów oligosacharydów .
α-amylaza zwana „Termamyl”, pochodząca z Bacillus licheniformis , jest również stosowana w niektórych detergentach, zwłaszcza detergentach do zmywania naczyń i usuwających skrobię.
Zobacz amylaza, aby uzyskać więcej ogólnych zastosowań rodziny amylaz.
Potencjał do zastosowań medycznych
α-amylaza wykazała skuteczność w rozkładaniu biofilmów bakteryjnych zawierających wiele drobnoustrojów poprzez hydrolizę wiązań glikozydowych α(1-4) w strukturalnych egzopolisacharydach macierzy zewnątrzkomórkowej substancji polimerycznej (EPS).
Hamowanie bufora
Uważa się, że cząsteczka tris hamuje szereg α-amylaz bakteryjnych, dlatego nie należy ich stosować w buforze tris.
Determinacja
Dostępnych jest kilka metod oznaczania aktywności α-amylazy, a różne branże zwykle opierają się na różnych metodach. Test jodowo-skrobiowy, będący rozwinięciem testu jodowego , opiera się na zmianie koloru, ponieważ α-amylaza rozkłada skrobię i jest powszechnie stosowana w wielu zastosowaniach. Podobnym, ale produkowanym przemysłowo testem jest test amylazy Phadebas , który jest używany jako test jakościowy i ilościowy w wielu gałęziach przemysłu, takich jak detergenty, różne rodzaje mąki, zboża i słodu oraz biologia sądowa.
Architektura domeny
α-amylazy zawierają szereg odrębnych domen białkowych. Katalityczna domena posiada strukturę składającą się z ośmiu nici alfa / beta, baryłki, zawierający miejsce aktywne, przerwaną przez ~ 70- aminokwasowej domeny wiążące wapń wystający między nici beta 3 i alfa helisy 3 i C-końcu Greek kluczowa domena beta-beczki . Kilka alfa-amylaz zawiera domenę arkusza beta, zwykle na końcu C. Ta domena jest zorganizowana jako pięcioniciowy antyrównoległy arkusz beta. Kilka alfa-amylaz zawiera domenę całkowicie beta, zwykle na końcu C.
Zobacz też
Bibliografia
Zewnętrzne linki
- Białko alfa-amylazy
- alfa-amylaza w amerykańskiej National Library of Medicine Medical Subject Headings (MeSH)
