Dyfuzja powierzchniowa - Surface diffusion

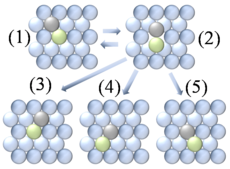
Dyfuzja powierzchniowa to ogólny proces obejmujący ruch adatomów , cząsteczek i klastrów atomowych ( cząstek adnotacji ) na powierzchniach materiałów stałych . Ogólnie proces ten można rozpatrywać w kategoriach cząstek przeskakujących między sąsiednimi miejscami adsorpcji na powierzchni, jak na rysunku 1. Podobnie jak w przypadku dyfuzji masowej , ruch ten jest zwykle procesem wspomaganym termicznie, z szybkością wzrastającą wraz ze wzrostem temperatury. Wiele systemów wykazuje zachowanie dyfuzyjne, które odbiega od konwencjonalnego modelu skoków najbliższego sąsiada. Dyfuzja tunelowa jest szczególnie interesującym przykładem niekonwencjonalnego mechanizmu, w którym wodór dyfunduje na czyste powierzchnie metalu poprzez efekt tunelowania kwantowego .
Do wyjaśnienia mechanizmów i szybkości dyfuzji powierzchniowej można wykorzystać różne narzędzia analityczne , z których najważniejsze to polowa mikroskopia jonowa i skaningowa mikroskopia tunelowa . Chociaż w zasadzie proces może przebiegać na różnych materiałach, większość eksperymentów przeprowadza się na krystalicznych powierzchniach metalowych. Z powodu ograniczeń eksperymentalnych większość badań dyfuzji powierzchniowej są ograniczone do znacznie poniżej temperatury topnienia z podłożem , a wiele ma jeszcze do odkrycia dotyczące jak te procesy odbywają się w wyższych temperaturach.
Na szybkość i mechanizmy dyfuzji powierzchniowej wpływa szereg czynników, w tym siła wiązania powierzchniowo-cząsteczka , orientacja sieci powierzchniowej, przyciąganie i odpychanie między gatunkami powierzchniowymi oraz chemiczne gradienty potencjału . Jest to ważna koncepcja dotycząca tworzenia się fazy powierzchniowej , wzrostu epitaksjalnego , katalizy heterogenicznej i innych zagadnień z dziedziny nauki o powierzchni . Jako takie, zasady dyfuzji powierzchniowej mają kluczowe znaczenie dla produkcji chemicznej i przemysłu półprzewodników . Rzeczywiste zastosowania w dużym stopniu polegające na tych zjawiskach obejmują konwertery katalityczne , układy scalone używane w urządzeniach elektronicznych oraz sole halogenków srebra używane w kliszach fotograficznych .
Kinetyka
Kinetykę dyfuzji powierzchniowej można rozpatrywać w kategoriach adatomów znajdujących się w miejscach adsorpcji w sieci 2D , przemieszczających się między sąsiednimi (najbliższymi sąsiadami) miejscami adsorpcji w procesie skokowym. Częstotliwość skoków charakteryzuje się częstotliwością prób i czynnikiem termodynamicznym , który określa prawdopodobieństwo, że próba zakończy się sukcesem. Częstotliwość próby ν jest zwykle przyjmowana jako po prostu częstotliwość drgań adatomu, podczas gdy czynnik termodynamiczny to czynnik Boltzmanna zależny od temperatury i E diff , potencjalnej bariery energetycznej dla dyfuzji. Równanie 1 opisuje zależność:
Gdzie ν i E diff są takie, jak opisano powyżej, Γ jest szybkością przeskoku, T jest temperaturą, a k B jest stałą Boltzmanna . E diff musi być mniejsza niż energia desorpcji, aby nastąpiła dyfuzja, w przeciwnym razie dominowałyby procesy desorpcji. Co ważne, równanie 1 mówi nam, jak silnie szybkość przeskoku zmienia się wraz z temperaturą. Sposób, w jaki zachodzi dyfuzja, zależy od relacji między E diff i k B T, jak podano we współczynniku termodynamicznym: gdy E diff <k B T czynnik termodynamiczny zbliża się do jedności, a E diff przestaje być znaczącą barierą dla dyfuzji . Ten przypadek, znany jako mobilna dyfuzja , jest stosunkowo rzadki i został zaobserwowany tylko w kilku systemach. Dla zjawisk opisanych w tym artykule przyjmuje się, że E diff >> k B T, a zatem Γ << ν . W przypadku dyfuzji Ficka , że jest możliwe, aby wyodrębnić zarówno v i E Diff z wykresie Arrheniusa logarytmu współczynnika dyfuzji D , w porównaniu z 1 / T . W przypadkach, w których występuje więcej niż jeden mechanizm dyfuzji (patrz poniżej), może występować więcej niż jeden współczynnik dyfuzji E, tak że względny rozkład między różnymi procesami zmienia się wraz z temperaturą.
Statystyki wędrówek losowych opisują średnie kwadratowe przemieszczenie gatunków dyfuzyjnych pod względem liczby skoków N i odległości na skok a . Liczbę udanych skoków mnoży się po prostu Γ przez czas dyfuzji, t . W najbardziej podstawowym modelu uwzględniane są tylko skoki najbliższego sąsiada, a a odpowiada odległości między najbliższymi sąsiadującymi miejscami adsorpcji. Pierwiastkowa średnia kwadratowa przemieszczenia wygląda następująco:
Współczynnik dyfuzji podaje się jako:
gdzie dla dyfuzji 1D, jak w przypadku dyfuzji w kanale, dyfuzji 2D i dyfuzji 3D.
Reżimy
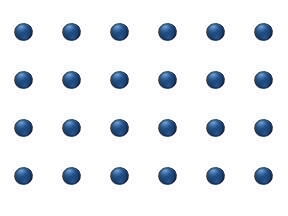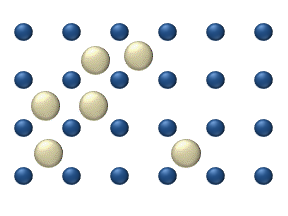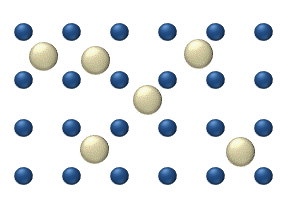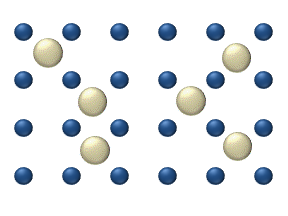
Istnieją cztery różne ogólne schematy, w których może mieć miejsce dyfuzja. Dyfuzja znacznika i dyfuzja chemiczna różnią się stopniem pokrycia adsorbatu na powierzchni, natomiast dyfuzja wewnętrzna i dyfuzja z transferu masy różnią się charakterem środowiska dyfuzyjnego. Zarówno dyfuzja znacznika, jak i dyfuzja wewnętrzna, odnoszą się do systemów, w których cząsteczki adnotacji doświadczają stosunkowo jednorodnego środowiska, podczas gdy w dyfuzji chemicznej i dyfuzji masy cząsteczki są silniej zależne od otoczenia.
- Dyfuzja znacznika opisuje ruch pojedynczych cząstek na powierzchni przy stosunkowo niskim poziomie pokrycia. Na tych niskich poziomach (<0,01 monowarstwy ) oddziaływanie cząstek jest niskie i można uznać, że każda cząstka porusza się niezależnie od innych. Dyfuzja pojedynczego atomu na ryc. 1 jest dobrym przykładem dyfuzji znacznika.
- Dyfuzja chemiczna opisuje proces na wyższym poziomie pokrycia, w którym wpływ przyciągania lub odpychania między atomami staje się ważny. Te interakcje służą do zmiany ruchliwości atomów. W uproszczony sposób rysunek 3 służy do pokazania, jak adatomy mogą oddziaływać na wyższe poziomy pokrycia. Adatomy nie mają innego „wyboru”, jak najpierw przesunąć się w prawo, a sąsiednie adatomy mogą blokować miejsca adsorpcji od siebie.
- Dyfuzja wewnętrzna zachodzi na jednolitej powierzchni (np. Bez stopni lub wolnych miejsc ), takiej jak pojedynczy taras, na którym nie ma pułapek ani źródeł adatomów. Ten tryb jest często badany przy użyciu polowej mikroskopii jonowej , w której taras jest ostrą końcówką próbki, na której dyfunduje cząsteczka. Nawet w przypadku czystego tarasu na proces może wpływać nierównomierność przy krawędziach tarasu.
- Dyfuzja w wyniku transferu masy ma miejsce w przypadku występowania źródeł cząstek i pułapek, takich jak załamania, stopnie i luki. Zamiast być zależna tylko od skoku barierę potencjału E diff , dyfuzja w tym systemie jest również zależny od energii formacji adparticles mobilnych. Dokładny charakter środowiska dyfuzyjnego odgrywa zatem rolę w decydowaniu o szybkości dyfuzji, ponieważ energia formowania się cząsteczki jest różna dla każdego typu cechy powierzchni, jak opisano w modelu Terrace Ledge Kink .
Anizotropia
Anizotropia orientacyjna przybiera postać różnic w szybkościach i mechanizmach dyfuzji przy różnych orientacjach powierzchni danego materiału. Dla danego materiału krystalicznego każda płaszczyzna wskaźnika Millera może wykazywać unikalne zjawisko dyfuzji. Ściśle upakowane powierzchnie, takie jak fcc (111), mają zwykle wyższe szybkości dyfuzji niż odpowiednio bardziej „otwarte” powierzchnie tego samego materiału, takie jak fcc (100).
Anizotropia kierunkowa odnosi się do różnicy w mechanizmie lub szybkości dyfuzji w określonym kierunku na danej płaszczyźnie krystalograficznej. Różnice te mogą wynikać albo z anizotropii w sieci powierzchniowej (np. Krata prostokątna ), albo z obecności stopni na powierzchni. Jednym z bardziej dramatycznych przykładów anizotropii kierunkowej jest dyfuzja adatomów na powierzchniach kanałowych, takich jak fcc (110), gdzie dyfuzja wzdłuż kanału jest znacznie szybsza niż dyfuzja przez kanał.
Mechanizmy
Dyfuzja adatomów
Dyfuzja adatomów może zachodzić za pośrednictwem różnych mechanizmów. Sposób, w jaki dyfundują, jest ważny, ponieważ może dyktować między innymi kinetykę ruchu, zależność od temperatury i ogólną mobilność gatunków powierzchniowych. Poniżej znajduje się podsumowanie najważniejszych z tych procesów:
- Podskakiwanie lub skakanie jest koncepcyjnie najbardziej podstawowym mechanizmem dyfuzji atomów. W tym modelu adatomy znajdują się w miejscach adsorpcji na siatce powierzchniowej. Ruch następuje poprzez kolejne skoki do sąsiednich miejsc, których liczba zależy od rodzaju sieci powierzchniowej. Ryciny 1 i 3 przedstawiają adatomy ulegające dyfuzji w procesie chmielenia. Badania wykazały obecność metastabilnych stanów przejściowych między miejscami adsorpcji, w których możliwe jest tymczasowe przebywanie adatomów.
- Wymiana atomowa polega na wymianie pomiędzy adatomem a sąsiednim atomem w sieci powierzchniowej. Jak pokazano na ryc. 4, po zdarzeniu wymiany atomowej adatom zajął miejsce atomu powierzchniowego, a atom powierzchniowy został przemieszczony i stał się teraz atomem. Proces ten może zachodzić zarówno w heterodyfuzji (np. Adatomy Pt na Ni ), jak i autodyfuzji (np. Adatomy Pt na Pt). Z teoretycznego punktu widzenia nadal nie jest jasne, dlaczego mechanizm wymiany atomowej dominuje w niektórych systemach niż w innych. Obecna teoria wskazuje na wiele możliwości, w tym naprężenia powierzchniowe rozciągające, relaksację powierzchniową wokół adatomu i zwiększoną stabilność półproduktu ze względu na fakt, że oba zaangażowane atomy utrzymują wysoki poziom koordynacji w całym procesie.
- Dyfuzja tunelowa jest fizyczną manifestacją efektu tunelowania kwantowego obejmującego tunelowanie cząstek przez bariery dyfuzyjne. To może nastąpić w przypadku niskiego poziomu cząstek rozpraszający masy i niskiej E diff i zaobserwowano w przypadku wodoru dyfuzję w wolframu i miedzi powierzchni. Zjawisko to jest wyjątkowe, ponieważ w reżimie, w którym dominuje mechanizm tunelowania, szybkość dyfuzji jest prawie niezależna od temperatury.
- Dyfuzja pustostanów może występować jako dominująca metoda dyfuzji powierzchniowej przy wysokich poziomach pokrycia, zbliżających się do całkowitego pokrycia. Ten proces jest podobny do sposobu, w jaki elementy przesuwają się w „ przesuwanej układance ”. Bezpośrednia obserwacja dyfuzji w pustostanie jest bardzo trudna ze względu na zwykle wysokie szybkości dyfuzji i niskie stężenie pustostanów . Rysunek 5 przedstawia podstawowy motyw tego mechanizmu w aczkolwiek uproszczony sposób.
Najnowsze prace teoretyczne, a także prace eksperymentalne prowadzone od końca lat siedemdziesiątych XX wieku ujawniły niezwykłą różnorodność zjawisk dyfuzji powierzchniowej, zarówno w odniesieniu do kinetyki, jak i mechanizmów. Poniżej znajduje się podsumowanie niektórych z bardziej znaczących zjawisk:
- Skoki w dal polegają na przemieszczeniu adatomu do miejsca adsorpcji, które nie jest najbliższym sąsiadem. Mogą obejmować podwójne, potrójne i dłuższe skoki w tym samym kierunku, w którym przeskoczyłby skok najbliższego sąsiada, lub mogą odbywać się w zupełnie innych kierunkach, jak pokazano na rysunku 6. Teoria przewiduje, że istnieją w wielu różnych systemach, i jak wykazano eksperymentalnie, zachodziły w temperaturach tak niskich jak 0,1 T m (temperatura topnienia). W niektórych przypadkach dane wskazują, że długie skoki dominują w procesie dyfuzji w porównaniu z pojedynczymi skokami w podwyższonych temperaturach; zjawisko o różnych długościach skoku wyraża się w różnych charakterystycznych rozkładach przemieszczenia atomu w czasie (patrz rysunek 7).
- Eksperymenty i symulacje wykazały, że skoki odbicia mają miejsce w niektórych systemach. Ponieważ ruch nie powoduje przemieszczenia netto zaangażowanego adatomu, eksperymentalne dowody na skoki odbicia ponownie pochodzą ze statystycznej interpretacji rozkładów atomowych. Skok z odbicia pokazano na rysunku 6. Rysunek jest jednak nieco mylący, ponieważ skoki odbicia zostały wykazane eksperymentalnie tylko w przypadku dyfuzji 1D na powierzchni kanałowej (w szczególności na powierzchni bcc (211) wolframu ).
- W przypadku powierzchni kanałowych może wystąpić dyfuzja międzykanałowa . Zwykle dominuje dyfuzja w kanale ze względu na niższą barierę energetyczną dla dyfuzji tego procesu. W niektórych przypadkach wykazano występowanie kanałów krzyżowych, zachodzących w sposób podobny do tego pokazanego na fig. 8. Pośrednia pozycja „hantli” może prowadzić do rozmaitych końcowych przemieszczeń atomów adatomu i powierzchni.
- Wymiana atomowa na duże odległości jest procesem polegającym na wprowadzaniu adatomu do powierzchni, jak w normalnym mechanizmie wymiany atomowej, ale zamiast atomu najbliższego sąsiada jest to atom znajdujący się w pewnej odległości od początkowego adatomu, który się wyłania. Przedstawiony na rysunku 9 proces ten został zaobserwowany tylko w symulacjach dynamiki molekularnej i nie został jeszcze potwierdzony eksperymentalnie. Pomimo tej wymiany atomowej na duże odległości, jak również szeregu innych egzotycznych mechanizmów dyfuzyjnych, przewiduje się, że będą się one znacząco przyczyniać w temperaturach obecnie zbyt wysokich do bezpośredniej obserwacji.
Dyfuzja klastrów
Dyfuzja klastrów obejmuje ruch klastrów atomów o różnej wielkości, od dimerów do wysp zawierających setki atomów. Ruch gromady może nastąpić poprzez przemieszczenie pojedynczych atomów, odcinków gromady lub całego gromada poruszającego się naraz. Wszystkie te procesy obejmują zmianę środka masy klastra .
-
Poszczególne mechanizmy to takie, które obejmują ruch jednego atomu na raz.
- Dyfuzja brzegowa obejmuje ruch gruczołów lub pustek w miejscach krawędzi lub załamań. Jak pokazano na rysunku 10, ruchomy atom utrzymuje swoją bliskość do klastra podczas całego procesu.
- Parowanie-kondensacja polega na „ odparowywaniu ” atomów ze skupiska na taras, czemu towarzyszy „ kondensacja ” adatomów tarasowych na gromadzie, co prowadzi do zmiany środka masy klastra. Podczas gdy rysunek 10 wydaje się wskazywać, że ten sam atom paruje i kondensuje się na gromadzie, w rzeczywistości może to być inny atom kondensujący się z gazu 2D.
- Dyfuzja Leapfrog jest podobna do dyfuzji krawędziowej, z tą różnicą, że dyfuzyjny atom faktycznie porusza się na szczycie gromady, zanim osiądzie w innym miejscu niż jego pozycja początkowa.
- Przesunięcie sekwencyjne odnosi się do procesu obejmującego ruch jednego atomu na raz, przemieszczania się do wolnych miejsc najbliższych sąsiadów.
 |
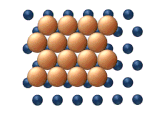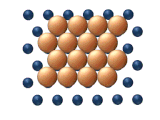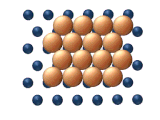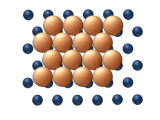
|
| (a) Zwichnięcie | (b) Szybowanie |
 |
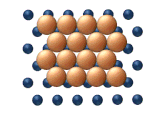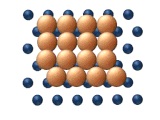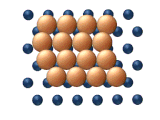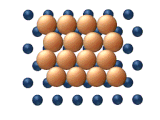
|
| (c) Reptacja | (d) Ścinanie |
| Rysunek 11. Uzgodnione mechanizmy dyfuzji klastrów. | |
-
Uzgodnione mechanizmy to takie, które obejmują ruch jednej z sekcji klastra lub całego klastra jednocześnie.
- Dyfuzja dyslokacji występuje, gdy sąsiednie podjednostki klastra poruszają się rząd po rzędzie poprzez przemieszczenie dyslokacji . Jak pokazano na rysunku 11 (a), proces rozpoczyna się od zarodkowania dyslokacji, po której następuje zasadniczo sekwencyjne przemieszczenie na uzgodnionej podstawie.
- Glide diffusion odnosi się do skoordynowanego ruchu całej gromady naraz (patrz rysunek 11 (b)).
- Reptacja to ruch podobny do węża (stąd nazwa) obejmujący sekwencyjny ruch podjednostek klastra (patrz rysunek 11 (c)).
- Ścinanie to skoordynowane przemieszczenie podjednostki atomów w klastrze (patrz rysunek 11 (d)).
- Zależność od wielkości : szybkość dyfuzji klastra jest silnie zależna od wielkości klastra, przy czym większy rozmiar klastra ogólnie odpowiada wolniejszej dyfuzji. Nie jest to jednak trend uniwersalny iw niektórych układach wykazano, że tempo dyfuzji przybiera okresową tendencję, w której niektóre większe klastry dyfundują szybciej niż mniejsze od nich.
Dyfuzja powierzchniowa i kataliza heterogeniczna
Dyfuzja powierzchniowa jest pojęciem krytycznie ważnym w katalizie heterogenicznej, ponieważ szybkość reakcji jest często podyktowana zdolnością reagentów do „znajdowania się” siebie nawzajem na powierzchni katalizatora. W przypadku cząsteczek zaadsorbowanych w podwyższonej temperaturze fragmenty molekularne, atomy i klastry mają zwykle znacznie większą ruchliwość (patrz równanie 1). Jednak wraz ze wzrostem temperatury czas życia adsorpcji zmniejsza się, ponieważ współczynnik k B T staje się wystarczająco duży, aby zaadsorbowane substancje pokonały barierę desorpcji Q (patrz rysunek 2). Pomijając termodynamikę reakcji, ze względu na wzajemne oddziaływanie między zwiększonymi szybkościami dyfuzji i zmniejszoną żywotnością adsorpcji, podwyższona temperatura może w niektórych przypadkach zmniejszyć całkowitą szybkość reakcji.
Eksperymentalny
Dyfuzję powierzchniową można badać różnymi technikami, w tym obserwacjami bezpośrednimi i pośrednimi. Dwie techniki eksperymentalne, które okazały się bardzo przydatne w tej dziedzinie badań, to polowa mikroskopia jonowa i skaningowa mikroskopia tunelowa . Wizualizując przemieszczanie się atomów lub klastrów w czasie, można uzyskać użyteczne informacje dotyczące sposobu, w jaki dany gatunek dyfunduje - zarówno informacje mechaniczne, jak i związane z szybkością. Aby zbadać dyfuzję powierzchniową w skali atomistycznej, niestety konieczne jest wykonanie badań na powierzchniach ściśle czystych oraz w warunkach ultra wysokiej próżni (UHV) lub w obecności niewielkich ilości gazu obojętnego , jak ma to miejsce przy stosowaniu He lub Ne jako gaz obrazujący w eksperymentach polowej mikroskopii jonowej .
Zobacz też
Bibliografia
Cytowane prace
- G. Antczak, G. Ehrlich. Surface Science Reports 62 (2007), 39-61. (Przejrzeć)
- Oura, K .; VG Lifshits; AA Saranin; AV Zotov; M. Katayama (2003). Nauka o powierzchni: wprowadzenie . Springer-Verlag Berlin Heidelberg. ISBN 3-540-00545-5 .
- Shustorovich, E. (1991). Energetyka reakcji metal-powierzchnia: teoria i zastosowania do heterogenicznej katalizy, chemisorpcji i dyfuzji powierzchniowej . VCH Publishers, Inc. ISBN 3-527-27938-5 .