Zasolenie - Salinity
| Część serii na |
| Zasolenie wody |
|---|
 |
| Poziomy zasolenia |
|
Świeżej wody (<0,05%) Słonawa wody (0,05-3%) Roztwór soli woda (3-5%) solanka (> 5% do 26% -28% max) |
| Zbiorniki wodne |
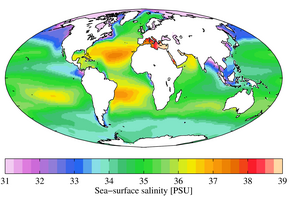
Zasolenie ( / e ə l ɪ n ɪ T i / ) jest słoność lub ilość soli rozpuszcza się w organizmie wody , zwana woda roztwór soli (patrz także zasolenie gleby ). Zwykle jest mierzona wg/L lub g/kg (gramy soli na litr/kilogram wody; ta ostatnia jest bezwymiarowa i równa ‰).
Zasolenie jest ważnym czynnikiem determinującym wiele aspektów chemizmu wód naturalnych i procesów biologicznych w nich zachodzących, a także jest zmienną stanu termodynamicznego, która wraz z temperaturą i ciśnieniem rządzi właściwościami fizycznymi, takimi jak gęstość i pojemność cieplna wody.
Linia konturowa o stałym zasoleniu nazywana jest izohaliną lub czasami isohale .
Definicje
Zasolenie rzek, jezior i oceanów jest koncepcyjnie proste, ale technicznie trudne do precyzyjnego zdefiniowania i zmierzenia. Koncepcyjnie zasolenie to ilość rozpuszczonej soli w wodzie. Sole to związki takie jak chlorek sodu , siarczan magnezu , azotan potasu i wodorowęglan sodu, które rozpuszczają się w jony. Stężenie rozpuszczonych jonów chlorkowych jest czasami określane jako chlorowość. Pod względem operacyjnym materia rozpuszczona jest definiowana jako ta, która może przejść przez bardzo drobny filtr (historycznie filtr o wielkości porów 0,45 μm, obecnie zwykle 0,2 μm). Zasolenie można wyrazić w postaci ułamka masowego , tj. masy rozpuszczonego materiału w jednostce masy roztworu.
Woda morska zazwyczaj ma masowe zasolenie około 35 g/kg, chociaż niższe wartości są typowe w pobliżu wybrzeży, gdzie rzeki wpływają do oceanu. Rzeki i jeziora mogą mieć szeroki zakres zasolenia, od mniej niż 0,01 g/kg do kilku g/kg, chociaż istnieje wiele miejsc, w których występuje wyższe zasolenie. Dead Sea ma zasolenie więcej niż 200 g / kg. Woda deszczowa przed zetknięciem się z ziemią ma zazwyczaj TDS 20 mg/L lub mniej.
Bez względu na wielkość porów użytą w definicji, wynikowa wartość zasolenia danej próbki wody naturalnej nie będzie się różnić o więcej niż kilka procent (%). Jednak oceanografowie fizyczni pracujący w oceanie głębinowym często troszczą się o precyzję i porównywalność pomiarów dokonywanych przez różnych badaczy w różnym czasie, do prawie pięciu cyfr znaczących. Produkt butelkowanej wody morskiej znany jako IAPSO Standard Seawater jest używany przez oceanografów do standaryzacji ich pomiarów z wystarczającą precyzją, aby spełnić to wymaganie.
Kompozycja
Trudności związane z pomiarem i definicją pojawiają się, ponieważ wody naturalne zawierają złożoną mieszaninę wielu różnych pierwiastków z różnych źródeł (nie wszystkie z rozpuszczonych soli) w różnych formach molekularnych. Właściwości chemiczne niektórych z tych form zależą od temperatury i ciśnienia. Wiele z tych form jest trudnych do zmierzenia z dużą dokładnością, aw każdym razie pełna analiza chemiczna nie jest praktyczna przy analizie wielu próbek. Różne praktyczne definicje zasolenia wynikają z różnych prób wyjaśnienia tych problemów, z różnym stopniem precyzji, a jednocześnie pozostają w miarę łatwe w użyciu.
Ze względów praktycznych zasolenie jest zwykle związane z sumą mas podzbioru tych rozpuszczonych składników chemicznych (tzw. zasolenie roztworu ), a nie z nieznaną masą soli, która dała początek temu składowi (wyjątkiem jest sytuacja, gdy sztuczna woda morska jest Utworzony). Dla wielu celów suma ta może być ograniczona do zestawu ośmiu głównych jonów w wodach naturalnych, chociaż dla wody morskiej z najwyższą precyzją uwzględniono również dodatkowe siedem mniejszych jonów. Główne jony dominują w nieorganicznym składzie większości (ale nie wszystkich) naturalnych wód. Wyjątkiem są niektóre jeziora wykopowe i wody z niektórych źródeł hydrotermalnych .
Stężenia rozpuszczonych gazów, takich jak tlen i azot, zwykle nie są uwzględniane w opisach zasolenia. Jednak często zawiera się gazowy dwutlenek węgla , który po rozpuszczeniu jest częściowo przekształcany w węglany i wodorowęglany . Krzem w postaci kwasu krzemowego , który zwykle występuje jako obojętna cząsteczka w zakresie pH większości wód naturalnych, może być również włączony do niektórych celów (np. gdy badane są relacje zasolenie/gęstość).
Woda morska
Termin „zasolenie” jest dla oceanografów zwykle kojarzony z jedną z określonych technik pomiarowych. W miarę ewolucji dominujących technik zmieniają się również różne opisy zasolenia. Zasolenie mierzono w dużej mierze za pomocą technik opartych na miareczkowaniu przed latami osiemdziesiątymi. Miareczkowanie azotanem srebra może być wykorzystane do określenia stężenia jonów halogenkowych (głównie chloru i bromu ) w celu uzyskania chloru . Chlorowość została następnie pomnożona przez współczynnik, aby uwzględnić wszystkie inne składniki. Wynikowe „zasolenia Knudsena” są wyrażone w jednostkach części na tysiąc (ppt lub ‰ ).
Wykorzystanie pomiarów przewodności elektrycznej do oszacowania zawartości jonów w wodzie morskiej doprowadziło do opracowania skali zwanej praktyczną skalą zasolenia 1978 (PSS-78). Zasolenia mierzone za pomocą PSS-78 nie mają jednostek.Przyrostek psu lub PSU (oznaczający praktyczną jednostkę zasolenia ) jest czasami dodawany do wartości pomiarowych PSS-78. Dodanie PSU jako jednostki po wartości jest „formalnie niepoprawne i zdecydowanie odradzane”.
W 2010 roku wprowadzono nowy standard właściwości wody morskiej nazwany równaniem termodynamicznym wody morskiej 2010 ( TEOS-10 ), zalecający zasolenie bezwzględne jako zastąpienie zasolenia praktycznego i temperaturę konserwatywną za zastąpienie temperatury potencjalnej . Norma ta zawiera nową skalę zwaną skalą zasolenia składu odniesienia . Zasolenie bezwzględne w tej skali jest wyrażone jako ułamek masowy w gramach na kilogram roztworu. Zasolenie w tej skali określa się, łącząc pomiary przewodności elektrycznej z innymi informacjami, które mogą uwzględniać regionalne zmiany w składzie wody morskiej. Można je również określić, wykonując bezpośrednie pomiary gęstości.
Próbka wody morskiej z większości lokalizacji o chlorowaniu 19,37 ppt będzie miała zasolenie Knudsena 35,00 ppt, zasolenie praktyczne PSS-78 około 35,0 i zasolenie absolutne TEOS-10 około 35,2 g/kg. Przewodność elektryczna tej wody w temperaturze 15°C wynosi 42,9 mS/cm.
Jeziora i rzeki
Limnolodzy i chemicy często definiują zasolenie w postaci masy soli na jednostkę objętości, wyrażonej w jednostkach mg na litr lub g na litr. Sugeruje się, choć często nie stwierdza się, że ta wartość ma zastosowanie tylko w pewnej temperaturze odniesienia. Przedstawione w ten sposób wartości są zazwyczaj z dokładnością rzędu 1%. Limnolodzy stosują również przewodnictwo elektryczne lub „przewodność referencyjną”, jako wskaźnik zasolenia. Pomiar ten może być skorygowany o wpływ temperatury i jest zwykle wyrażany w jednostkach μS/cm.
Woda w rzekach lub jeziorach o zasoleniu około 70 mg/l zazwyczaj ma przewodność właściwą w temperaturze 25°C między 80 a 130 μS/cm. Rzeczywisty stosunek zależy od obecnych jonów. Rzeczywista przewodność zwykle zmienia się o około 2% na stopień Celsjusza, więc zmierzona przewodność w temperaturze 5 °C może mieścić się tylko w zakresie 50–80 μS/cm.
Do szacowania zasolenia, szczególnie w jeziorach o wysokim zasoleniu, wykorzystuje się również bezpośrednie pomiary gęstości . Czasami gęstość w określonej temperaturze jest używana jako wskaźnik zasolenia. W innych przypadkach empiryczna zależność zasolenie/gęstość opracowana dla konkretnego akwenu jest wykorzystywana do oszacowania zasolenia próbek na podstawie zmierzonej gęstości.
| Zasolenie wody | |||
|---|---|---|---|
| Świeża woda | Woda słonawa | Woda słona | Solanka |
| < 0,05% | 0,05 – 3% | 3 – 5% | > 5% |
| < 0,5 | 0,5 – 30 | 30 – 50 | > 50 |
Klasyfikacja zbiorników wodnych na podstawie zasolenia
| Seria talasowa |
| > 300 |
| hiperhaliczny |
| 60–80 |
| metahalina |
| 40 |
| miksoeuhalina |
| 30 dni |
| wielohalogenkowy |
| 18 lat |
| mezohalina |
| 5 dni |
| oligohalinowy |
| 0,5 |
Wody morskie to wody oceanu, inne określenie to morza euhaliczne . Zasolenie mórz euhalicznych wynosi od 30 do 35 ‰. Morza lub wody słonawe mają zasolenie w zakresie od 0,5 do 29 , a morza metahaliczne od 36 do 40 ‰. Wszystkie te wody są uważane za talasowe, ponieważ ich zasolenie pochodzi z oceanu i jest definiowane jako homoiohalinowe, jeśli zasolenie nie zmienia się znacznie w czasie (w zasadzie stałe). Tabela po prawej, zmodyfikowana z Por (1972), podąża za „systemem weneckim” (1959).
W przeciwieństwie do środowisk homoiohalinowych istnieją pewne środowiska poikilohalinowe (które mogą być również talassiowe ), w których zmienność zasolenia jest istotna biologicznie. Zasolenie wody poikilohalinowej może wynosić od 0,5 do ponad 300 ‰. Ważną cechą jest to, że wody te mają tendencję do różnicowania zasolenia w pewnym biologicznie znaczącym zakresie sezonowo lub w innej mniej więcej porównywalnej skali czasowej. Mówiąc prościej, są to zbiorniki wodne o dość zmiennym zasoleniu.
Woda silnie zasolona, z której krystalizują (lub wkrótce nastąpią) sole, nazywana jest solanką .
Względy środowiskowe
Zasolenie to czynnik ekologiczny o dużym znaczeniu, mający wpływ na rodzaje organizmów żyjących w zbiorniku wodnym. Zasolenie wpływa również na rodzaje roślin, które będą rosły w zbiorniku wodnym lub na lądzie zasilanym wodą (lub wodą gruntową ). Roślina przystosowana do warunków zasolonych nazywana jest halofitem . Halofity, odporny na resztkową węglanu sodu zasolenia nazywane solirodem lub saltwort lub Barilla rośliny. Organizmy (głównie bakterie), które mogą żyć w bardzo zasolonych warunkach, są klasyfikowane jako ekstremofile lub konkretnie halofile . Organizmem, który może wytrzymać szeroki zakres zasolenia jest euryhalina .
Usuwanie soli z wody jest drogie, a zawartość soli jest ważnym czynnikiem w zużyciu wody (takim jak zdatność do picia ). Wzrost zasolenia zaobserwowano w jeziorach i rzekach w Stanach Zjednoczonych, z powodu spływania soli drogowej i innych soli odladzających .
Stopień zasolenia oceanów jest motorem światowej cyrkulacji oceanicznej , gdzie zmiany gęstości spowodowane zarówno zmianami zasolenia, jak i zmianami temperatury na powierzchni oceanu powodują zmiany wyporu, co powoduje zatapianie i podnoszenie się mas wody. Uważa się, że zmiany w zasoleniu oceanów przyczyniają się do globalnych zmian dwutlenku węgla, ponieważ bardziej zasolone wody są mniej rozpuszczalne w dwutlenku węgla. Ponadto w okresach lodowcowych hydrografia jest taka, że możliwą przyczyną zmniejszonej cyrkulacji jest produkcja warstwowych oceanów. W takich przypadkach trudniej jest odprowadzić wodę przez obieg termohalinowy.
Zobacz też
- Odsalanie do celów gospodarczych
- Odsalanie wody
- Odsalanie gleby: kontrola zasolenia gleby
- Współczynnik adsorpcji sodu
- Pomiar zasolenia
- Zasolenie w kontekście biologicznym
- W organizmach ogólnie, ze szczególnym uwzględnieniem zdrowia człowieka
- W roślinach
- W rybach
- Zasolenie według kontekstu geologicznego
- Świeża woda
- Woda morska
- Zasolenie gleby
- Cyrkulacja termohalinowa
- Paleosaliność
- Dane z zestawu danych CORA dotyczące zasolenia globalnych oceanów
- Ogólne przypadki koncentracji substancji rozpuszczonych
Bibliografia
Dalsza lektura
- Mantyla, AW (1987). „Zaktualizowano standardowe porównania wody morskiej” . J. Fiz. Oceanogr. 17 (4): 543–548. Kod Bibcode : 1987JPO....17..543M . doi : 10.1175/1520-0485(1987)017<0543:sscu>2.0.co;2 .
- Strona MIT dotycząca właściwości wody morskiej, z procedurami biblioteki Matlab, EES i Excel VBA
- Równania i algorytmy obliczania podstawowych właściwości wody morskiej.
- Historia oznaczania zasolenia
- Praktyczna skala zasolenia 1978.
- Kalkulator zasolenia
- Lewis, EL 1982. Praktyczna skala zasolenia 1978 i jej poprzednicy. Geodezja Morska. 5(4):350–357.
- Równania i algorytmy obliczania zasolenia wód śródlądowych


