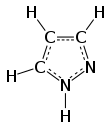
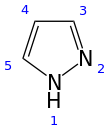
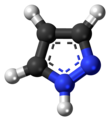
Pirazol - Pyrazole
|
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
1 H- pirazol |
|||
|
Systematyczna nazwa IUPAC
1,2-Diazacyklopenta-2,4-dien |
|||
| Inne nazwy
1,2-diazol
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Karta informacyjna ECHA |
100.005.471 |
||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 3 H 4 N 2 | |||
| Masa cząsteczkowa | 68,079 g·mol -1 | ||
| Temperatura topnienia | 66 do 70 °C (151 do 158 °F; 339 do 343 K) | ||
| Temperatura wrzenia | 186 do 188 °C (367 do 370 °F; 459 do 461 K) | ||
| Zasadowość (p K b ) | 11,5 | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Pirazolu jest organiczny związek o wzorze C 3 H 3 N 2 H. Jest to heterocykl charakteryzuje się 5-członowy pierścień o trzech atomach węgla, a dwa sąsiednie atomy azotu. Pirazolu jest słaba zasada, gdzie p K b 11,5 (p K A kwasu sprzężonego 2,49 w temperaturze 25 ° C). Pirazole są również klasę związków, które mają pierścień C 3 N 2 z sąsiednimi atomami azotu. Godnymi uwagi lekami zawierającymi pierścień pirazolowy są celekoksyb (Celebrex) i steryd anaboliczny stanozolol .
Przygotowanie i reakcje
Pirazole są syntetyzowane w reakcji α,β-nienasyconych aldehydów z hydrazyną, a następnie odwodornienia :
Podstawione pirazole wytwarza się przez kondensację 1,3- diketonów z hydrazyną (reakcje typu Knorra). Na przykład acetyloaceton i hydrazyna dają 3,5-dimetylopirazol:
- CH 3 C (O) CH 2 C (O) CH 3 + N 2 H 4 → (CH 3 ) 2 C 3 HN 2 H + 2 H 2 O
Historia
Termin pirazol został nadany tej klasie związków przez niemieckiego chemika Ludwiga Knorra w 1883 roku. W klasycznej metodzie opracowanej przez niemieckiego chemika Hansa von Pechmanna w 1898 roku pirazol został zsyntetyzowany z acetylenu i diazometanu .
Konwersja do skorpionów
Pirazole reagują z borowodorkiem potasu, tworząc klasę ligandów znanych jako skorpionian . Sam pirazol reaguje z borowodorkiem potasu w wysokich temperaturach (~200 ° C), tworząc ligand trójkleszczowy znany jako ligand Tp :
3,5-difenylo- 1H- pirazol
3,5-difenylo- 1H- pirazol powstaje w wyniku reakcji ( E )-1,3-difenyloprop-2-en-1-onu z wodzianem hydrazyny w obecności siarki elementarnej lub nadsiarczanu sodu lub przy użyciu hydrazonu w takim przypadku azyna jest wytwarzana jako produkt uboczny.
Występowanie i zastosowania

W 1959 roku z nasion arbuzów wyizolowano pierwszy naturalny pirazol, 1-pirazolilo-alaninę .
W medycynie szeroko stosowane są pochodne pirazolu
Pierścień pirazolowy znajduje się w różnych pestycydach, takich jak fungicydy, insektycydy i herbicydy, w tym fenpiroksymat , fipronil , tebufenpirad i tolfenpirad . Ugrupowania pirazolowe są wymienione przez amerykańską FDA wśród najczęściej używanych układów pierścieniowych dla leków małocząsteczkowych
Zobacz też
- 3,5-dimetylopirazol
- imidazol , analog pirazolu z dwoma non -adjacent atomów azotu.
- izoksazol , inny analog, atom azotu w pozycji 1 zastąpiony tlenem.
Bibliografia
Dalsza lektura
A. Schmidta; A. Dregera (2011). „Ostatnie postępy w chemii pirazoli. Część 2. Reakcje i N-heterocykliczne karbeny pirazolu”. Aktualn. Organizacja Chem . 15 (16): 2897–2970. doi : 10.2174/138527211796378497 .