Inhibitor peptydazy dipeptydylowej-4 - Dipeptidyl peptidase-4 inhibitor
Inhibitory dipeptydylopeptydazy 4 ( DPP-4 inhibitory lub gliptins ) są klasą hipoglikemicznych doustnych , które blokują ten enzym dipeptydylowej peptydazy-4 (DPP-4). Mogą być stosowane w leczeniu cukrzycy typu 2 .
Pierwszy środek z tej klasy – sitagliptyna – został zatwierdzony przez FDA w 2006 roku.
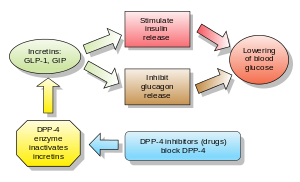
Glukagon zwiększa poziom glukozy we krwi , a inhibitory DPP-4 obniżają poziom glukagonu i glukozy we krwi. Mechanizm działania inhibitorów DPP-4 polega na zwiększeniu poziomu inkretyn ( GLP-1 i GIP ), które hamują uwalnianie glukagonu , co z kolei zwiększa wydzielanie insuliny , zmniejsza opróżnianie żołądka i obniża poziom glukozy we krwi .
Metaanaliza z 2018 r. nie wykazała korzystnego wpływu inhibitorów DPP-4 na śmiertelność z jakiejkolwiek przyczyny, śmiertelność z przyczyn sercowo-naczyniowych, zawał mięśnia sercowego lub udar mózgu u pacjentów z cukrzycą typu 2.
Przykłady
Leki należące do tej klasy to:
- Sitagliptyna (zatwierdzona przez FDA 2006, sprzedawana przez Merck & Co. jako Januvia)
- Vildagliptyna (zatwierdzona przez UE 2007, sprzedawana w UE przez Novartis jako Galvus)
- Saksagliptyna (zatwierdzona przez FDA w 2009 roku, sprzedawana jako Onglyza)
- Linagliptyna (zatwierdzona przez FDA w 2011 roku, sprzedawana jako Tradjenta przez Eli Lilly and Company i Boehringer Ingelheim )
- Gemigliptyna (zatwierdzona w Korei w 2012 roku, sprzedawana przez LG Life Sciences ) sprzedawana jako Zemiglo
- Anagliptyna (zatwierdzona w Japonii w 2012 roku, sprzedawana przez Sanwa Kagaku Kenkyusho Co., Ltd. i Kowa Company, Ltd. )
- Teneligliptyna (zatwierdzona w Japonii w 2012 r.)
- Alogliptyna (zatwierdzona przez FDA 2013, sprzedawana przez Takeda Pharmaceutical Company )
- Trelagliptyna (zatwierdzona do użytku w Japonii w 2015 r.)
- Omarigliptyna (MK-3102) (zatwierdzona w Japonii w 2015 r., opracowana przez Merck & Co .; badania wykazały, że omarigliptyna może być stosowana w leczeniu raz w tygodniu i ogólnie dobrze tolerowana w badaniach podstawowych i rozszerzonych)
- Evogliptin (zatwierdzony do użytku w Korei Południowej)
- Gosogliptyna (zatwierdzona do użytku w Rosji)
- Dutogliptyna (opracowywana przez Phenomix Corporation ), faza III
Inne chemikalia, które mogą hamować DPP-4 obejmują:
- Berberyna , alkaloid występujący w roślinach z rodzaju Berberis , hamuje peptydazę dipeptydylową-4, co może przynajmniej częściowo wyjaśniać jej działanie przeciwhiperglikemiczne.
Niekorzystne skutki
U osób już przyjmujących pochodne sulfonylomocznika istnieje zwiększone ryzyko niskiego poziomu cukru we krwi podczas przyjmowania leku z klasy leków DPP-4.
Działania niepożądane obejmują zapalenie nosogardzieli, ból głowy , nudności , niewydolność serca , nadwrażliwość i reakcje skórne.
Amerykańska Agencja ds. Żywności i Leków (FDA) ostrzega, że leki na cukrzycę typu 2, takie jak sitagliptyna , saksagliptyna , linagliptyna i alogliptyna, mogą powodować ból stawów, który może być ciężki i powodować niepełnosprawność. FDA dodała nowe ostrzeżenie i środki ostrożności dotyczące tego ryzyka na etykietach wszystkich leków z tej klasy leków, zwanych inhibitorami dipeptydylopeptydazy-4 (DPP-4). Jednak badania oceniające ryzyko wystąpienia reumatoidalnego zapalenia stawów wśród użytkowników inhibitorów DPP-4 były niejednoznaczne.
Przegląd z 2014 r. wykazał zwiększone ryzyko niewydolności serca w przypadku saksagliptyny i alogliptyny, co skłoniło FDA w 2016 r. do dodania ostrzeżeń do odpowiednich etykiet leków.
Metaanaliza z 2018 r. wykazała, że stosowanie inhibitorów DPP-4 wiązało się z 58% zwiększonym ryzykiem rozwoju ostrego zapalenia trzustki w porównaniu z placebo lub brakiem leczenia.
Badanie obserwacyjne z 2018 r. sugerowało zwiększone ryzyko rozwoju nieswoistego zapalenia jelit (w szczególności wrzodziejącego zapalenia jelita grubego), osiągającego szczyt po trzech do czterech latach stosowania i zmniejszającego się po ponad czterech latach stosowania.
Nowotwór
W odpowiedzi na doniesienie o zmianach przedrakowych w trzustce szczurów i dawców narządów leczonych inhibitorem DPP-4 sitagliptyną, amerykańska FDA i Europejska Agencja Leków przeprowadziły niezależne przeglądy wszystkich danych klinicznych i przedklinicznych związanych z możliwym powiązaniem Inhibitory DPP-4 z rakiem trzustki. We wspólnym liście do New England Journal of Medicine agencje stwierdziły, że nie doszły jeszcze do ostatecznego wniosku dotyczącego możliwego związku przyczynowego.
Metaanaliza z 2014 r. nie znalazła dowodów na zwiększone ryzyko raka trzustki u osób leczonych inhibitorami DPP-4, ale ze względu na niewielką ilość dostępnych danych nie była w stanie całkowicie wykluczyć możliwego ryzyka.
Leki złożone
Niektóre leki z grupy inhibitorów DPP-4 zostały zatwierdzone przez FDA do stosowania z metforminą jednocześnie z efektem addytywnym w celu zwiększenia poziomu glukagonopodobnego peptydu 1 (GLP-1), który również zmniejsza wytwarzanie glukozy w wątrobie .