Trójtlenek ksenonu - Xenon trioxide
|
|
|
|
| Nazwy | |
|---|---|
|
Nazwy IUPAC
Trójtlenek
ksenonu Tlenek ksenonu(VI) |
|
| Inne nazwy
Bezwodnik ksenowy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| XeO 3 | |
| Masa cząsteczkowa | 179,288 g/mol |
| Wygląd zewnętrzny | bezbarwne krystaliczne ciało stałe |
| Gęstość | 4,55 g / cm 3 , stałe |
| Temperatura topnienia | 25 ° C (77 ° F; 298 K) Gwałtowny rozkład |
| Rozpuszczalny (z reakcją) | |
| Struktura | |
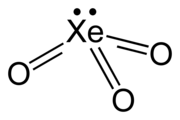
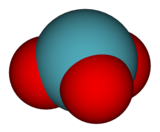
| trójkątny piramidalny (C 3v ) | |
| Termochemia | |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
402 kJ·mol -1 |
| Zagrożenia | |
| NFPA 704 (ognisty diament) | |
| Związki pokrewne | |
|
Związki pokrewne
|
Ksenon osmu Kwas ksenonowy |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Ksenon trójtlenek jest nietrwałym związkiem z ksenonem w +6 utlenienia . Jest bardzo silnym środkiem utleniającym i powoli uwalnia tlen z wody, przyspieszany przez ekspozycję na światło słoneczne. Jest niebezpiecznie wybuchowy w kontakcie z materiałami organicznymi. Kiedy wybucha, uwalnia gazowy ksenon i tlen.
Chemia
Trójtlenek ksenonu jest silnym środkiem utleniającym i może utleniać większość substancji, które w ogóle ulegają utlenieniu. Działa jednak wolno, co zmniejsza jego użyteczność.
Powyżej 25 °C trójtlenek ksenonu jest bardzo podatny na gwałtowną eksplozję:
Po rozpuszczeniu w wodzie powstaje kwaśny roztwór kwasu ksenowego :
- XeO 3 (roztwór wodny) + H 2 O → H 2 XeO 4 ⇌ H + + HXeO−
4
Ten roztwór jest stabilny w temperaturze pokojowej i nie posiada właściwości wybuchowych trójtlenku ksenonu. Ilościowo utlenia kwasy karboksylowe do dwutlenku węgla i wody .
Alternatywnie rozpuszcza się w roztworach alkalicznych tworząc kseniany . HXeO−
4anion jest dominującym gatunkiem w roztworach ksenianowych. Nie są one stabilne i zaczynają dysproporcjonować na nadkseniany (stan utlenienia +8) oraz ksenon i tlen. Stałe nadkseniany zawierające XeO4-
6zostały wyizolowane przez reakcję XeO
3z wodnym roztworem wodorotlenków. Trójtlenek ksenonu reaguje z nieorganicznymi fluorkami, takimi jak KF, RbF lub CsF, tworząc stabilne ciała stałe w postaci MXeO
3F .
Właściwości fizyczne
Hydroliza ksenonowej heksafluorku lub ksenonowej tetrafluorek otrzymuje się roztwór, z którego bezbarwny Xeo 3 kryształy można otrzymać przez odparowanie. Kryształy są stabilne przez kilka dni w suchym powietrzu, ale łatwo wchłaniają wodę z wilgotnego powietrza, tworząc stężony roztwór. Struktura krystaliczna jest rombowa z a = 6,163 A, b = 8,115 A, c = 5,234 A i 4 cząsteczkami na komórkę elementarną . Gęstość wynosi 4,55 g / cm 3 .
 |
 |

|
| ball-and-stick modelu części struktury krystalicznej Xeo 3 |
model wypełniający przestrzeń | geometria koordynacyjna Xe |
Bezpieczeństwo
Z XeO 3 należy obchodzić się bardzo ostrożnie. Próbki zdetonowały się, gdy nie zostały zakłócone w temperaturze pokojowej. Suche kryształy reagują wybuchowo z celulozą.

