Oksytetrafluorek ksenonu - Xenon oxytetrafluoride
|
|

|
|
| Identyfikatory | |
|---|---|
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
|
|
|
|
| Nieruchomości | |
| XeOF 4 | |
| Masa cząsteczkowa | 223,23 g/mol |
| Wygląd | bezbarwna ciecz |
| Gęstość | 3,17 g / cm 3 , ciekłe |
| Temperatura topnienia | -46,2 ° C (-51,2 ° F; 227,0 K) |
| Reaguje z wodą | |
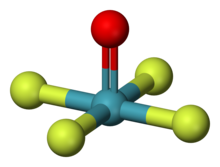
| Struktura | |
| kwadratowy piramidalny | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Oksytetrafluorek ksenonu ( Xe O F 4 ) jest nieorganicznym związkiem chemicznym . Jest to bezbarwna, stabilna ciecz o temperaturze topnienia -46,2°C, którą można zsyntetyzować przez częściową hydrolizę XeF
6, czyli reakcja XeF
6z krzemionką lub NaNO
3:
-
NaNO
3+ XeF
6→ NaF + XeOF
4+ FNO
2
Synteza wysokowydajna przebiega w reakcji XeF
6z POF
3 w -196 °C.
Podobnie jak większość tlenków ksenonu, jest on niezwykle reaktywny i niestabilny, hydrolizuje w wodzie dając niebezpiecznie niebezpieczne i korozyjne produkty, w tym fluorowodór :
- 2 XeOF 4 + 4 H 2 O → 2 Xe + 8 HF + 3 O 2
Ponadto powstaje również pewna ilość ozonu i fluoru. Reakcja ta jest niezwykle niebezpieczna, dlatego oksytetrafluorek ksenonu powinien być trzymany z dala od wszelkich śladów wody lub pary wodnej w każdych warunkach.
Reakcje
XeOF 4 reaguje z H 2 O w następujących etapach:
- XeOF 4 + H 2 O → XeO 2 F 2 + 2 HF
- XeO 2 F 2 + H 2 O → XeO 3 + 2 HF
Utworzony XeO 3 jest niebezpiecznym materiałem wybuchowym rozkładającym się wybuchowo na Xe i O 2 :
- 2 XeO 3 → 2 Xe + 3 O 2
W postaci płynnej XeOF
4wykazuje zachowanie amfoteryczne, tworząc kompleksy zarówno z silnymi zasadami Lewisa, takimi jak CsF, jak i silnymi kwasami Lewisa, takimi jak SbF
5. Tworzy addukt 1:1 z XeF
2, izostrukturalny z XeF
2· JEŚLI
5, a także różne fluorki metali ciężkich.
Reakcja XeOF
4z XeO
3zapewnia wygodną drogę syntezy dla XeO
2fa
2.
Linki zewnętrzne
Bibliografia
