Powierzchnia Van der Waalsa - Van der Waals surface
| Element | promień ( Å ) |
|---|---|
| Wodór | 1,2 (1,09) |
| Węgiel | 1,7 |
| Azot | 1,55 |
| Tlen | 1,52 |
| Fluor | 1,47 |
| Fosfor | 1,8 |
| Siarka | 1,8 |
| Chlor | 1,75 |
| Miedź | 1,4 |
|
Promienie Van der Waalsa zaczerpnięte z kompilacji Bondiego (1964). Wartości z innych źródeł mogą się znacznie różnić ( patrz tekst ) |
|
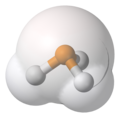
Van der Waalsa powierzchni z cząsteczką abstrakcyjne przedstawienie lub model cząsteczce ilustrujący gdzie bardzo nierównych zarysach powierzchni może znajdować się do cząsteczki, bazując na twardych odcięcia od Van der Waalsa na poszczególnych atomów i oznacza powierzchnia, przez którą cząsteczka może być postrzegana jako oddziałująca z innymi cząsteczkami. Nazywana również obwiednią Van der Waalsa, powierzchnia Van der Waalsa została nazwana na cześć Johannesa Diderika van der Waalsa , holenderskiego fizyka teoretycznego i termodynamika, który opracował teorię zapewniającą równanie stanu ciecz-gaz, które wyjaśniało niezerową objętość atomów i molekuł, a także na ich oddziaływaniu siły przyciągania (konstrukcje teoretyczne, które również noszą jego imię). Powierzchnie Van der Waalsa są zatem narzędziem wykorzystywanym w abstrakcyjnych reprezentacjach cząsteczek, niezależnie od tego, czy były dostępne, tak jak były pierwotnie, za pomocą obliczeń ręcznych, fizycznych modeli drewna/plastiku, a teraz również cyfrowo, za pomocą oprogramowania do chemii obliczeniowej . Praktycznie rzecz biorąc, modele CPK , opracowane i nazwane przez Roberta Coreya , Linusa Paulinga i Waltera Koltuna , były pierwszymi szeroko stosowanymi fizycznymi modelami molekularnymi opartymi na promieniach Van der Waalsa i umożliwiły szerokie zastosowanie pedagogiczne i badawcze modelu przedstawiającego Van der Waalsa. Powierzchnie Waalsa cząsteczek.
Objętość Van der Waalsa i powierzchnia Van der Waalsa

Podobne do tytułowego pojęcia są pomysły o Van der Waalsa , V wagowo , a Van der Waalsa powierzchni, skrócone różnorodnie jako A w , vdWSA, VSA i WSA. Pole powierzchni Van der Waalsa jest abstrakcyjną koncepcją pola powierzchni atomów lub molekuł z matematycznego oszacowania, albo obliczając ją na podstawie pierwszych zasad, albo całkując przez odpowiednią objętość Van der Waalsa. W najprostszym przypadku, dla kulistego gazu jednoatomowego, jest to po prostu obliczona powierzchnia kuli o promieniu równym promieniowi Van der Waalsa atomu gazowego:
.
Van der objętości Waalsa , rodzaj atomowej lub cząsteczkowego objętość, jest właściwością bezpośrednio związaną z Van der Waalsa promieniu i jest zdefiniowana jako objętość zajmowana przez pojedynczy atom, lub w połączonej sensie, wszystkie atomy w cząsteczce . Można ją obliczyć dla atomów, jeśli znany jest promień Van der Waalsa, a dla cząsteczek, jeśli znane są promienie ich atomów oraz odległości międzyatomowe i kąty. Jak powyżej, w najprostszym przypadku, na kulistej monoatomowego gazu V w po prostu obliczona objętości kuli o promieniu równym Van der Waalsa promienia atomu gazowej:
.
Dla cząsteczki Vw jest objętością zamkniętą przez powierzchnię Van der Waalsa ; W związku z tym, obliczenie V w zdolności zakłada opisać i obliczyć Van der Waalsa powierzchni. Objętości Van der Waalsa cząsteczek są zawsze mniejsze niż suma objętości Van der Waalsa ich atomów składowych, ponieważ odległości międzyatomowe wynikające z wiązania chemicznego są mniejsze niż suma promieni Van der Waalsa atomowego. W tym sensie powierzchnia Van der Waalsa homojądrowej cząsteczki dwuatomowej może być postrzegana jako obrazowe nakładanie się dwóch sferycznych powierzchni Van der Waalsa poszczególnych atomów, podobnie jak w przypadku większych cząsteczek, takich jak metan, amoniak itp. (patrz zdjęcia).
Promienie i objętości Van der Waalsa można wyznaczyć z właściwości mechanicznych gazów (metoda oryginalna wyznaczania stałej Van der Waalsa ), z punktu krytycznego (np. cieczy), z pomiarów krystalograficznych odstępów między parami niespojonych atomy w kryształach lub z pomiarów właściwości elektrycznych lub optycznych (tj. polaryzowalności lub refrakcji molowej ). We wszystkich przypadkach pomiary wykonywane są na próbkach makroskopowych, a wyniki wyrażane są jako wielkości molowe . Objętości Van der Waalsa pojedynczego atomu lub cząsteczek uzyskuje się dzieląc makroskopowo określone objętości przez stałą Avogadro . Różne metody dają wartości promienia, które są podobne, ale nie identyczne – na ogół w zakresie 1–2 Å (100–200 pm ). Przydatne tabelaryczne wartości promieni Van der Waalsa uzyskuje się, biorąc średnią ważoną wielu różnych wartości doświadczalnych, iz tego powodu różne tabele będą przedstawiać różne wartości promienia Van der Waalsa tego samego atomu. Argumentowano również, że promień Van der Waalsa nie jest stałą właściwością atomu we wszystkich okolicznościach, a raczej, że będzie się zmieniał w zależności od chemicznego środowiska atomu.
Galeria
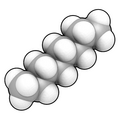
Zapełniający przestrzeń model n- oktanu , prostołańcuchowego (normalnego) węglowodoru złożonego z 8 atomów węgla i 18 wodorów, wzory: CH 3 CH 2 (CH 2 ) 4 CH 2 CH 3 lub C
8h
18. Należy zauważyć, że przedstawiony przedstawiciel ma pojedynczą konformacyjną „pozę” populacji cząsteczek, która z powodu niskich barier energetycznych Gibbsa dla rotacji wokół wiązań węgiel-węgiel (nadając „łańcuchowi” węgla dużą elastyczność). zwykle składa się z bardzo dużej liczby różnych takich konformacji (np. w roztworze).Przykład trójwymiarowego, wypełniającego przestrzeń, opartego na Van der Waala modelu złożonej molekuły, THC , substancji czynnej w medycznej marihuanie. Może być konieczne kliknięcie obrazu, aby zobaczyć obrót.
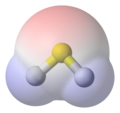
Siarkowodór, H 2 S, wypełniający przestrzeń, przedstawienie Van der Waala, nałożony model kulowo-kijowy, siarka (S) na żółto, wodór (H) na biało z niebieskim cieniowaniem. Pokazuje również na jej powierzchni powierzchnię potencjału elektrostatycznego (obliczoną dla cząsteczki w nieznany sposób), przy użyciu narzędzi chemii obliczeniowej . Jest zacieniowany od niebieskiego dla obszarów elektrododatnich do czerwonego dla obszarów elektroujemnych .
Zobacz też
Referencje i uwagi
Dalsza lektura
- DC Whitley, wykresy powierzchniowe Van der Waalsa i kształt molekularny , Journal of Mathematical Chemistry , tom 23, numery 3-4, 1998, s. 377-397(21).
- M. Petitjean, O analitycznym obliczaniu powierzchni i objętości Van der Waalsa: niektóre aspekty liczbowe , Journal of Computational Chemistry , tom 15, numer 5, 1994, s. 507-523.
Zewnętrzne linki
- VSA dla różnych cząsteczek , Anton Antonov, The Wolfram Demonstrations Project , 2007.
- Promienie Van der Waalsa , Słownik biologii strukturalnej, Biblioteka obrazów biologicznych makrocząsteczek.
- Obliczenia analityczne powierzchni i objętości Van der Waalsa.