Węglowodory - Hydrocarbon
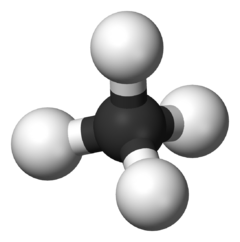
W chemii organicznej , A węglowodór jest związek organiczny składający się w całości z wodoru i dwutlenku węgla . Węglowodory są przykładami wodorków grupy 14 . Węglowodory są na ogół bezbarwne i hydrofobowe o słabym zapachu. Ze względu na ich zróżnicowane struktury molekularne trudno jest dalej uogólniać. Większość antropogenicznych emisji węglowodorów pochodzi ze spalania paliw kopalnych, w tym z produkcji i spalania paliw. Naturalne źródła węglowodorów, takie jak etylen, izopren i monoterpeny, pochodzą z emisji roślinności.
Rodzaje
Zgodnie z nomenklaturą chemii organicznej IUPAC klasyfikacje węglowodorów są następujące:
- Węglowodory nasycone to najprostszy z gatunków węglowodorów. Składają się w całości z pojedynczych wiązań i są nasycone wodorem. Wzór na acykliczne węglowodory nasycone (tj. alkany ) to C n H 2 n +2 . Najbardziej ogólną formą węglowodorów nasyconych jest C n H 2 n +2(1- r ) , gdzie r jest liczbą pierścieni. Te z dokładnie jednym pierścieniem to cykloalkany . Węglowodory nasycone są podstawą paliw ropopochodnych i występują jako związki liniowe lub rozgałęzione. Reakcja substytucji jest ich właściwością charakterystyczną (podobnie jak reakcja chlorowania do chloroformu ). Węglowodory o tym samym wzorze cząsteczkowym, ale różnych wzorach strukturalnych nazywane są izomerami strukturalnymi . Jak podano w przykładzie 3-metyloheksanu i jego wyższych homologów , węglowodory rozgałęzione mogą być chiralne . Chiralne węglowodory nasycone stanowią łańcuchy boczne biocząsteczek, takich jak chlorofil i tokoferol .
- Węglowodory nienasycone mają jedno lub więcej podwójnych lub potrójnych wiązań między atomami węgla. Te z podwójnym wiązaniem nazywane są alkenami . Te z jednym podwójnym wiązaniem mają wzór C n H 2 n (zakładając struktury niecykliczne). Te zawierające potrójne wiązania nazywane są alkinami . Te z jednym potrójnym wiązaniem mają wzór C n H 2 n -2 .
- Węglowodory aromatyczne , znane również jako areny , to węglowodory posiadające co najmniej jeden pierścień aromatyczny . 10% całkowitej emisji niemetanowego węgla organicznego to węglowodory aromatyczne ze spalin pojazdów napędzanych benzyną.
Węglowodorami mogą być gazy (np. metan i propan ), ciecze (np. heksan i benzen ), woski lub niskotopliwe ciała stałe (np. parafina i naftalen ) lub polimery (np. polietylen , polipropylen i polistyren ).
Termin „alifatyczny” odnosi się do węglowodorów niearomatycznych. Nasycone węglowodory alifatyczne są czasami nazywane „parafinami”. Węglowodory alifatyczne zawierające podwójne wiązanie między atomami węgla są czasami nazywane „olefinami”.
Węglowodory proste i ich odmiany
| Liczba atomów węgla |
Alkan (pojedyncze wiązanie) | Alken (podwójne wiązanie) | Alkin (potrójne wiązanie) | Cykloalkan | Alkadien |
|---|---|---|---|---|---|
| 1 | Metan | — | — | — | — |
| 2 | Etan | Eten (etylen) | Etyn (acetylen) | — | — |
| 3 | Propan | Propen (propylen) | Propyn (metyloacetylen) | Cyklopropan | Propadien (alen) |
| 4 | Butan | Buten (butylen) | Butyne | Cyklobutan | Butadien |
| 5 | Pentan | Penten | Pentyn | Cyklopentan | Pentadien (piperylen) |
| 6 | Heksan | Heksen | Heksyna | Cykloheksan | Heksadien |
| 7 | Heptan | Hepten | Heptyna | Cykloheptan | Heptadien |
| 8 | Oktan | Okten | Oktyn | Cyklooktan | Oktadien |
| 9 | Nonane | Brak | Nienine | Cyklononan | Nonadien |
| 10 | Dekan | Decena | Decyne | Cyklodekan | Dekadien |
| 11 | Undekane | Nieprzyzwoitość | Undecyna | Cykloundekan | Undekadien |
| 12 | Dodekan | Dodecen | Dodecyna | Cyklododekan | Dodekadien |
Stosowanie

Dominującym zastosowaniem węglowodorów jest paliwo palne . Metan jest dominującym składnikiem gazu ziemnego. C 6 do C 10 alkany, alkeny i cykloalkany, takie jak izomeryczne górne składniki benzyny , nafty , paliwa do silników odrzutowych i specjalistycznych techniczne mieszaniny rozpuszczalników. Dzięki stopniowemu dodawaniu jednostek węglowych proste węglowodory o strukturze niepierścieniowej mają wyższe lepkości , wskaźniki smarności, temperatury wrzenia, temperatury krzepnięcia i głębszy kolor. Na przeciwległym krańcu od metanu znajdują się ciężkie smoły, które pozostają jako najniższa frakcja w retorcie do rafinacji ropy naftowej . Są one gromadzone i szeroko stosowane jako mieszanki dachowe, skład nawierzchni ( bitum ), środki do konserwacji drewna ( seria kreozotowa ) oraz jako ciecze odporne na ścinanie o bardzo dużej lepkości.
Niektóre niepaliwowe zastosowania węglowodorów na dużą skalę zaczynają się od etanu i propanu, które są otrzymywane z ropy naftowej i gazu ziemnego. Te dwa gazy są przekształcane albo w gaz syntezowy, albo w etylen i propylen . Te dwa alkeny są prekursorami polimerów, w tym polietylenu , polistyrenu, akrylanów, polipropylenu itp. Inną klasą specjalnych węglowodorów jest BTX , mieszanina benzenu , toluenu i trzech izomerów ksylenu . Światowe zużycie benzenu szacowane na ponad 40 000 000 ton (2009).
Węglowodory są również powszechne w przyrodzie. Niektóre stawonogi eusocjalne, takie jak brazylijska pszczoła bezżądłowa, Schwarziana quadripunctata , używają unikalnych „zapachów” węglowodorowych w celu odróżnienia krewnych od niespokrewnionych. Skład chemiczny węglowodorów różni się w zależności od wieku, płci, lokalizacji gniazda i pozycji hierarchicznej.
Istnieje również możliwość pozyskiwania węglowodorów z roślin takich jak Euphorbia lathyri i Euphorbia tirucalli jako alternatywne i odnawialne źródło energii dla pojazdów napędzanych olejem napędowym. Ponadto bakterie endofityczne z roślin, które naturalnie wytwarzają węglowodory, zostały wykorzystane w degradacji węglowodorów w próbach zmniejszenia stężenia węglowodorów w zanieczyszczonych glebach.
Reakcje
Cechą godną uwagi węglowodorów jest ich obojętność, zwłaszcza dla nasyconych składników. W przeciwnym razie można zidentyfikować trzy główne typy reakcji:
Reakcje wolnorodnikowe
Reakcje substytucji zachodzą tylko w węglowodorach nasyconych (pojedyncze wiązania węgiel-węgiel). Takie reakcje wymagają wysoce reaktywnych odczynników, takich jak chlor i fluor . W przypadku chlorowania jeden z atomów chloru zastępuje atom wodoru. Reakcje przebiegają szlakami wolnorodnikowymi .
- CH 4 + CI 2 → CH 3 Cl + HCl
- CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl
aż do CCl 4 ( tetrachlorek węgla )
- C 2 H 6 + Cl 2 → C 2 H 5 Cl + HCl
- C 2 H 4 Cl 2 + Cl 2 → C 2 H 3 Cl 3 + HCl
aż do C 2 Cl 6 ( heksachloroetan )
Podstawienie
Spośród klas węglowodorów, związki aromatyczne wyjątkowo (lub prawie) ulegają reakcjom substytucji. Przykładem jest proces chemiczny praktykowany na największą skalę: reakcja benzenu i etylenu w etylobenzen .
Reakcje dodawania
Reakcje addycji dotyczą alkenów i alkinów. W tej reakcji różne odczynniki dodają „w poprzek” wiązania pi. Przykładowymi odczynnikami są chlor, chlorowodór, woda i wodór . Alkeny i niektóre alkiny również ulegają polimeryzacji , metatezie alkenów i metatezie alkinów .
Utlenianie
Węglowodory są obecnie głównym źródłem światowych źródeł energii elektrycznej i ciepła (takich jak ogrzewanie domów) ze względu na energię wytwarzaną podczas ich spalania. Często ta energia jest wykorzystywana bezpośrednio jako ciepło, na przykład w domowych grzejnikach, które wykorzystują ropę naftową lub gaz ziemny . Węglowodór jest spalany, a ciepło wykorzystywane do podgrzewania wody, która jest następnie cyrkulowana. Podobną zasadę stosuje się do wytwarzania energii elektrycznej w elektrowniach .
Wspólne właściwości węglowodorów to fakt, że podczas spalania wytwarzają one parę wodną, dwutlenek węgla i ciepło oraz że do spalania potrzebny jest tlen . Najprostszy węglowodór, metan , spala się w następujący sposób:
- CH 4 + 2 O 2 → 2 H 2 O + CO 2 + energia
Przy niedostatecznym dopływie powietrza powstaje tlenek węgla i para wodna :
- 2 CH 4 + 3 O 2 → 2 CO + 4 H 2 O
Innym przykładem jest spalanie propanu :
- C 3 H 8 + 5 O 2 → 4 H 2 O + 3 CO 2 + energia
I wreszcie, dla dowolnego liniowego alkanu o n atomach węgla,
- C n H 2 n +2 + 3 n + 1/2 O 2 → ( n + 1) H 2 O + n CO 2 + energia.
Częściowe utlenianie charakteryzuje reakcje alkenów i tlenu. Proces ten jest podstawą jełczenia i wysychania farby .
Początek
Ogromna większość węglowodorów występujących na Ziemi występuje w ropie naftowej , ropie naftowej , węglu i gazie ziemnym. Ropa naftowa (dosłownie „olej skalny” – w skrócie benzyna) i węgiel są powszechnie uważane za produkty rozkładu materii organicznej. Węgiel, w przeciwieństwie do ropy naftowej, jest bogatszy w węgiel i uboższy w wodór. Gaz ziemny jest produktem metanogenezy .
Pozornie nieograniczona różnorodność związków zawiera ropa naftowa, stąd konieczność rafinerii. Węglowodory te składają się z węglowodorów nasyconych, węglowodorów aromatycznych lub ich kombinacji. W ropie naftowej brakuje alkenów i alkinów. Ich produkcja wymaga rafinerii. Węglowodory ropopochodne są wykorzystywane głównie jako paliwo, ale są również źródłem praktycznie wszystkich syntetycznych związków organicznych, w tym tworzyw sztucznych i farmaceutyków. Gaz ziemny jest zużywany prawie wyłącznie jako paliwo. Węgiel jest wykorzystywany jako paliwo oraz jako środek redukujący w metalurgii .
Węglowodory abiologiczne
Uważa się, że niewielka część węglowodorów występujących na ziemi jest abiologiczna .
Niektóre węglowodory są również szeroko rozpowszechnione i obfite w Układzie Słonecznym . Na Tytanie , największym księżycu Saturna , odkryto jeziora ciekłego metanu i etanu , co potwierdziła misja Cassini-Huygens . Węglowodory są również obfite w mgławice tworzące wielopierścieniowe związki węglowodorów aromatycznych (WWA).
Bioremediacja
Bioremediacja węglowodorów ze skażonej gleby lub wody jest ogromnym wyzwaniem ze względu na chemiczną obojętność charakteryzującą węglowodory (stąd przetrwały miliony lat w skale macierzystej). Niemniej jednak opracowano wiele strategii, w tym bioremediację. Podstawowym problemem bioremediacji jest niedobór enzymów, które na nie działają. Mimo to obszar ten cieszy się regularną uwagą. Bakterie w warstwie gabroicznej skorupy oceanicznej mogą rozkładać węglowodory; ale ekstremalne środowisko utrudnia badania. Inne bakterie, takie jak Lutibacterium anuloederans, również mogą rozkładać węglowodory. Możliwa jest mikormediacja lub rozkład węglowodorów przez grzybnię i grzyby .
Bezpieczeństwo
Węglowodory mają na ogół niską toksyczność, stąd powszechne stosowanie benzyny i powiązanych produktów lotnych. Związki aromatyczne, takie jak benzen, są toksynami narkotycznymi, chronicznymi i rakotwórczymi . Niektóre rzadkie wielopierścieniowe związki aromatyczne są rakotwórcze. Węglowodory są wysoce łatwopalne .
Wpływ środowiska
Spalanie węglowodorów jako paliwa, które wytwarza dwutlenek węgla i wodę , jest głównym czynnikiem przyczyniającym się do antropogenicznego globalnego ocieplenia . Węglowodory są wprowadzane do środowiska poprzez ich szerokie wykorzystanie jako paliw i chemikaliów, a także poprzez wycieki lub przypadkowe wycieki podczas poszukiwań, produkcji, rafinacji lub transportu paliw kopalnych. Antropogeniczne skażenie gleby węglowodorami jest poważnym problemem globalnym ze względu na utrzymywanie się zanieczyszczeń i negatywny wpływ na zdrowie ludzi.
Zanieczyszczenie gleby węglowodorami może mieć istotny wpływ na jej właściwości mikrobiologiczne, chemiczne i fizyczne. Może to służyć zapobieganiu, spowolnieniu lub nawet przyspieszeniu wzrostu roślinności w zależności od dokładnie zachodzących zmian. Ropa naftowa i gaz ziemny to dwa największe źródła skażenia gleby węglowodorami.
Zobacz też
Bibliografia
Zewnętrzne linki


