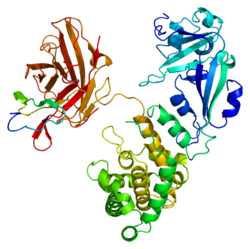
Wiążący heparynę czynnik wzrostu podobny do EGF - Heparin-binding EGF-like growth factor
Wiążący heparynę czynnik wzrostu EGF ( HB- EGF ) należy do rodziny białek EGF , które u ludzi są kodowane przez gen HBEGF .
HB-EGF-podobny czynnik wzrostu jest syntetyzowany jako zakotwiczona w błonie mitogenna i chemotaktyczna glikoproteina . Naskórkowy czynnik wzrostu wytwarzany przez monocyty i makrofagi ze względu na powinowactwo do heparyny określany jest jako HB-EGF. Wykazano, że odgrywa rolę w gojeniu się ran , przerostu serca oraz rozwoju i funkcjonowaniu serca . Po raz pierwszy zidentyfikowany w kondycjonowanych pożywkach ludzkich komórek podobnych do makrofagów, HB-EGF jest 87-aminokwasową glikoproteiną, która wykazuje wysoce regulowaną ekspresję genów. Zrzucanie ektodomen powoduje powstanie rozpuszczalnej dojrzałej formy HB-EGF, która wpływa na czynniki mitogenne i chemotaktyczne komórek mięśni gładkich i fibroblastów. Transbłonowa forma HB-EGF jest unikalnym receptorem dla toksyny błoniczej i działa w sygnalizacji jukstakrynowej w komórkach. Obie formy HB-EGF uczestniczą w normalnych procesach fizjologicznych oraz w procesach patologicznych obejmujących progresję i przerzuty nowotworu, przerost narządów i chorobę miażdżycową. HB-EGF może wiązać dwa miejsca na powierzchni komórek: proteoglikany siarczanu heparanu i oddziaływania międzykomórkowe na receptor EGF.
Interakcje
Wykazano, że czynnik wzrostu wiążący heparynę podobny do EGF oddziałuje z białkiem 16 zawierającym NRD1 , palec cynkowy i domenę BTB oraz BAG1 .
Aktywność biologiczna HB-EGF z tymi genami wpływa na progresję cyklu komórkowego, molekularną regulację białek opiekuńczych, przeżycie komórek, funkcje komórkowe, adhezję i pośredniczenie w migracji komórek. Gen NRD1 koduje białko nardilizynę, modulator HB-EGF. Białko 16 zawierające palec cynkowy i domenę BTB oraz molekularny regulator opiekuńczy z rodziny BAG działają jako białka współopiekuńcze w procesach z udziałem HB-EGF.
Rola w raku
Ostatnie badania wskazują na znaczne podwyższenie ekspresji genu HB-EGF w wielu ludzkich nowotworach, jak również w liniach komórkowych pochodzących z nowotworu. Dowody wskazują, że HB-EGF odgrywa znaczącą rolę w rozwoju złośliwych fenotypów przyczyniających się do przerzutowych i inwazyjnych zachowań guzów. Proliferacyjne i chemotaktyczne działanie HB-EGF wynika z docelowego oddziaływania na poszczególne komórki, w tym fibroblasty, komórki mięśni gładkich i keratynocyty. W przypadku wielu typów komórek, takich jak komórki nowotworu sutka i jajnika, ludzkie komórki nabłonkowe i keratynocyty, HB-EGF jest silnym mitogenem powodującym wyraźną regulację w górę HB-EGF w takich próbkach. Zarówno badania in vivo, jak i in vitro tworzenia nowotworu w liniach komórkowych pochodzących z raka wskazują, że ekspresja HB-EGF jest niezbędna do rozwoju nowotworu. W rezultacie badania, w których wdrożono zastosowanie specyficznych inhibitorów HB-EGF i przeciwciał monoklonalnych przeciwko HB-EGF, wykazują potencjał do opracowania nowych terapii do leczenia nowotworów poprzez ukierunkowanie na ekspresję HB-EGF.
Rola w rozwoju serca i unaczynienia
Wiązanie HB-EGF i aktywacja receptorów EGF odgrywa kluczową rolę podczas rozwoju tkanki zastawki serca i utrzymywania prawidłowej czynności serca u dorosłych. Podczas rozwoju tkanki zastawki interakcja HB-EGF z receptorami EGF i proteoglikanami siarczanu heparanu ma zasadnicze znaczenie dla zapobiegania wadom rozwojowym zastawek spowodowanym powiększeniem. W układzie naczyniowym obszary zaburzonego przepływu wykazują regulację w górę HB-EGF z promocją zmian naczyniowych, miażdżycy i przerostu tkanki wewnętrznej naczyń. Remodeling zaburzeń przepływu w tkankach naczyniowych spowodowany ekspresją HB-EGF przyczynia się do choroby zastawki aortalnej, choroby naczyń obwodowych i zwężenia konduitu.
Rola w gojeniu się ran
HB-EGF jest głównym czynnikiem wzrostu w nabłonku niezbędnym do gojenia ran skóry. Działanie mitogenne i migracyjne HB-EGF na keratynocyty i fibroblasty sprzyja naprawie skóry i angiogenezie niezbędnej do gojenia się ran i jest głównym składnikiem płynów z ran. HB-EGF wykazuje specyficzność komórek docelowych we wczesnych stadiach gojenia się ran, uwalnianych przez makrofagi, monocyty i keratynoktysy. Wiązanie powierzchni komórek HB-EGF z proteoglikanami siarczanu heparanu zwiększa zdolności promowania mitogenów, zwiększając szybkość gojenia się ran skóry, skracając czas gojenia przeszczepu ludzkiej skóry i przyspieszając gojenie owrzodzeń, oparzeń i rozszczepionych ran naskórka.
Rola w innych procesach fizjologicznych
HB-EGF jest uznawany za ważny składnik modulacji aktywności komórek w różnych interakcjach biologicznych. Szeroko rozpowszechniony w neuronach mózgowych i neurogleju, HB-EGF indukowany przez niedotlenienie i/lub niedokrwienie mózgu stymuluje następnie neurogenezę. Interakcje między macicznym HB-EGF a receptorami naskórkowego czynnika wzrostu blastocyst wpływają na interakcje między zarodkiem a macicą i implantację. Badania pokazują, że HB-EGF chroni komórki macierzyste jelit i komórki nabłonka jelit w martwiczym zapaleniu jelit , chorobie dotykającej wcześniaki. W związku z załamaniem funkcji bariery jelitowej w martwiczym zapaleniu jelit może pośredniczyć wpływ HB-EGF na błonę śluzową jelit. HB-EGF wyrażany podczas skurczu mięśni szkieletowych ułatwia obwodowe usuwanie glukozy, tolerancję i wychwyt glukozy. Regulacja w górę HB-EGF podczas ćwiczeń może wyjaśniać molekularne podstawy zmniejszenia zaburzeń metabolicznych, takich jak otyłość i cukrzyca typu 2, przy regularnych ćwiczeniach.
Bibliografia
Dalsza lektura
- Higashiyama S, Lau K, Besner GE, et al. (1992). „Struktura wiążącego heparynę czynnika wzrostu podobnego do EGF. Wiele form, struktura pierwotna i glikozylacja dojrzałego białka” . J. Biol. Chem . 267 (9): 6205–12. doi : 10.1016/S0021-9258(18)42682-8 . PMID 1556128 .
- Yoshizumi M, Kourembanas S, Temizer DH, et al. (1992). „Czynnik martwicy nowotworu zwiększa transkrypcję genu czynnika wzrostu podobnego do naskórkowego czynnika wzrostu wiążącego heparynę w komórkach śródbłonka naczyniowego” . J. Biol. Chem . 267 (14): 9467-9. doi : 10.1016/S0021-9258(19)50112-0 . PMID 1577791 .
- Higashiyama S, Abraham JA, Miller J, et al. (1991). „Wiążący heparynę czynnik wzrostu wydzielany przez komórki podobne do makrofagów, który jest związany z EGF”. Nauka . 251 (4996): 936-9. Kod Bibcode : 1991Sci...251..936H . doi : 10.1126/science.1840698 . PMID 1840698 . S2CID 23639487 .
- Iwamoto R, Senoh H, Okada Y, et al. (1991). „Przeciwciało, które hamuje wiązanie toksyny błoniczej z komórkami, ujawniło powiązanie białka błonowego o masie 27 kDa z receptorem toksyny błoniczej” . J. Biol. Chem . 266 (30): 20463-9. doi : 10.1016/S0021-9258(18)54947-4 . PMID 1939101 .
- Hayes H, Kaneda Y, Uchida T, Okada Y (1988). „Regionalne przypisanie genu wrażliwości na toksynę błonicy przy użyciu fragmentów subchromosomalnych w hybrydach mikrokomórkowych”. Chromosoma . 96 (1): 26–32. doi : 10.1007/BF00285879 . PMID 3436221 . S2CID 35349033 .
- Bennett KL, Jackson DG, Simon JC i in. (1995). „Za prezentację czynnika wzrostu wiążącego heparynę odpowiadają izoformy CD44 zawierające ekson V3” . J. Cell Biol . 128 (4): 687–98. doi : 10.1083/jcb.128.4.687 . PKW 2199889 . PMID 7532176 .
- Pathak BG, Gilbert DJ, Harrison CA, et al. (1995). „Lokalizacja mysiego chromosomu trzech ligandów receptora EGF: amfiregulina (Areg), betacellulina (Btc) i EGF wiążący heparynę (Hegfl)” . Genomika . 28 (1): 116-8. doi : 10.1006/geno.1995.1116 . PMID 7590736 .
- Mitamura T, Higashiyama S, Taniguchi N, et al. (1995). „Toksyna błonicza wiąże się z domeną podobną do naskórkowego czynnika wzrostu (EGF) ludzkiego wiążącego heparynę receptora czynnika wzrostu podobnego do EGF/toksyny błoniczej i hamuje specyficznie jego aktywność mitogenną” . J. Biol. Chem . 270 (3): 1015-9. doi : 10.1074/jbc.270.3.11015 . PMID 7836353 .
- Hashimoto K, Higashiyama S, Asada H, et al. (1994). „Wiążący heparynę naskórkowy czynnik wzrostu podobny do czynnika wzrostu jest autokrynnym czynnikiem wzrostu dla ludzkich keratynocytów” . J. Biol. Chem . 269 (31): 20060-6. doi : 10.1016/S0021-9258(17)32127-0 . PMID 8051092 .
- Kobrin MS, Funatomi H, Friess H, et al. (1994). „Indukcja i ekspresja wiążącego heparynę czynnika wzrostu podobnego do EGF w ludzkim raku trzustki”. Biochem. Biofizyka. Res. Komuna . 202 (3): 1705-9. doi : 10.1006/bbrc.1994.2131 . PMID 8060360 .
- Maruyama K, Sugano S (1994). „Oligo-capping: prosta metoda zastąpienia struktury czapeczki eukariotycznych mRNA z oligorybonukleotydami”. Gen . 138 (1–2): 171–4. doi : 10.1016/0378-1119(94)90802-8 . PMID 8125298 .
- Thompson SA, Higashiyama S, Wood K, et al. (1994). „Charakterystyka sekwencji w wiążącym heparynie czynniku wzrostu podobnym do EGF, które pośredniczą w interakcji z heparyną” . J. Biol. Chem . 269 (4): 2541-9. doi : 10.1016/S0021-9258(17)41979-X . PMID 8300582 .
- Fen Z, Dhadly MS, Yoshizumi M i in. (1993). „Organizacja strukturalna i przypisanie chromosomów genu kodującego ludzki czynnik wzrostu naskórka-podobny czynnik wzrostu wiążący heparynę / receptor toksyny błonicy”. Biochemia . 32 (31): 7932-8. doi : 10.1021/bi00082a014 . PMID 8347598 .
- Elenius K, Paul S, Allison G, et al. (1997). „Aktywacja HER4 przez wiążący heparynę czynnik wzrostu podobny do EGF stymuluje chemotaksję, ale nie proliferację” . EMBO J . 16 (6): 1268–78. doi : 10.1093/emboj/16.6.1268 . PMC 1169725 . PMID 9135143 .
- Suzuki Y, Yoshitomo-Nakagawa K, Maruyama K, et al. (1997). „Budowa i charakterystyka biblioteki cDNA wzbogaconej o pełnej długości i wzbogaconej na końcu 5'”. Gen . 200 (1–2): 149–56. doi : 10.1016/S0378-1119(97)00411-3 . PMID 9373149 .
- Louie GV, Yang W, Bowman ME, Choe S (1998). „Struktura krystaliczna kompleksu toksyny błoniczej z zewnątrzkomórkowym fragmentem jej receptora” . Mol. Komórka . 1 (1): 67-78. doi : 10.1016/S1097-2765(00)80008-8 . PMID 9659904 .
- Borer JG, Park JM, Atala A, et al. (1999). „Ekspresja czynnika wzrostu wiążącego heparynę EGF-podobnego zwiększa się selektywnie w mięśniach gładkich pęcherza w odpowiedzi na niedrożność dolnych dróg moczowych”. Laboratorium. Zainwestuj . 79 (11): 1335–45. PMID 10576204 .
- Nakamura K, Mitamura T, Takahashi T i in. (2000). „Znaczenie głównej zewnątrzkomórkowej domeny CD9 i domeny podobnej do naskórkowego czynnika wzrostu (EGF) wiążącego heparynę czynnika wzrostu podobnego do EGF dla regulacji w górę wiązania i aktywności” . J. Biol. Chem . 275 (24): 18284-90. doi : 10.1074/jbc.M907971199 . PMID 10749879 .
- Duque JL, Adam RM, Mullen JS i in. (2001). „Wiążący heparynę naskórkowy czynnik wzrostu podobny do czynnika wzrostu jest autokrynnym mediatorem wzrostu komórek zrębu ludzkiej prostaty in vitro”. J. Urola . 165 (1): 284–8. doi : 10.1097/00005392-200101000-00080 . PMID 11125426 .
- Lin J, Hutchinson L, Gaston SM i in. (2001). „BAG-1 to nowy cytoplazmatyczny partner wiążący błonowej postaci wiążącego heparynę czynnika wzrostu podobnego do EGF: wyjątkowa rola proHB-EGF w regulacji przeżycia komórek” . J. Biol. Chem . 276 (32): 30127-32. doi : 10.1074/jbc.M010237200 . PMID 11340068 .
Zewnętrzne linki
- wiążący heparynę czynnik wzrostu podobny do EGF w amerykańskiej National Library of Medicine Medical Subject Headings (MeSH)