Zasadowy węglan miedzi - Basic copper carbonate

|
|
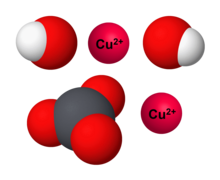
Model wypełniający przestrzeń jednostki formuły podstawowego węglanu miedzi
|
|
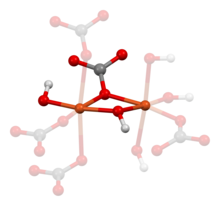
Kulowym i przywieraniu modelu części w strukturze krystalicznej z malachit , podkreślając Formuła jednostkowa
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Diwodorotlenek węglanu dimiedzi
|
|
| Inne nazwy
wodorotlenek węglanu miedzi, węglan miedzi, węglan miedzi, greenium
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.031.909 |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| Cu 2 (OH) 2 CO 3 | |
| Masa cząsteczkowa | 221.114 g/mol |
| Wygląd zewnętrzny | zielony proszek |
| Gęstość | 4 g / cm 3 |
| Temperatura topnienia | 200 ° C (392 ° F; 473 K) |
| Temperatura wrzenia | 290 ° C (554 ° F; 563 K) rozkłada się |
| nierozpuszczalny | |
|
Iloczyn rozpuszczalności ( K sp )
|
7.08·10 -9 |
| Termochemia | |
|
Standardowa
entropia molowa ( S |
88 J/mol·K |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-595 kJ/mol |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | Karta charakterystyki dla Oksfordu |
| Piktogramy GHS |

|
| Hasło ostrzegawcze GHS | Ostrzeżenie |
| H302 , H315 , H319 , H335 | |
| P261 , P305+351+338 | |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
159 mg/kg (szczur, doustnie) |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
TWA 1 mg/m 3 (jako Cu) |
|
REL (zalecane)
|
TWA 1 mg/m 3 (jako Cu) |
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
TWA 100 mg/m 3 (jako Cu) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Zasadowy węglan miedzi jest związkiem chemicznym, dokładniej zwanym wodorotlenkiem węglanu miedzi(II) . Jest to związek jonowy ( sól ) składający się z jonów miedzi(II) Cu2+
, węglan CO2
3, i wodorotlenek OH−
.
Nazwa najczęściej odnosi się do związku o wzorze Cu
2WSPÓŁ
3( OH ) 2 . Jest to zielone, krystaliczne ciało stałe, które występuje w naturze jako mineralny malachit . Jest używany od starożytności jako pigment i nadal jest używany jako taki w farbach artystycznych, czasami nazywanych verditer , green bice lub mountain green .
Czasami nazwa jest używana dla Cu
3( CO
3) 2 ( OH ) 2 , niebieskie krystaliczne ciało stałe znane również jako mineralny azuryt . On również był używany jako pigment, czasami pod nazwą mountain blue lub blue verditer .
Zarówno malachit, jak i azuryt można znaleźć w patynowej patynie, którą można znaleźć na zwietrzałym mosiądzu , brązie i miedzi . Skład patyny może się zmieniać, w środowisku morskim w zależności od środowiska może być obecny zasadowy chlorek, w środowisku miejskim mogą być obecne zasadowe siarczany.
Związek ten nazywa się często nieprawidłowo (również w artykułach chemicznych), węglan miedzi , miedziowego węglanu i tym podobnych nazwami. Prawdziwy (neutralny) węglan miedzi(II) CuCO 3 nie występuje naturalnie. Jest rozkładany przez wodę lub wilgoć z powietrza i został zsyntetyzowany dopiero w 1973 roku przez wysoką temperaturę i bardzo wysokie ciśnienia.
Przygotowanie
Zasadowy węglan miedzi wytwarza się przez połączenie wodnych roztworów siarczanu miedzi(II) i węglanu sodu w temperaturze i ciśnieniu otoczenia . Zasadowy węglan miedzi wytrąca się z roztworu z uwolnieniem dwutlenku węgla CO
2:
- 2 CuSO 4 + 2 Na 2 CO 3 + H 2 O → Cu 2 (OH) 2 CO 3 + 2 Na 2 SO 4 + CO 2
Zasadowy węglan miedzi można również wytworzyć w reakcji wodnych roztworów siarczanu miedzi(II) i wodorowęglanu sodu w warunkach otoczenia. Z roztworu wytrąca się zasadowy węglan miedzi, ponownie z uwolnieniem dwutlenku węgla:
- 2 CuSO 4 + 4 NaHCO 3 → Cu 2 (OH) 2 CO 3 + 2 Na 2 SO 4 + 3 CO 2 + H 2 O
Reakcje
Zasadowy węglan miedzi jest rozkładany przez kwasy, takie jak roztwory kwasu solnego HCl , na sól miedzi(II) i dwutlenek węgla.
W 1794 roku francuski chemik Joseph Louis Proust (1754-1826) rozłożył termicznie węglan miedzi do CO 2 i CuO, tlenku miedzi .
Podstawowe węglany miedzi, malachit i azuryt, rozkładają się tworząc CO 2 i CuO, tlenek miedzi .
Zastosowania
Jako pigmenty stosowano zarówno malachit i azuryt, jak i zasadowy węglan miedzi . Jednym z przykładów wykorzystania zarówno Azuryt i jego forma sztucznej niebieskim verditer jest portret rodziny Balthasar Gerbier przez Petera Paula Rubensa . Zielona osłona Deborah Kip jest malowany azuryt , Smalt , niebieski verditer (postać sztucznego z azuryt) żółtej ochry , ołów-cyna-żółty i żółty jeziora. Zielony kolor uzyskuje się poprzez zmieszanie niebieskiego i żółtego pigmentu.
Był również stosowany w niektórych rodzajach makijażu, takich jak szminka , chociaż może być również toksyczny dla ludzi. Od wielu lat jest również stosowany jako skuteczny środek glonocydowy w stawach hodowlanych i w akwakulturze.

