Zbaczanie -Yaws
| Frambezja | |
|---|---|
| Inne nazwy | Frambesia tropica, grasica, polypapilloma tropicum, nieweneryczna kiła endemiczna, parangi i paru (malajski), bouba (hiszpański), frambösie, pian (francuski), frambesia (niemiecki), bakataw (maguindanaoan) |
 | |
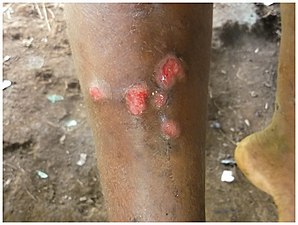
| Guzki na łokciu wynikające z infekcji bakteryjnej Treponema pallidum pertenue | |
| Specjalność | Choroba zakaźna |
| Objawy | Twardy obrzęk skóry, owrzodzenie , ból stawów i kości |
| Powoduje | Treponema pallidum pertenue rozprzestrzeniana przez bezpośredni kontakt |
| Metoda diagnostyczna | Na podstawie objawów, testów przeciwciał krwi , reakcji łańcuchowej polimerazy |
| Zapobieganie | Leczenie masowe |
| Lek | Azytromycyna , penicylina benzatynowa |
| Częstotliwość | 46 000–500 000 |
Yaws to tropikalna infekcja skóry , kości i stawów wywołana przez bakterię krętka Treponema pallidum pertenue . Choroba zaczyna się od okrągłego, twardego obrzęku skóry o średnicy od 2 do 5 cm (0,79 do 1,97 cala). Środek może pęknąć i utworzyć owrzodzenie . Ta początkowa zmiana skórna zwykle goi się po 3–6 miesiącach. Po tygodniach lub latach stawy i kości mogą stać się bolesne, może rozwinąć się zmęczenie i mogą pojawić się nowe zmiany skórne. Skóra dłoni i podeszwy stóp może stać się gruba i pękać. Kości (zwłaszcza nosowe) mogą ulec zniekształceniu. Po 5 latach lub dłużej duże obszary skóry mogą umrzeć, pozostawiając blizny.
Faza rozprzestrzenia się poprzez bezpośredni kontakt z płynem ze zmiany chorobowej osoby zakażonej. Kontakt ma zwykle charakter nieseksualny. Choroba najczęściej występuje u dzieci, które rozprzestrzeniają ją poprzez wspólne zabawy. Inne pokrewne choroby krętkowe to bejel ( T. pallidum endemicum ), pinta ( T. carateum ) i kiła ( T. p. pallidum ). Fazę często diagnozuje się na podstawie pojawienia się zmian. Testy na obecność przeciwciał we krwi mogą być przydatne, ale nie mogą oddzielić wcześniejszych infekcji od obecnych. Reakcja łańcuchowa polimerazy jest najdokładniejszą metodą diagnozy.
Nie znaleziono jeszcze szczepionki. Zapobieganie polega po części na leczeniu chorych na tę chorobę, co zmniejsza ryzyko transmisji. Tam, gdzie choroba jest powszechna, skuteczne jest leczenie całej społeczności. Poprawa czystości i warunków sanitarnych zmniejsza również rozprzestrzenianie się. Leczenie obejmuje zazwyczaj antybiotyki , w tym: azytromycynę doustną lub penicylinę benzatynową we wstrzyknięciach. Bez leczenia deformacje fizyczne występują w 10% przypadków.
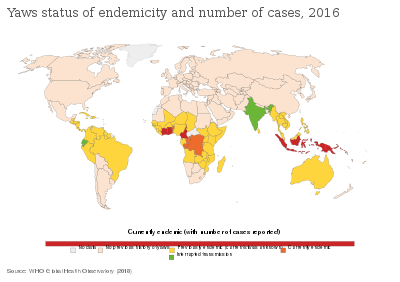
W 2012 r. często występuje w co najmniej 13 krajach tropikalnych . Prawie 85% infekcji wystąpiło w trzech krajach — Ghanie , Papui Nowej Gwinei i Wyspach Salomona . Choroba zaraża tylko ludzi. Wysiłki Światowej Organizacji Zdrowia w latach 50. i 60. zmniejszyły liczbę przypadków o 95%. Od tego czasu liczba zachorowań wzrosła, ale dzięki wznowionym wysiłkom zmierzającym do globalnego wyeliminowania choroby do 2020 r. W 1995 r. liczbę zarażonych osób oszacowano na ponad 500 000. W 2016 r. liczba zgłoszonych przypadków wyniosła 59 000. Chociaż jeden z pierwszych opisów choroby został sporządzony w 1679 roku przez Willema Piso , dowody archeologiczne sugerują, że u przodków człowieka mogło występować już 1,6 miliona lat temu.
objawy i symptomy
Yaws jest klasyfikowany jako podstawowy, drugorzędny i trzeciorzędny; jest to przydatne, ale ludzie często mają mieszankę etapów.
W ciągu 9-90 dni (ale zwykle około 21 dni) od zakażenia pojawia się bezbolesny, ale charakterystyczny guzek „matki zboczenia” . Początkowo zaczerwieniony i zaogniony , może stać się brodawczakiem , a następnie wrzodem , prawdopodobnie z żółtą skórką. Zboczenie matki jest najczęściej spotykane na nogach i kostkach, a rzadko na genitaliach (w przeciwieństwie do kiły). Zboczenie matki powiększa się i staje się brodawkowate. Równocześnie mogą pojawiać się również pobliskie „fasady córki”. Ten pierwotny etap całkowicie ustępuje, z bliznowaceniem, w ciągu 3–6 miesięcy. Blizna jest często pigmentowana.
Faza wtórna pojawia się kilka miesięcy do dwóch lat później (ale zwykle 1–2 miesiące później) i może zatem rozpocząć się, gdy matczyne zboczenie jeszcze się nie zagoiło. Dzieje się tak, gdy bakteria rozprzestrzenia się we krwi i limfie. Zaczyna się jako wiele grudek przypominających główkę od szpilki ; te początkowe zmiany rosną i zmieniają wygląd i mogą utrzymywać się tygodnie przed wygojeniem, z bliznami lub bez.
Wtórne zbaczanie zazwyczaj wykazuje rozległe zmiany skórne, które różnią się wyglądem, w tym „krabie ziewanie” (obszary skóry o nieprawidłowym kolorze) na dłoniach i podeszwach stóp (nazwane od chodu kraba, który powodują u osób z bolesnymi podeszwami zakładać). Mogą one wykazywać złuszczanie . Te wtórne zmiany często ulegają owrzodzeniu, a następnie są wysoce zakaźne, ale goją się po 6 miesiącach lub dłużej.
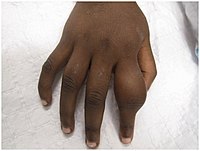
Faza wtórna wpływa na skórę i kości. Najczęstszym problemem związanym z kośćmi jest zapalenie okostnej , zapalenie wokół kości, które często występuje w kościach palców i długich kościach przedramion i nóg, powodując obrzęk palców i kończyn. Powoduje to ból w nocy i zgrubienie dotkniętych kości (zapalenie okostnej). Około 75% zarażonych dzieci ankietowanych w Papui Nowej Gwinei zgłosiło ból stawów. Częste są również obrzęk węzłów chłonnych , gorączka i złe samopoczucie.
Po pierwotnym i wtórnym odchyleniu (i ewentualnie w niektórych przypadkach bez tych faz) rozwija się utajona infekcja. W ciągu pięciu lat (rzadko w ciągu dziesięciu) może nawrócić i ponownie uaktywnić się, powodując kolejne wtórne zmiany, które mogą zarażać innych. Te zmiany nawrotowe najczęściej znajdują się wokół pach, ust i odbytu.
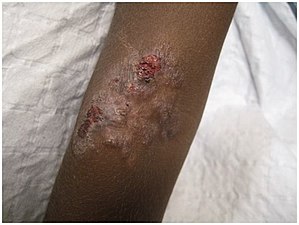
Zmiany wtórne różnią się wyglądem (patrz lista terminów )
Tutaj dwa różne wyglądy (blaszka grudkowo-płaskonabłonkowa i guzki z żółtą skorupą ) są widoczne u tej samej 10-latki (obie w dużej skali, zbliżenie guzków)
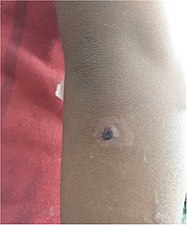
odchylenia wtórne; odbarwione obszary skóry pokryte różowymi i brązowymi grudkami , 9-latek
Erozja na podeszwie stopy, zbliżenie ( duża skala ). Gdyby był głębszy, byłby to wrzód
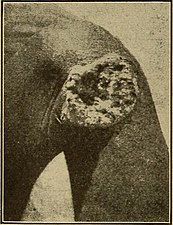
Wybuch wtórny u dziecka jawajskiego w wieku 12 lat. Model woskowy
Szacuje się, że u 10% osób z odchyleniem dawniej rozwijają się objawy trzeciorzędowej choroby, ale ostatnio rzadziej zgłaszano trzeciorzędowe odchylenia.
Fasady trzeciorzędowe mogą obejmować guzki gumowate . Najczęściej wpływa na skórę. Skóra dłoni i podeszew może zgęstnieć ( hiperkeratoza ). Guzki owrzodzenia w pobliżu stawów mogą powodować obumieranie tkanek . Zapalenie okostnej może być znacznie cięższe. Piszczele mogą być wygięte (goleń szabli) z przewlekłego zapalenia okostnej.
Faza może, ale nie musi mieć skutków sercowo-naczyniowych lub neurologicznych ; brakuje ostatecznych dowodów.
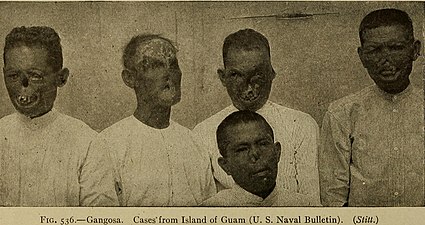
okaleczające zapalenie błony śluzowej nosa i gardła
Okaleczające zapalenie błony śluzowej nosa i gardła , znane również jako gangosa , jest niszczącą chorobą wrzodową , która zwykle wywodzi się z podniebienia miękkiego i rozprzestrzenia się na podniebienie twarde , nosogardło i nos , powodując blizny , a na zewnątrz twarzy , erodując kości , chrząstki i chrząstki . tkanki miękkie . Występuje w późnych stadiach odchylenia, zwykle od 5 do 10 lat po pierwszych objawach infekcji . To jest teraz rzadkie. Bardzo rzadko, zboczenie może powodować ostrogi kostne w górnej szczęce w pobliżu nosa (gondou); gondou był rzadki, nawet wtedy, gdy yaws był powszechną chorobą.
Przyczyna
Choroba jest przenoszona przez kontakt ze skórą ze zmianą zakaźną, w której bakteria przedostaje się przez wcześniej istniejące skaleczenie, ugryzienie lub zadrapanie.
Wczesne (pierwotne i wtórne) zmiany fałdowe mają większy ładunek bakteryjny, przez co są bardziej zakaźne. Zarówno brodawczaki, jak i wrzody są zakaźne. Uważa się, że zakaźność trwa 12-18 miesięcy po zakażeniu, dłużej w przypadku nawrotu. Wczesne zmiany chorobowe często są swędzące, a więcej zmian może tworzyć się wzdłuż linii, które są zadrapane . Fałdy mogą ewoluować w mniej widocznych zmianach.
Fałszowanie występuje najczęściej wśród dzieci, które rozprzestrzeniają je poprzez wspólną zabawę. Uważa się, że nie przenosi się z matki na dziecko w łonie matki. Yaws nie jest chorobą weneryczną .
T. pallidum pertenue został zidentyfikowany u naczelnych innych niż człowiek ( pawiany , szympansy i goryle ), a eksperymentalna inokulacja istot ludzkich izolatem małpy powoduje chorobę podobną do odchylenia. Jednak nie ma dowodów na krzyżową transmisję między ludźmi a naczelnymi, ale potrzebne są dalsze badania, aby zdyskontować możliwość występowania rezerwuaru zwierzęcego u naczelnych innych niż człowiek.
Diagnoza
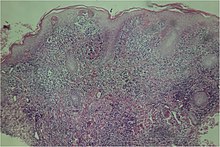
Najczęściej diagnozę stawia się klinicznie. Mikroskopia ciemnego pola próbek pobranych z wczesnych zmian chorobowych (szczególnie zmian wrzodziejących) może pokazać odpowiedzialne bakterie; krętki mają tylko 0,3 µm szerokości i 6–20 µm długości, więc mikroskopia w polu świetlnym nie wystarczy.
Badanie mikroskopowe biopsji zboczenia może wykazać skórę z wyraźnym przerostem naskórka (rodzaj zgrubienia skóry) i brodawczakowatością (rodzaj nieregularności powierzchni), często z ogniskową gąbczastą (nagromadzenie płynu w określonej części naskórka). Komórki układu odpornościowego , granulocyty obojętnochłonne i komórki plazmatyczne gromadzą się w skórze w zagęszczeniach, które mogą powodować mikroropnie.
Barwienie srebrem Warthina-Starry'ego lub Levaditiego wybiórczo barwi T. pallidum , a bezpośrednie i pośrednie testy immunofluorescencyjne i immunoperoksydazy mogą wykryć przeciwciała poliklonalne przeciwko T. pallidum . Histologia często wykazuje pewne cechy przestrzenne, które odróżniają kiłę od kiły (kiła częściej występuje w skórze właściwej, a nie w naskórku i wykazuje większą proliferację komórek śródbłonka i obliterację naczyń ).
Testy surowicy krwi (serologiczne) są coraz częściej wykonywane w miejscu opieki. Obejmują one rosnący zakres testów krętkowych i niekrętkowych. Testy krętkowe są bardziej szczegółowe i są pozytywne dla każdego, kto kiedykolwiek został zarażony zboczeniem; obejmują one test aglutynacji cząstek Treponema pallidum . Testy niekrętkowe mogą być użyte do wskazania postępu infekcji i wyleczenia, a pozytywne wyniki słabną i mogą stać się negatywne po wyzdrowieniu, zwłaszcza po wczesnym leczeniu. Obejmują one badania laboratoryjne nad chorobami wenerycznymi ( VDRL ; wymaga mikroskopii) i szybkie testy reaginowe w osoczu ( RPR ; wynik gołym okiem), z których oba gromadzą przeciwciała pochodzące od pacjenta z antygenami .
Testy serologiczne nie potrafią odróżnić kiły od blisko spokrewnionej kiły ; żaden test odróżniający zbaczanie od kiły nie jest powszechnie dostępny. Oba genomy różnią się o około 0,2%. Sekwencjonowanie PCR i DNA może je rozróżnić. Nie ma również wspólnych badań krwi, które rozróżniają cztery treponematozy : kiłę (Treponema pallidum pallidum), ziewanie (Treponema pallidum pertenue), bejel (Treponema pallidum endemicum) i pinta (Treponema carateum).
Infekcje Haemophilus ducreyi mogą powodować choroby skóry, które naśladują pierwotne krzywienie. Osoby zakażone zmianami Haemophilus ducreyi mogą, ale nie muszą mieć utajonego odchylenia, a zatem mogą, ale nie muszą, uzyskać dodatni wynik w testach serologicznych. Zostało to odkryte w połowie 2010 roku. Wydaje się, że niedawno odmienny szczep Haemophilus ducreyi przekształcił się z zakażenia przenoszonego drogą płciową w patogen wrzodu skóry, który wygląda jak ziewanie.
Odnotowano odchylenia w krajach nieendemicznych.
Leczenie
Leczenie polega zwykle na pojedynczym wstrzyknięciu domięśniowym długo działającej benzatynowej penicyliny benzylowej lub rzadziej na serii innych antybiotyków, takich jak tabletki azytromycyny lub tetracykliny . Penicylina jest lekiem pierwszego rzutu od co najmniej lat 60., ale nie ma solidnych dowodów na ewolucję oporności na penicylinę u krzywych.
Historyczna strategia zwalczania odchyleń (1952-1964) była następująca:
| Częstość występowania klinicznie aktywnych odchyleń | Strategia leczenia |
|---|---|
| Hiperendemiczny: powyżej 10% | Benzynopenicylina benzylowa dla całej społeczności
(całkowita kuracja masowa) |
| Mezoendemiczny: 5–10% | Leczyć wszystkie aktywne przypadki, wszystkie dzieci poniżej 15 roku życia i wszystkie kontakty z przypadkami zakaźnymi
(masa młodociana) |
| Hipendemiczny: poniżej 5% | Traktuj wszystkie aktywne sprawy oraz wszystkie kontakty domowe i inne
(selektywne leczenie masowe) |
Benzatyna penicylina benzylowa wymaga łańcucha chłodniczego i personelu, który może ją wstrzykiwać, a ryzyko anafilaksji jest niewielkie . Nie był również dostępny w sposób wiarygodny w 2010 roku; wystąpiły niedobory dostaw.
W 2010 roku pojedyncza doustna dawka azytromycyny okazała się równie skuteczna jak domięśniowa penicylina. W przeciwieństwie do penicyliny istnieją mocne dowody na to, że yaws rozwija oporność antybiotykową na azytromycynę; istnieją dwie znane mutacje w bakterii, z których każda może wywołać oporność i sprawić, że leczenie będzie nieskuteczne. Zagroziło to wysiłkom zwalczania.
W ciągu 8–10 godzin leczenia penicyliną w biopsjach zmian chorobowych nie można już znaleźć bakterii. Zmiany pierwotne i wtórne zwykle goją się w ciągu 2–4 tygodni; ból kości może ulec poprawie w ciągu dwóch dni. Odpowiednio wcześnie leczone deformacje kości mogą ulec odwróceniu i zagojeniu. Zmiany w stadium pierwotnym i wtórnym mogą zagoić się całkowicie, ale destrukcyjne zmiany w trzeciorzędowych odchyleniach są w dużej mierze nieodwracalne.
Jeśli zmiany nie goją się lub wyniki testu RPR nie ulegają poprawie, może to wskazywać na niepowodzenie leczenia lub ponowne zakażenie; leczenie jest zazwyczaj powtarzane. Wytyczne WHO mówią, że wszelkie przypuszczalne niepowodzenia leczenia po 4 tygodniach wymagają testowania oporności na makrolidy .
Epidemiologia
Tam, gdzie kończy się droga, zaczyna się zbaczanie
— powiedzenie WHO, cytowane przez Kingsleya Asiedu.
Ponieważ T. pallidum pertenue jest zależny od temperatury i wilgotności, yaws występuje w wilgotnych regionach lasów tropikalnych w Ameryce Południowej , Afryce , Azji i Oceanii .
Około trzy czwarte osób dotkniętych chorobą to dzieci w wieku poniżej 15 lat, z największą zachorowalnością u dzieci w wieku 6–10 lat. Dlatego dzieci są głównym rezerwuarem infekcji.
Częściej występuje na obszarach oddalonych, gdzie dostęp do leczenia jest utrudniony. Kojarzy się z biedą i złymi warunkami sanitarnymi i higieną osobistą.
Na całym świecie prawie 85% przypadków dewiacji występuje w Ghanie, Papui Nowej Gwinei i na Wyspach Salomona. Wskaźniki w Afryce Subsaharyjskiej są niskie, ale zwykle koncentrują się w określonych populacjach. Szacuje się, że w 2015 r. około 89 milionów ludzi żyje na obszarach endemicznych, w których występuje zboczenie, ale dane są skąpe i jest to prawdopodobnie zawyżone szacunki.
Na początku XX wieku zbaczanie było bardzo powszechne; w Afryce Subsaharyjskiej był leczony częściej niż malaria, czasami stanowiąc ponad połowę zabiegów.
Kampanie masowego leczenia w latach 50. zmniejszyły rozpowszechnienie na całym świecie z 50 do 150 milionów do mniej niż 2,5 miliona; jednak w latach 70. wybuchły epidemie w Azji Południowo-Wschodniej , a sporadyczne przypadki kontynuowane są w Ameryce Południowej. Od 2011 roku nie było jasne, ile osób na całym świecie jest obecnie zarażonych.
W latach 2008-2012 13 krajów zgłosiło WHO ponad 300 000 nowych przypadków. Nie było systemu poświadczania lokalnej eliminacji zbaczania i nie wiadomo, czy brak zgłoszeń z niektórych krajów wynika z tego, że przestali mieć przypadki zachorowań, czy też przestali je zgłaszać. Szacuje się, że jeśli nie ma aktywnego programu nadzoru, jest mniej niż 1 na 2 szanse, że kraj z powodzeniem zgłosi przypadki odchyleń (jeśli je otrzyma) w ponad trzech czwartych krajów z historią odchyleń. . Uważa się, że kraje te potrzebują międzynarodowej pomocy, aby wprowadzić skuteczny nadzór.
Ogólnie rzecz biorąc, yaws nie jest chorobą podlegającą obowiązkowi zgłoszenia .
Historia
Badanie szczątków Homo erectus z Kenii , które mają około 1,6 mln lat, ujawniło oznaki typowe dla odchyleń. Analiza genetyczna bakterii wywołujących yaws — Treponema pallidum pertenue — doprowadziła do wniosku, że yaws jest najstarszą z czterech znanych chorób Treponema . Wszystkie inne podgatunki Treponema pallidum prawdopodobnie wyewoluowały z Treponema pallidum pertenue . Uważa się, że Yaws pochodzi z tropikalnych obszarów Afryki i rozprzestrzenił się na inne tropikalne obszary świata poprzez imigrację i handel niewolnikami . Ten ostatni jest prawdopodobnie sposobem, w jaki został sprowadzony do Europy z Afryki w XV wieku. Pierwszego jednoznacznego opisu odchyleń dokonał holenderski lekarz Willem Piso . Ziewanie zostało wyraźnie opisane w 1679 r. wśród afrykańskich niewolników przez Thomasa Sydenhama w swoim liście o chorobach wenerycznych , chociaż uważał, że to ta sama choroba, co kiła . Czynnik ten został odkryty w 1905 roku przez Aldo Castellani w wrzodach pacjentów z Cejlonu .
Uważa się, że obecna angielska nazwa pochodzi od Carib , od „yaya”, co oznacza ból.
Pod koniec II wojny światowej, pod okupacją japońską, na północy Malajów rozpowszechniły się odchylenia. Po wyzwoleniu kraju ludność leczono na zboczenie zastrzykami z arszeniku, którego bardzo brakowało, więc leczono tylko osoby z 1. stadium.
Likwidacja
Seria prób kontroli odchyleń WHO, które rozpoczęły się wkrótce po utworzeniu WHO w 1948 r., doprowadziła do lokalnego wykorzenienia choroby w wielu krajach, ale nie trwała wystarczająco długo, aby zwalczyć ją na całym świecie. Program Global Control of Treponematoses (TCP) prowadzony przez WHO i UNICEF rozpoczął się w 1952 r. i trwał do 1964 r. Oszacowano na podstawie kwestionariusza z 1953 r., że w 90 krajach było 50–150 mln przypadków odchyleń. Globalna częstość występowania krętków i innych endemicznych krętków, bejel i pinta , została zmniejszona przez program Global Control of Treponematoses (TCP) w latach 1952-1964 z około 50 milionów przypadków do około 2,5 miliona (redukcja o 95%). Jednak „przedwczesna integracja aktywności krętków i innych endemicznych krętków w słabych systemach podstawowej opieki zdrowotnej oraz demontaż programów pionowej eradykacji po 1964 r. doprowadziły do nieukończenia w pozostałych 5% przypadków” i doprowadziły do odrodzenia odchyleń w latach 70., z największą liczbą przypadków w regionie Afryki Zachodniej. Po zaprzestaniu tego programu, zasoby, uwaga i zaangażowanie w walkę z wahaniem stopniowo zanikały, a w niektórych częściach Azji, Afryki i obu Ameryk, ze sporadycznymi wybuchami epidemii, częstość występowania tego zjawiska utrzymywała się na niskim poziomie. Z kilkoma przypadkami, dotykającymi głównie ubogie, odległe społeczności, z niewielkim dostępem do leczenia, frejkowanie stało się słabo znane, wiedza i umiejętności dotyczące tego zjawiska wymarły nawet wśród pracowników służby zdrowia, a eliminacja frejma nie była postrzegana jako wysoki priorytet. Chociaż pojedyncze wstrzyknięcie długo działającej penicyliny lub innego antybiotyku beta-laktamowego leczy chorobę i jest powszechnie dostępne, a choroba jest wysoce zlokalizowana, wiele kampanii eradykacyjnych zakończyło się samozadowoleniem i zaniedbaniem; nawet na obszarach, gdzie transmisja została pomyślnie przerwana, nastąpiło ponowne wprowadzenie wirusa z zakażonych obszarów. Likwidacja odchyleń pozostała priorytetem w południowo-wschodniej Azji. W 1995 roku WHO oszacowała 460 000 przypadków na całym świecie.
Na Filipinach w 1973 r. framczak przestał być wymieniany jako choroba podlegająca obowiązkowi zgłoszenia ; od 2020 roku nadal jest obecny w kraju.
Indie wdrożyły udaną kampanię zwalczania odchyleń, która zaowocowała certyfikatem WHO w 2016 r., że Indie są wolne od odchyleń. W 1996 roku w Indiach było 3571 przypadków odchyleń; w 1997 r., po rozpoczęciu poważnych wysiłków eliminacyjnych, liczba przypadków spadła do 735. Do 2003 r. liczba przypadków wyniosła 46. Ostatni przypadek kliniczny w Indiach zgłoszono w 2003 r., a ostatni przypadek utajony w 2006 r.; certyfikacja WHO została osiągnięta w 2016 roku.
W 2012 r. WHO oficjalnie skierowała do 2020 r. dezynsekcję w celu wyeliminowania jej po opracowaniu doustnie podawanej azytromycyny jako leczenia, ale nie osiągnęła tego celu. Podejście Morgesa (od nazwiska Morges w Szwajcarii, gdzie odbyło się spotkanie na jego temat) obejmowało masowe leczenie azytromycyną . Było to bezpieczne, ale napotkało problemy z opornością na antybiotyki i nie przerwało całkowicie transmisji.
Odkrycie, że doustny antybiotyk azytromycyna może być stosowany zamiast dotychczasowego standardu, wstrzykiwanej penicyliny , było testowane na wyspie Lihir w latach 2013-2014; pojedyncza doustna dawka antybiotyku makrolidowego zmniejszyła częstość występowania choroby z 2,4% do 0,3% po 12 miesiącach. Obecnie WHO zaleca oba kursy leczenia (doustna azytromycyna i wstrzykiwana penicylina), przy czym preferowaną metodą leczenia jest doustna azytromycyna.
W 2020 r. było 15 krajów znanych jako endemiczne dla zboczenia, z niedawnym odkryciem transmisji endemicznej w Liberii i na Filipinach . W 2020 r. do WHO zgłoszono 82 564 przypadki odchyleń i potwierdzono 153 przypadki. Większość przypadków pochodzi z Papui Nowej Gwinei , a ponad 80% wszystkich przypadków pochodzi z jednego z trzech krajów w okresie 2010–2013: Papui Nowej Gwinei, Wysp Salomona i Ghany. Raport ze spotkania WHO z 2018 r. oszacował całkowity koszt eliminacji na 175 mln USD (z wyłączeniem Indonezji).
W Biurze Regionalnym WHO Azji Południowo-Wschodniej, regionalne wysiłki w zakresie zwalczania koncentrują się na pozostałych endemicznych krajach tego regionu ( Indonezja i Timor Wschodni ) po tym , jak Indie zostały uznane za wolne od odchyleń w 2016 r.
Chociaż zboczenie jest wysoce zlokalizowane i jego wykorzenienie może być wykonalne, ludzie mogą nie być jedynym rezerwuarem infekcji.
Bibliografia
Zewnętrzne linki
- " Treponema pallidum subsp. pertenue " . Przeglądarka taksonomii NCBI . 168.