Winylogia - Vinylogy
Winylogia to przekazywanie efektów elektronicznych poprzez sprzężony system wiązań organicznych. Koncepcja została wprowadzona w 1926 roku przez Ludwiga Claisena w celu wyjaśnienia kwasowych właściwości formyloacetonu i pokrewnych ketoaldehydów. Jego forma przymiotnikowa, winylogeniczna , jest używana do opisania grup funkcyjnych, w których standardowe ugrupowania grupy są oddzielone podwójnym wiązaniem węgiel-węgiel. Na przykład kwas karboksylowy z podwójnym wiązaniem węgiel-węgiel (-HC = CH-, ugrupowanie „ winylowe ”; właściwie grupa winylenowa) między grupą karbonylową a grupą hydroksylową jest określany jako winylogenny kwas karboksylowy .
Ze względu na przekazywanie informacji elektronicznych poprzez koniugację winylogiczne grupy funkcyjne często mają „ analogiczną ” reaktywność lub właściwości chemiczne w porównaniu z macierzystą grupą funkcyjną. Dlatego winylogia jest użyteczną heurystyką do przewidywania zachowania systemów, które są strukturalnie podobne, ale zawierają pośrednie wiązania C = C, które są sprzężone z dołączonymi grupami funkcyjnymi. Na przykład kluczową właściwością kwasów karboksylowych jest ich kwasowość Brønsteda. Najprostszy kwas karboksylowy, kwas mrówkowy (HC (= O) –OH), jest umiarkowanie mocnym kwasem organicznym o ap K a 3,7. Spodziewalibyśmy się, że winylogenowe kwasy karboksylowe będą miały podobną kwasowość. Rzeczywiście, winyloog kwasu mrówkowego, 2-formylo-1-eten-1-ol, HC (= O) –CH = CH – OH ma znaczną kwasowość Brønsteda, z szacowaną wartością p K a ~ 5-6. W szczególności vinylogous kwasy karboksylowe, kwasy są znacznie silniejsze niż typowe enole (p K a ~ 12). Witamina C ( kwas askorbinowy , patrz poniżej ) jest biologicznie ważnym przykładem winylogawego kwasu karboksylowego.
Wstawienie o- lub p- fenylenu (tj. Pierścienia benzenowego w orientacji 1,2 lub 1,4) również powoduje pewne podobieństwa w reaktywności (zwane „fenologią”), chociaż efekt jest ogólnie słabszy, ponieważ sprzęganie przez pierścień arylowy wymaga rozważenia form rezonansowych lub związków pośrednich, w których zaburzona jest aromatyczność.

Reaktywność winylogenna
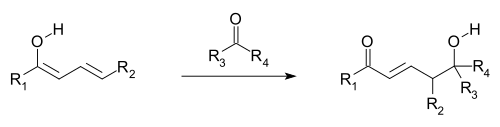
Uważa się, że reakcje winylogeniczne zachodzą, gdy orbitale podwójnych wiązań grupy winylowej i przyłączonej grupy wyciągającej elektrony (EWG; orbitale π) są wyrównane, a zatem mogą nakładać się i mieszać (tj. Są sprzężone ). Delokalizacja elektronów umożliwia EWG otrzymanie gęstości elektronów poprzez udział układu sprzężonego. Reakcje winylogeniczne obejmują również addycje koniugatów , w których nukleofil reaguje na końcu winylowym, a także winylogeniczną odmianę reakcji aldolowej , w której elektrofil jest atakowany przez nukleofilowy winylogenny enolan (patrz pierwszy i następny obraz). Winylogenny enolan reaguje raczej w końcowej pozycji układu podwójnych wiązań (węgiel γ), a nie α-węgiel bezpośrednio przylegający do karbonylu, tak jak zwykły enolan. Aliliczne elektrofile często reagują raczej przez winylogeniczny atak nukleofila niż bezpośrednią addycję.
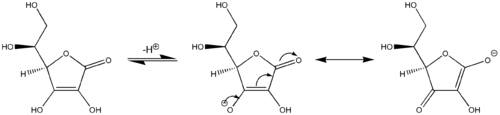
Kolejny przykład winylogennej reaktywności: kwas askorbinowy (witamina C) zachowuje się jak winylogenowy kwas karboksylowy poprzez zaangażowanie jego ugrupowania karbonylowego, grupy winylowej w pierścieniu i samotnej pary na grupie hydroksylowej działającej jako układ sprzężony . Kwasowość protonu hydroksylowego na końcu grupy winylowej w kwasie askorbinowym jest bardziej porównywalna z typowym kwasem karboksylowym niż alkoholem, ponieważ dwie główne struktury rezonansowe stabilizują ujemny ładunek na sprzężonej zasadzie kwasu askorbinowego (centralna i prawa struktura na ostatnim zdjęciu ), analogicznie do dwóch struktur rezonansowych, które stabilizują ujemny ładunek anionu wynikający z usunięcia protonu z prostego kwasu karboksylowego (por. pierwszy obraz). Analogicznie, pochodne kwasu sorbinowego , wydłużone o inne ugrupowanie „winylowe”, również wykazują właściwości winylogenne.
Dalsza lektura
- Lisboa, Marilda P .; Hoang, Tung T .; Dudley, Gregory B. (2011). „Tandem Nukleofilowe Dodawanie / Fragmentacja Winylogenowych Acyl Triflat: 2-Metylo-2- (1-Okso-5-Heptynylo) -1,3-Ditian” . Synteza organiczna . 88 : 353. doi : 10.15227 / orgsyn.088.0353 .