Fluorek cyny(IV) - Tin(IV) fluoride
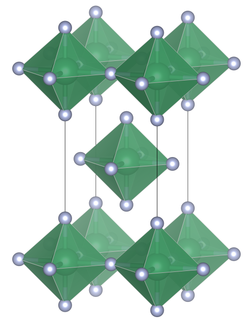 Komórka elementarna fluorku cyny(IV)
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
fluorek cyny(IV)
|
|
| Inne nazwy
fluorek cynowy, tetrafluorek cyny
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| Karta informacyjna ECHA |
100.029.105 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
|
|
|
| Nieruchomości | |
| SnF 4 | |
| Masa cząsteczkowa | 194,704 g/mol |
| Wygląd zewnętrzny | białe ciało stałe |
| Temperatura topnienia | powyżej 700 °C (sublimuje) |
| Struktura | |
| Czworokątny , Ti10 | |
| I4/mmm, nr 139 | |
| Związki pokrewne | |
|
Inne aniony
|
Chlorek cyny(IV) Bromek cyny(IV) Jodek cyny(IV) |
|
Inne kationy
|
Tetrafluorek węgla Tetrafluorek krzemu Tetrafluorek germanu Tetrafluorek cyny Tetrafluorek ołowiu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Cyny (IV), fluorek jest związek chemiczny z cyny i fluoru z wzoru chemicznego SNF 4 i jest białym ciałem stałym o temperaturze topnienia powyżej 700 ° C.
SnF 4 można otrzymać w reakcji metalicznej cyny z gazowym fluorem:
- Sn + 2F 2 → SnF 4
Jednak utworzy się pasywująca warstwa fluorku metalu i powierzchnia w końcu stanie się niereaktywna. Alternatywną syntezę stanowi reakcja SnCl 4 bezwodnym fluorowodorem :
- SnCI 4 + 4HF → SNF 4 + 4HCl
Z fluorki metali alkalicznych (np KF) hexafluorostannates wytwarza (EGK 2 SNF 6 ), która zawiera ośmiościenny SNF 6 2- anionu. SnF 4 zachowuje się jak kwas Lewisa i powstały addukty L 2 · SnF 4 i L · SnF 4 .
Struktura
W przeciwieństwie do innych cyny tetrahalogenki , cyna (IV), chlorek , (IV), bromek cyny i cyny (IV), jodek , które zawierają tetraedrycznie skoordynowane cyny, cyna (IV), fluorek zawiera płaskie warstwy octahedrally skoordynowany cyny, gdzie udział ośmiościanów czterech rogach i istnieją dwa terminalne, nie dzielone atomy fluoru trans względem siebie. Temperatura topnienia SNF 4 jest znacznie wyższa (700 ° C) niż drugi cyny (IV), halogenki, które mają stosunkowo niską temperaturę topnienia, ( SnCl 4 , -33,3 ° C; SnBr 4 , 31 ° C; sni 4 , 144 ° C, ). Struktura ta może być również kontrastuje z tetrafluorides zapalniczki członków grupy 14, ( CF 4 , SiF 4 i Gef 4 ), który w stałych kryształów molekularnym tworzy stan.
