Tężec - Tetanus
| Tężec | |
|---|---|
| Inne nazwy | Tężec |
 | |
| Skurcze mięśni (w szczególności opisthotonos ) u osoby z tężcem. Obraz Sir Charlesa Bella , 1809. | |
| Specjalność | Choroba zakaźna |
| Objawy | Skurcze mięśni , gorączka , ból głowy |
| Zwykły początek | 3–21 dni po ekspozycji |
| Czas trwania | Miesiące |
| Powoduje | Clostridium tetani |
| Czynniki ryzyka | Przerwa w skórze |
| Metoda diagnostyczna | Na podstawie objawów |
| Zapobieganie | Szczepionka przeciwtężcowa |
| Leczenie | Immunoglobulina tężcowa , leki zwiotczające mięśnie , wentylacja mechaniczna |
| Rokowanie | 10% ryzyko śmierci |
| Częstotliwość | 209 000 (2015) |
| Zgony | 56 700 (2015) |
Tężec , znany również jako szczękościsk , to infekcja bakteryjna charakteryzująca się skurczami mięśni . W najczęstszym typie skurcze zaczynają się w szczęce, a następnie przechodzą na resztę ciała. Każdy skurcz trwa zwykle kilka minut. Skurcze występują często przez trzy do czterech tygodni. Niektóre skurcze mogą być na tyle poważne, że mogą złamać kości . Inne objawy tężca mogą obejmować gorączkę , pocenie się , bóle głowy , problemy z połykaniem , wysokie ciśnienie krwi i szybkie bicie serca . Początek objawów występuje zwykle od trzech do dwudziestu jeden dni po zakażeniu. Odzyskiwanie może potrwać miesiące. Około dziesięć procent przypadków kończy się śmiercią .
Tężec jest spowodowany infekcją bakterią Clostridium tetani , która powszechnie występuje w glebie, ślinie, kurzu i oborniku. Bakterie zazwyczaj wnikają przez przerwę w skórze, taką jak skaleczenie lub ukłucie przez skażony przedmiot. Wytwarzają toksyny, które zakłócają normalne skurcze mięśni. Diagnoza opiera się na prezentowanych objawach i objawach. Choroba nie rozprzestrzenia się między ludźmi.
Tężec może być uniemożliwione przez immunizację z tężcowi . U osób, które mają znaczną ranę i otrzymały mniej niż trzy dawki szczepionki, zaleca się zarówno szczepienie, jak i immunoglobulinę przeciwtężcową . Rana powinna zostać oczyszczona i usunięta martwa tkanka. U osób zakażonych stosuje się immunoglobulinę przeciwtężcową lub, jeśli nie jest dostępna, immunoglobulinę dożylną (IVIG). Środki zwiotczające mięśnie mogą być stosowane do kontrolowania skurczów. Wentylacja mechaniczna może być wymagana w przypadku upośledzenia oddychania.
Tężec występuje we wszystkich częściach świata, ale najczęściej występuje w gorącym i wilgotnym klimacie, gdzie gleba ma wysoką zawartość substancji organicznych. W 2015 roku na całym świecie odnotowano około 209 000 infekcji i około 59 000 zgonów. Jest to spadek z 356 000 zgonów w 1990 roku. W Stanach Zjednoczonych jest około 30 przypadków rocznie, z których prawie wszystkie nie zostały zaszczepione. Wczesny opis choroby został dokonany przez Hipokratesa w V wieku p.n.e. Przyczynę choroby ustalili w 1884 roku Antonio Carle i Giorgio Rattone na Uniwersytecie Turyńskim , a szczepionkę opracowano w 1924 roku.
Symptomy i objawy
Tężec często zaczyna się od łagodnych skurczów mięśni szczęki – znanych również jako szczękościsk lub szczękościsk . Skurcze mogą również wpływać na mięśnie twarzy, powodując wygląd zwany risus sardonicus . Może to mieć wpływ na klatkę piersiową, szyję, plecy, mięśnie brzucha i pośladki. Skurcze mięśni pleców często powodują wygięcia , zwane opistotonami . Czasami skurcze wpływają na mięśnie, które pomagają w oddychaniu, co może prowadzić do problemów z oddychaniem.
Przedłużone działanie mięśni powoduje nagłe, silne i bolesne skurcze grup mięśniowych, co nazywa się „tężyczką”. Te epizody mogą powodować złamania i naderwania mięśni. Inne objawy to gorączka , ból głowy , niepokój, drażliwość , trudności w karmieniu, problemy z oddychaniem , pieczenie podczas oddawania moczu , zatrzymanie moczu i utrata kontroli stolca .
Nawet po leczeniu umiera około 10% osób zarażonych tężcem. Śmiertelność jest wyższa u nieszczepionych osób oraz osób powyżej 60 roku życia.
Okres wylęgania
Okres inkubacji tężca może trwać do kilku miesięcy, ale zwykle wynosi około dziesięciu dni. Ogólnie rzecz biorąc, im dalej miejsce urazu od ośrodkowego układu nerwowego , tym dłuższy jest okres inkubacji. Im krótszy okres inkubacji, tym ostrzejsze objawy. W trismus nascentium (tj. tężec noworodkowy) objawy pojawiają się zwykle od 4 do 14 dni po urodzeniu, średnio około 7 dni. Na podstawie wyników badań klinicznych opisano cztery różne formy tężca.
Uogólniony tężec
Tężec uogólniony to najczęstszy typ tężca, stanowiący około 80% przypadków. Forma uogólniona zwykle przedstawia się w formie zstępującej. Pierwszym objawem jest szczękościsk lub skurcze twarzy zwane risus sardonicus , po których następuje sztywność karku, trudności w połykaniu oraz sztywność mięśni piersiowych i łydek . Inne objawy to podwyższona temperatura, pocenie się, podwyższone ciśnienie krwi i epizodyczne przyspieszone tętno. Skurcze mogą występować często i trwać kilka minut z ciałem ukształtowanym w charakterystyczną formę zwaną opistotonos . Skurcze trwają do czterech tygodni, a całkowite wyzdrowienie może zająć miesiące.
Tężec noworodkowy
Tężec noworodkowy ( trismus nascentium ) jest formą uogólnionego tężca, która występuje u noworodków, zwykle urodzonych przez matki, które same nie zostały zaszczepione. Jeśli matka została zaszczepiona przeciwko tężcowi, niemowlęta uzyskują odporność bierną i dzięki temu są chronione. Zwykle następuje poprzez infekcję niezagojonego kikuta pępowinowego, szczególnie gdy kikut jest przecinany niesterylnym narzędziem. W 1998 r. tężec noworodkowy był powszechny w wielu krajach rozwijających się i był odpowiedzialny za około 14% (215 000) wszystkich zgonów noworodków. W 2010 roku liczba zgonów na całym świecie wyniosła 58 000 noworodków. W wyniku kampanii zdrowia publicznego liczba zgonów z powodu tężca noworodków została zmniejszona o 90% w latach 1990-2010, a do 2013 r. choroba została w dużej mierze wyeliminowana we wszystkich krajach poza 25. Tężec noworodkowy występuje rzadko w krajach rozwiniętych.
Lokalny tężec
Miejscowy tężec jest rzadką postacią choroby, w której ludzie mają uporczywe skurcze mięśni w tym samym obszarze anatomicznym co uraz. Skurcze mogą utrzymywać się przez wiele tygodni, po czym stopniowo ustępują. Miejscowy tężec jest na ogół łagodniejszy; tylko około 1% przypadków kończy się śmiercią, ale może poprzedzać wystąpienie tężca uogólnionego.
Tężec głowowy
Tężec głowowy jest najrzadszą postacią choroby (0,9–3% przypadków) i ogranicza się do mięśni i nerwów głowy. Zwykle występuje po urazie okolicy głowy, w tym złamaniu czaszki , skaleczeniu, uszkodzeniu oka, usunięciu zębów i zapaleniu ucha środkowego , ale obserwowano go w przypadku urazów innych części ciała. Najczęściej w grę wchodzi paraliż nerwu twarzowego , który może powodować szczękościsk, porażenie twarzy lub opadanie powieki , ale może to również dotyczyć innych nerwów czaszkowych. Tężec głowowy może przejść do bardziej uogólnionej postaci choroby. Ze względu na rzadkość występowania tej choroby lekarze mogą nie znać obrazu klinicznego i nie podejrzewać tężca jako choroby. Leczenie może być skomplikowane, ponieważ objawy mogą współistnieć z początkowym urazem, który spowodował infekcję. Tężec głowowy jest bardziej prawdopodobny niż inne postacie tężca, które są śmiertelne, a progresja do tężca uogólnionego prowadzi do śmiertelności 15-30% przypadków.
Przyczyna

Tężec jest wywoływany przez bakterię tężca Clostridium tetani . Tężec jest międzynarodowym problemem zdrowotnym, ponieważ endospory C. tetani są wszechobecne. Endospory mogą zostać wprowadzone do organizmu przez ranę kłującą ( uraz penetrujący ). Ponieważ C. tetani jest bakterią beztlenową, ona i jej przetrwalniki rozwijają się w środowiskach pozbawionych tlenu , takich jak rana kłuta. Wraz ze zmianami poziomu tlenu endospory w kształcie pałeczek bębna mogą powodować szybkie rozprzestrzenianie się.
Choroba występuje prawie wyłącznie u osób niedostatecznie uodpornionych. Występuje częściej w gorącym, wilgotnym klimacie z glebą bogatą w materię organiczną. Nawóz -treated gleby może zawierać zarodniki, ponieważ są one powszechnie w jelitach i kału wielu zwierząt, takich jak konie, bydło, owce, psy, koty, szczury, świnki morskie i kurcząt. Na terenach rolniczych organizm może być schronieniem dla znacznej liczby dorosłych ludzi.
Zarodniki można również znaleźć na powierzchni skóry iw skażonej heroinie . Osoby używające heroiny, zwłaszcza te, które wstrzykują narkotyk podskórnie, wydają się być narażone na wysokie ryzyko zachorowania na tężec. Rzadko tężec może zostać zarażony przez zabiegi chirurgiczne, zastrzyki domięśniowe, złożone złamania i infekcje zębów. Ukąszenia zwierząt mogą przenosić tężec.
Tężec często kojarzy się z rdzą , zwłaszcza zardzewiałymi paznokciami. Chociaż sama rdza nie powoduje tężca, przedmioty, które gromadzą rdzę, często znajdują się na zewnątrz lub w miejscach, w których znajdują się bakterie beztlenowe. Dodatkowo, szorstka powierzchnia zardzewiałego metalu tworzy szczeliny dla brudu zawierającego C. tetani , podczas gdy gwóźdź umożliwia nakłucie skóry i dostarczanie przetrwalników w głąb ciała w miejscu rany. Endospora to niemetabolizująca struktura przetrwania, która zaczyna metabolizować i powodować infekcję w odpowiednim środowisku. Stąd nadepnięcie na paznokieć (zardzewiały lub nie) może spowodować zakażenie tężcem, ponieważ pod skórą może istnieć środowisko o niskiej zawartości tlenu (beztlenowe), a nakłuwany przedmiot może dostarczyć endospory do odpowiedniego środowiska do wzrostu. Powszechnym błędem jest przekonanie, że przyczyną jest sama rdza, a przebicie gwoździem wolnym od rdzy nie stanowi ryzyka.
Patofizjologia
Neurotoksyna tężcowa (TeNT) wiąże się z błoną presynaptyczną połączenia nerwowo-mięśniowego , ulega internalizacji i jest transportowana z powrotem przez akson aż do ośrodkowego układu nerwowego . Tutaj selektywnie wiąże się i jest transportowany do hamujących neuronów poprzez endocytozę . Następnie opuszcza pęcherzyk dla cytozolu neuronu, gdzie rozszczepia synaptobrewinę białka błonowego związanego z pęcherzykami (VAMP) , która jest niezbędna do fuzji błonowej małych pęcherzyków synaptycznych (SSV). SSV przenoszą neuroprzekaźnik do błony w celu uwolnienia, więc hamowanie tego procesu blokuje uwalnianie neuroprzekaźników.
Toksyna tężca specyficznie blokuje uwalnianie neuroprzekaźników GABA i glicyny z neuronów hamujących. Te neuroprzekaźniki zapobiegają aktywacji nadaktywnych neuronów ruchowych, a także odgrywają rolę w rozluźnieniu mięśni po skurczu. Kiedy neurony hamujące nie są w stanie uwolnić swoich neuroprzekaźników, neurony ruchowe wymykają się spod kontroli, a mięśnie mają trudności z rozluźnieniem. Powoduje to skurcze mięśni i paraliż spastyczny obserwowany przy zakażeniu tężcem.
Toksyna tężcowa , tetanospasmina , składa się z łańcucha ciężkiego i łańcucha lekkiego. Istnieją trzy domeny, z których każda przyczynia się do patofizjologii toksyny. Łańcuch ciężki ma dwie domeny. Strona N-końcowa łańcucha ciężkiego pomaga w translokacji błony, a strona C-końcowa pomaga toksynie zlokalizować określone miejsce receptora na prawidłowym neuronie. Domena łańcucha lekkiego przecina białko VAMP po dotarciu do hamującego cytozolu neuronu.
Istnieją cztery główne etapy mechanizmu działania tężca: wiązanie z neuronem, internalizacja toksyny, translokacja błony i rozszczepienie docelowego VAMP.
Wiązanie neurospecyficzne
Toksyna przemieszcza się z miejsca rany dla nerwowo-mięśniowej węzła w krwiobiegu, gdzie wiąże się z błoną presynaptyczną z neuronu ruchowego . Domena C-końcowa łańcucha ciężkiego pomaga w wiązaniu się z właściwym miejscem, rozpoznawaniu i wiązaniu odpowiednich glikoprotein i glikolipidów w błonie presynaptycznej. Toksyna wiąże się z miejscem, które zostanie przeniesione do neuronu jako pęcherzyk endocytarny, który będzie podróżował wzdłuż aksonu, przez ciało komórki i przez dendryty do końcówki dendrytycznej w kręgosłupie i ośrodkowym układzie nerwowym. Tutaj zostanie uwolniony do szczeliny synaptycznej i będzie mógł związać się z błoną presynaptyczną neuronów hamujących w podobny sposób, jak w przypadku wiązania z neuronem ruchowym.
Internalizacja
Toksyna tężcowa jest następnie ponownie internalizowana poprzez endocytozę , tym razem w kwaśnym pęcherzyku. W mechanizmie, który nie jest dobrze poznany, depolaryzacja spowodowana odpaleniem neuronu hamującego powoduje, że toksyna jest wciągana do neuronu wewnątrz pęcherzyków.
Translokacja błony
Następnie toksyna potrzebuje sposobu na wydostanie się z pęcherzyka do cytozolu neuronu, aby mogła działać na swój cel. Niskie pH światła pęcherzyka powoduje zmianę konformacyjną toksyny, przesuwając ją z postaci rozpuszczalnej w wodzie do postaci hydrofobowej . Po odsłonięciu hydrofobowych łat toksyna może przedostać się do błony pęcherzyka. Toksyna tworzy w błonie kanał jonowy niespecyficzny dla jonów Na + , K + , Ca 2+ i Cl − . Wśród ekspertów panuje zgoda, że ten nowy kanał jest zaangażowany w translokację łańcucha lekkiego toksyny z wnętrza pęcherzyka do cytozolu neuronu, ale mechanizm nie jest dobrze poznany ani uzgodniony. Zaproponowano, że kanał może umożliwić lekkiemu łańcuchowi (rozwiniętemu ze środowiska o niskim pH) opuszczenie przez pory toksyny lub że pory mogą wystarczająco zmienić gradient elektrochemiczny , wpuszczając lub wypuszczając jony, aby spowodować osmotyczną lizę pęcherzyk, rozlewając zawartość pęcherzyka.
Enzymatyczne rozszczepienie celu
Lekki łańcuch toksyny tężcowej to proteaza zależna od cynku . Ma wspólny motyw proteazy cynkowej (His-Glu-Xaa-Xaa-His), który według naukowców był niezbędny do cięcia docelowego, dopóki nie zostało to niedawno potwierdzone eksperymentalnie: kiedy cały cynk został usunięty z neuronu za pomocą chelatorów metali ciężkich , toksyna była hamowana jedynie być aktywowane gdy cynk dodano do wnętrza. lekkie wiąże łańcuch na VAMP i łączy się go między Gin 76 i Phe 77 . Bez VAMP pęcherzyki zawierające neuroprzekaźniki potrzebne do regulacji neuronów ruchowych ( GABA i glicyna) nie mogą zostać uwolnione, powodując wspomnianą powyżej deregulację neuronów ruchowych i napięcie mięśni.
Diagnoza
Obecnie nie ma badań krwi do diagnozowania tężca. Rozpoznanie opiera się na wystąpieniu objawów tężca i nie zależy od wyizolowania bakterii, która tylko w 30% przypadków jest wydzielona z rany i może być wyizolowana od osób bez tężca. Identyfikację laboratoryjną C. tetani można wykazać jedynie na podstawie produkcji tetanospasminy u myszy. Niedawny uraz głowy może wskazywać na tężec głowy, jeśli nie postawiono innej diagnozy.
„Test łopatkowy” to test kliniczny na tężec, który polega na dotknięciu tylnej ściany gardła narzędziem z miękką końcówką i obserwowaniu efektu. Pozytywny wynik testu to mimowolny skurcz szczęki (przygryzanie „łopatki”), a negatywny wynik testu to zwykle odruch wymiotny przy próbie wypchnięcia ciała obcego. Krótki raport w The American Journal of Tropical Medicine and Hygiene stwierdza, że w badaniu z udziałem osób dotkniętych chorobą, test szpatułkowy miał wysoką swoistość (zero wyników fałszywie dodatnich) i wysoką czułość (94% zakażonych osób dało wynik pozytywny). test).
Zapobieganie
W przeciwieństwie do wielu chorób zakaźnych, wyzdrowienie z naturalnie nabytego tężca zwykle nie skutkuje odpornością na tężec. Wynika to z ekstremalnej siły działania toksyny tetanospasminy. Tetanospasmina będzie prawdopodobnie śmiertelna, zanim wywoła odpowiedź immunologiczną.
Tężec może być uniemożliwione przez szczepienie z tężcowa . CDC zaleca, aby osoby dorosłe otrzymać przypominającą szczepionki raz na dziesięć lat, a standardową praktyką opieki w wielu miejscach jest zapewnienie dodatkowego, aby każda osoba z raną nakłucia, który jest niepewny, gdy on lub ona był ostatnio szczepiona, czy on lub ona ma otrzymał mniej niż trzy dawki szczepionki w całym okresie życia. Wspomaganie może jednak nie zapobiec potencjalnie śmiertelnemu przypadkowi tężca z obecnej rany, ponieważ może upłynąć do dwóch tygodni, zanim wytworzą się przeciwciała przeciw tężcowi.
U dzieci poniżej siódmego roku życia szczepionka przeciw tężcowi jest często podawana jako szczepionka skojarzona, szczepionka DPT/DTaP , która obejmuje również szczepionki przeciwko błonicy i krztuścowi . W przypadku dorosłych i dzieci powyżej siedmiu lat powszechnie stosuje się szczepionkę Td (tężec i błonica) lub Tdap (tężec, błonica i krztusiec bezkomórkowy).
Światowa Organizacja Zdrowia potwierdza kraje jak po wyeliminowaniu matczynych lub tężec noworodków . Certyfikacja wymaga co najmniej dwóch lat wskaźników poniżej 1 przypadku na 1000 żywych urodzeń. W 1998 roku w Ugandzie zarejestrowano 3433 przypadki tężca u noworodków; z nich 2403 zmarło. Po poważnych wysiłkach w zakresie zdrowia publicznego Uganda w 2011 roku uzyskała certyfikat wyeliminowania tężca.
Profilaktyka poekspozycyjna
Toksoid tężcowy można podać w przypadku podejrzenia narażenia na tężec. W takich przypadkach można go podawać z immunoglobuliną tężcową lub bez immunoglobuliny (zwanej również przeciwciałami przeciw tężcowi lub antytoksyną tężcową ). Może być podawany w terapii dożylnej lub poprzez wstrzyknięcie domięśniowe .
Wytyczne dotyczące takich wydarzeń w Stanach Zjednoczonych dla osób niebędących w ciąży w wieku 11 lat i starszych są następujące:
| Status szczepień | Czyste, drobne rany | Wszystkie inne rany |
|---|---|---|
| Nieznana lub mniej niż 3 dawki szczepionki zawierającej toksoid tężcowy | Tdap i polecam szczepienia uzupełniające |
Tdap i zaleca szczepienie uzupełniające Immunoglobulina przeciwtężcowa |
| 3 lub więcej dawek szczepionki zawierającej toksoid tężcowy ORAZ mniej niż 5 lat od ostatniej dawki | Brak wskazania | Brak wskazania |
| 3 lub więcej dawek szczepionki zawierającej toksoid tężcowy ORAZ 5–10 lat od ostatniej dawki | Brak wskazania | Preferowane Tdap (jeśli jeszcze nie otrzymano) lub Td |
| 3 lub więcej dawek szczepionki zawierającej toksoid tężcowy ORAZ ponad 10 lat od ostatniej dawki | Preferowane Tdap (jeśli jeszcze nie otrzymano) lub Td | Preferowane Tdap (jeśli jeszcze nie otrzymano) lub Td |
Leczenie
Łagodny tężec
Łagodne przypadki tężca można leczyć za pomocą:
- Immunoglobulina tężcowa (TIG), zwana także przeciwciałami przeciw tężcowi lub antytoksyną tężcową. Może być podawany w terapii dożylnej lub poprzez wstrzyknięcie domięśniowe .
- Terapia antybiotykowa w celu zmniejszenia produkcji toksyn. Korzystnym leczeniem jest metronidazol dożylnie (IV).
- Benzodiazepiny mogą być stosowane do kontrolowania skurczów mięśni. Opcje obejmują diazepam i lorazepam , doustnie lub dożylnie.
Ciężki tężec
Ciężkie przypadki będą wymagały przyjęcia na intensywną terapię . Oprócz środków wymienionych powyżej w przypadku łagodnego tężca:
- Ludzka immunoglobulina przeciwtężcowa wstrzykiwana dooponowo (co zwiększa kliniczną poprawę z 4% do 35%)
- Tracheotomia i wentylacja mechaniczna przez 3 do 4 tygodni. Tracheotomia jest zalecana w celu zabezpieczenia dróg oddechowych, ponieważ obecność rurki dotchawiczej jest bodźcem do skurczu
- Siarczan magnezu w postaci wlewu dożylnego w celu opanowania skurczów i dysfunkcji autonomicznych
- Diazepam jako ciągły wlew dożylny
- W autonomicznych efektów tężca może być trudne do przeprowadzenia (przemiennego hiper- i niedociśnienie gorączka / hipotermia ) i mogą wymagać IV labetalol , magnez, klonidyna , lub nifedypina
W celu opanowania skurczów mięśni można podawać leki takie jak diazepam lub inne środki zwiotczające mięśnie. W skrajnych przypadkach może być konieczne, aby sparaliżować osoby z kurary leków -jak i użycie mechanicznego respiratora.
Aby przeżyć infekcję tężcową, konieczne jest utrzymanie dróg oddechowych i odpowiednie odżywianie . Spożycie 3500 do 4000 kalorii i co najmniej 150 g białka dziennie jest często podawane w postaci płynnej przez rurkę bezpośrednio do żołądka ( przezskórna endoskopowa gastrostomia ) lub przez kroplówkę ( żywienie pozajelitowe ). Ta wysokokaloryczna dieta jest wymagana ze względu na zwiększone obciążenie metaboliczne spowodowane zwiększoną aktywnością mięśni. Pełna regeneracja trwa od 4 do 6 tygodni, ponieważ organizm musi zregenerować zniszczone zakończenia aksonów nerwowych .
Antybiotykiem z wyboru jest metronidazol . Może być podawany dożylnie, doustnie lub doodbytniczo. Równie skuteczna jest penicylina , ale niektórzy obawiają się wywołania skurczów, ponieważ hamuje ona receptor GABA , na który już wpływa tetanospazmina.
Epidemiologia
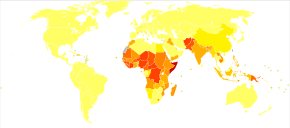
W 2013 r. spowodował około 59 000 zgonów – w porównaniu z 356 000 w 1990 r. Tężec – w szczególności forma noworodkowa – pozostaje poważnym problemem zdrowia publicznego w krajach nieuprzemysłowionych, a 59 000 noworodków na całym świecie zmarło w 2008 r. w wyniku tężca noworodkowego. W Stanach Zjednoczonych od 2000 do 2007 roku zgłaszano średnio 31 przypadków rocznie. Prawie wszystkie przypadki w Stanach Zjednoczonych występują u osób nieimmunizowanych lub osób, które pozwoliły na wygaśnięcie ich szczepień .
Historia
Tężec był dobrze znany starożytnym społecznościom i cywilizacjom, które rozpoznały związek między ranami a śmiertelnymi skurczami mięśni. W 1884 roku Arthur Nicolaier wyizolował przypominającą strychninę toksynę tężca z wolno żyjących, beztlenowych bakterii glebowych. Etiologia choroby została dokładniej wyjaśniona w 1884 roku przez Antonio Carle i Giorgio Rattone , dwóch patologów z Uniwersytetu Turyńskiego , którzy po raz pierwszy wykazali przenośność tężca. Wytwarzali tężec u królików, wstrzykując ropę od osoby ze śmiertelnym tężcem do nerwów kulszowych i testując ich reakcje podczas rozprzestrzeniania się tężca.
W 1891 roku Kitasato Shibasaburō wyizolował C. tetani z ludzkiej ofiary , który później wykazał, że organizm może wywołać chorobę po wstrzyknięciu zwierzętom, a toksynę można zneutralizować przez specyficzne przeciwciała . W 1897 r. Edmond Nocard wykazał, że antytoksyna tężcowa wywołuje u ludzi odporność bierną i może być stosowana w profilaktyce i leczeniu. Szczepionka na toksoid tężcowy została opracowana przez P. Descombey w 1924 roku i była szeroko stosowana w zapobieganiu tężcowi wywołanemu przez rany bojowe podczas II wojny światowej .
Etymologia
Słowo tężec pochodzi od starogreckiego : τέτανος , Romanized : tężcowi , oświetlony 'napięty', co jest dalsze od starożytnej greki : τείνειν , latynizowane : teinein , lit. 'rozciągać'.
Badania
Nie ma wystarczających dowodów, aby zalecać leczenie lub zapobieganie tężcowi witaminą C.
Zobacz też
Bibliografia
Zewnętrzne linki
- Informacje o tężcu od Medline Plus
- Nadzór nad tężcem -- Stany Zjednoczone, 1998-2000 (dane i analiza)
- "Tężec" . MedlinePlus . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
| Klasyfikacja | |
|---|---|
| Zasoby zewnętrzne |




