Arsfenamina - Arsphenamine
Arsfenamina , znana również jako salwarsan lub związek 606 , jest lekiem wprowadzonym na początku lat 1910 jako pierwsza skuteczna metoda leczenia kiły i trypanosomatozy afrykańskiej . Ten związek arsenoorganiczny był pierwszym nowoczesnym środkiem przeciwdrobnoustrojowym .
Historia
Arsfenamina została po raz pierwszy zsyntetyzowana w 1907 roku w laboratorium Paula Ehrlicha przez Alfreda Bertheima . Działanie antysyfilityczne tego związku odkrył Sahachiro Hata w 1909 roku, podczas badania setek nowo zsyntetyzowanych organicznych związków arsenu . Ehrlich wysunął teorię, że poprzez badanie przesiewowe wielu związków można odkryć lek, który miałby działanie przeciwdrobnoustrojowe, ale nie zabijałby ludzkiego pacjenta. Zespół Ehrlicha rozpoczął poszukiwania takiej „ magicznej kuli ” wśród chemicznych pochodnych niebezpiecznie toksycznego leku atoksyl . Ten projekt był pierwszym wysiłku zorganizowany zespół, aby zoptymalizować aktywność biologiczną o związkiem ołowiu dzięki systematycznym modyfikacjom chemicznym, podstawą prawie wszystkich nowoczesnych badań farmaceutycznych.
Arsfenamina była stosowana w leczeniu kiły, ponieważ jest toksyczna dla bakterii Treponema pallidum , krętka wywołującego kiłę.
Arsfenamina była pierwotnie nazywana „606”, ponieważ była szóstą w szóstej grupie związków zsyntetyzowanych do testów; został wprowadzony do obrotu przez Hoechst AG pod nazwą handlową „Salvarsan” w 1910 roku. Salvarsan był pierwszym organicznym środkiem antysyfilitycznym i stanowił znaczne ulepszenie w stosunku do wcześniej stosowanych nieorganicznych związków rtęci . Był rozprowadzany w postaci żółtego, krystalicznego, higroskopijnego proszku, który był bardzo niestabilny w powietrzu. To znacznie skomplikowało podawanie, ponieważ lek trzeba było rozpuścić w kilkuset mililitrach destylowanej, sterylnej wody przy minimalnej ekspozycji na powietrze, aby wytworzyć roztwór odpowiedni do wstrzyknięcia. Uważano, że niektóre z działań niepożądanych przypisywanych Salvarsanowi, w tym wysypki, uszkodzenie wątroby oraz zagrożenie życia i kończyn, były spowodowane niewłaściwym obchodzeniem się i podawaniem. To spowodowało, że Ehrlich, który wytrwale pracował nad standaryzacją praktyk, zauważył, że „krok z laboratorium do łóżka pacjenta… jest niezwykle żmudny i pełen niebezpieczeństw”.
Laboratorium Ehrlicha opracowało bardziej rozpuszczalny (ale nieco mniej skuteczny) związek arsenu, Neosalvarsan (neoarsfenamina), który był łatwiejszy do przygotowania i stał się dostępny w 1912 roku. Mniej poważne skutki uboczne, takie jak nudności i wymioty, były nadal powszechne. Dodatkowym problemem było to, że zarówno Salvarsan, jak i Neosalvarsan musiały być przechowywane w zamkniętych fiolkach w atmosferze azotu, aby zapobiec utlenianiu. Te związki arsenu zostały zastąpione w leczeniu kiły w latach czterdziestych przez penicylinę .
Po opuszczeniu laboratorium Ehrlicha Hata kontynuowała równoległe badania nowych leków w Japonii .
Struktura
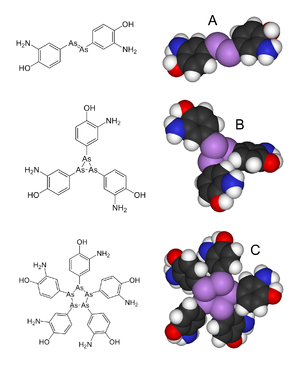
Od dawna zakładano, że salwarsan ma podwójne wiązanie As=As , podobne do wiązania N=N w azobenzenie . Jednak w 2005 roku w obszernej analizie spektrometrii masowej prowadzonej przez profesora Briana Nicholsona z Uniwersytetu Waikato wykazano, że wiązania arsenowo-arsenowe w Salvarsan są wiązaniami pojedynczymi, a nie podwójnymi. Przypuszczalnie składa się z cząsteczek RAs=AsR, tj. ( RAs ) 2 , Salvarsan faktycznie zawiera mieszaninę cyklo-(RAs) 3 i cyklo-(RAs) 5 , gdzie R oznacza 3-amino-4-hydroksyfenyl ugrupowanie . Według Nicholsona, te cykliczne gatunki powoli uwalniają utlenione związki, RAs (OH) 2 , które są prawdopodobnie odpowiedzialne za właściwości przeciwkiłowe salvarsanu.
Zobacz też
- Magic Bullet Dr. Ehrlicha , film z 1940 roku o dążeniu Ehrlicha do znalezienia lekarstwa na syfilis.

