Opiaty - Opiate
Opiatów w klasycznej farmakologii jest substancja pochodząca z opium . We współczesnym użyciu termin opioid jest używany do określenia wszystkich substancji, zarówno naturalnych, jak i syntetycznych, które wiążą się z receptorami opioidowymi w mózgu (w tym antagonistami). Opioidy są alkaloidy związki naturalnie w mak roślin Papaver somniferum . Związki psychoaktywne występujące w opium obejmują morfinę , kodeinę i tebainę . Opiaty były od dawna używane w różnych schorzeniach, a dowody na handel opiatami i stosowanie do łagodzenia bólu już w VIII wieku naszej ery. Opiaty są uważane za leki o umiarkowanym lub wysokim potencjale nadużywania i są wymienione w różnych „Harmonogramach kontroli substancji” zgodnie z Jednolitą Ustawą o Substancjach Kontrolowanych Stanów Zjednoczonych Ameryki.
W 2014 roku od 13 do 20 milionów ludzi używało opiatów rekreacyjnie (0,3% do 0,4% światowej populacji w wieku od 15 do 65 lat). Według CDC w tej populacji odnotowano 47 000 zgonów, w sumie pół miliona zgonów w latach 2000–2014. W 2016 roku Światowa Organizacja Zdrowia poinformowała, że 27 milionów ludzi cierpi na nadużywanie opioidów. Poinformowali również, że w 2015 r. 450 000 osób zmarło w wyniku zażywania narkotyków, z czego od jednej trzeciej do połowy tej liczby przypisano opioidom.
Przegląd
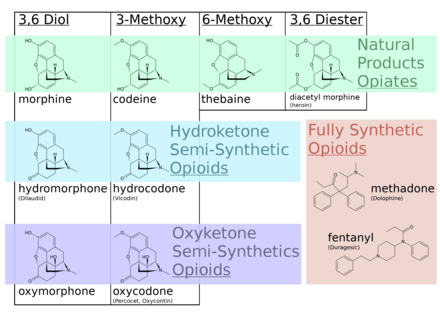
Opiaty należą do dużej biosyntetycznej grupy alkaloidów benzyloizochinolinowych i są tak nazwane, ponieważ są naturalnie występującymi alkaloidami występującymi w maku lekarskim. Główne psychoaktywne opiaty to morfina , kodeina i tebaina . Papaweryna , noskapina i około 24 inne alkaloidy są również obecne w opium , ale mają niewielki lub żaden wpływ na ośrodkowy układ nerwowy człowieka . Alkaloidy, które nie mają wpływu na centralny układ nerwowy, nie są uważane za opiaty. Bardzo małe ilości hydrokodonu i hydromorfonu są rzadko wykrywane w testach opium; wydaje się, że jest wytwarzany przez roślinę w okolicznościach i w procesach, które nie są obecnie rozumiane i mogą obejmować działanie bakterii. Dihydrokodeina , oksymorfol , oksykodon , oksymorfon , metopon i prawdopodobnie inne pochodne morfiny i/lub hydromorfonu również występują w śladowych ilościach w opium.
Pomimo tego, że morfina jest najbardziej znaczącym medycznie opiatem, większe ilości kodeiny są spożywane medycznie, w większości syntetyzowana z morfiny. Kodeina ma większą i bardziej przewidywalną biodostępność po podaniu doustnym, co ułatwia miareczkowanie dawki. Kodeina ma również mniejszy potencjał nadużywania niż morfina, a ponieważ jest łagodniejsza, wymagane są większe dawki kodeiny.
Efekty zespołu odstawienia opiatów są związane z nagłym zaprzestaniem lub ograniczeniem długotrwałego używania opiatów.
Manifestacja uzależnienia i nadużywania opiatów zależy od wielu czynników, w tym właściwości farmakokinetycznych opiatów i predyspozycji użytkownika do uzależnienia.
Synteza
Chociaż możliwa jest pełna synteza opioidów z naftochinonu (synteza Gatesa) lub innych prostych organicznych materiałów wyjściowych, są to procesy żmudne i nieekonomiczne. Dlatego większość stosowanych obecnie środków przeciwbólowych typu opiatów jest albo ekstrahowana z Papaver somniferum, albo syntetyzowana z tych opiatów, zwłaszcza tebainy .
W 2015 roku badania zgłoszone udanej biosyntezy z tebainy i hydrokodonu przy użyciu genetycznie zmodyfikowanych drożdży . Po przeskalowaniu do użytku komercyjnego proces ten skróciłby czas produkcji z roku do kilku dni i mógłby obniżyć koszty o 90%.
Farmakokinetyka
Kodeina
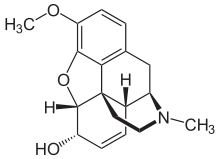
Kodeina jest prolekiem, który przekształca się w morfinę i działa na receptory μ- opiatowe. Jest przekształcany do morfiny poprzez metabolizm enzymów CYP2D6. Osoby, które mają niższą aktywność CYP2D6, mogą nie metabolizować kodeiny wystarczająco skutecznie, aby odczuć jej działanie przeciwbólowe. Odwrotnie, osoby z wyższą aktywnością CYP2D6 mogą zbyt szybko metabolizować lek i doświadczać skutków ubocznych związanych z dawką, takich jak uspokojenie polekowe i depresja oddechowa.
Fentanyl
Fentanyl jest syntetycznym opioidem strukturalnie podobnym do arylopiperydyn. Jest silnym agonistą receptora μ-r, który jest 80–100 razy silniejszy niż morfina i ma szybki początek z krótszym czasem działania niż morfina. Jest metabolizowany w wątrobie przez enzymy CYP3A4 do związku norfentanyl.
Heroina
| Substancja | Najlepsze oszacowanie |
Niskie oszacowanie |
Wysoka ocena |
|---|---|---|---|
| Stymulanty typu amfetaminy |
34,16 | 13.42 | 55,24 |
| Konopie indyjskie | 192.15 | 165,76 | 234,06 |
| Kokaina | 18.20 | 13.87 | 22.85 |
| Ekstaza | 20,57 | 8.99 | 32,34 |
| Opiaty | 19.38 | 13.80 | 26.15 |
| Opioidy | 34,26 | 27.01 | 44,54 |
Heroina, nazwa handlowa diacetylomorfiny, jest pierwszym z kilku półsyntetycznych opioidów otrzymywanych z morfiny, składnika naturalnego opium. Chociaż pochodzi z naturalnego opium, a nie bezpośrednio w nim, jest powszechnie określany jako opiat. Heroina (diacetylomorfina) jest prolekiem morfiny ; po podaniu jest metabolizowany przez wątrobę do morfiny. Jeden z głównych metabolitów heroiny, 6-monoacetylomorfina (6-MAM), jest również prolekiem morfiny.
hydromorfon
Hydromorfon jest stosowany jako alternatywa dla morfiny. Ma wysoki metabolizm pierwszego przejścia i jest głównie glukuronidowany w wątrobie do hydromorfonu-3-glukoronidu (H3G). 75% hydromorfonu jest wydalane przez nerki, a 7% jako opiat macierzysty.
Meperydyna
Meperydyna to syntetyczne opiaty należące do klasy arylopiperydyn. Jest silnym agonistą receptora μ-r z 1/10 siły działania morfiny. Jest stosowany w leczeniu rygorów i ma okres półtrwania od trzech do czterech godzin. Jest metabolizowany w wątrobie do aktywnych metabolitów normeperydyny, kwasu normepirydynowego i kwasu medperydynowego. Normeperydyna w stężeniach toksycznych może powodować pobudzenie ośrodkowego układu nerwowego i drgawki.
Metadon
Metadon ma wyższą biodostępność i okres półtrwania w porównaniu z morfiną. Jest metabolizowany do nieaktywnego produktu przez N-demetylację przez enzymy CYP3A4 w wątrobie. Charakteryzuje się dużą zmiennością między poszczególnymi osobami ze względu na różne poziomy CYP3A4 u poszczególnych osób. Jest zatwierdzony do leczenia bólu o nasileniu od umiarkowanego do silnego oraz uzależnienia od opioidów. Ze względu na wysokie ryzyko interakcji lekowych, toksyczne działanie na wątrobę i zmienność pacjentów, pacjenci muszą być ściśle monitorowani w klinikach metadonowych .
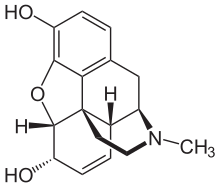
Morfina
Nikomorfina (morfina dinikotynian) dipropanoylmorphine (morfina dipropionian), dezomorfinę (di-hydro-dezoksy-morfina), metylodezorfina , acetylpropionylmorphine , dibenzoylmorphine , diacetyldihydromorphine i kilka innych są także pochodzić od morfiny.
Morfina jest metabolizowana w wątrobie do morfino-3-glukuronidu (M3G) i morfino-6-glukuronidu (M6G) i jest wydalana przez nerki. Są również w stanie przedostać się przez barierę krew-mózg do płynu mózgowo-rdzeniowego. M6G ma silne działanie przeciwbólowe, wiąże się z receptorami opioidowymi i jest głównym czynnikiem wpływającym na terapeutyczne korzyści morfiny. M3G nie działa jako środek przeciwbólowy, ma niskie powinowactwo do receptorów opioidowych i może antagonizować terapeutyczne działanie morfiny i M6G. Co więcej, wysokie dawki morfiny, a tym samym M3G, są związane z neurotoksycznymi skutkami ubocznymi, takimi jak przeczulica bólowa , allodynia i mioklonie .
Oksymorfon
Oksymorfon jest kongenerem morfiny. Jest metabolizowany do 6-hydroksy-oksymorfonu i oksymorfonu-3-glukuronidu, a 40% jest wydalane w postaci metabolitów. 6-hydroksy-oksymorfina jest aktywna i występuje w stosunku 1:1 z lekiem macierzystym. Aktywność oksymorfonu-3-glukuronidu jest nieznana.
Wskazanie
Opiaty stosuje się głównie w leczeniu bólu z założeniem, że korzyści zarówno dla bólu, jak i funkcji przewyższą ryzyko dla pacjenta. Innym wskazaniem jest objawowe łagodzenie duszności , zarówno w stanach ostrych (np. obrzęk płuc ), jak i u pacjentów w stanie terminalnym.
Zmiana dawki opiatów może być konieczna przy zmianie leków ze względu na różne właściwości farmakodynamiczne opiatów. Ogólnie rzecz biorąc, morfina jest używana jako standard do zamiany opiatów w celu uzyskania równoważnych efektów przeciwbólowych. Te różnice w ekwiwalentach morfiny mogą różnić się między preparatami tego samego leku. Obliczenie całkowitej dawki dobowej na podstawie ekwiwalentów morfiny w miligramach służy do identyfikacji pacjentów zagrożonych przedawkowaniem.
Powikłania i skutki uboczne
Częste działania niepożądane związane ze stosowaniem opioidów obejmują: uspokojenie , nudności , zawroty głowy, wymioty, zaparcia , uzależnienie fizyczne, tolerancję i depresję oddechową . Spośród nich najczęstsze to zaparcia i nudności i nie ma rozwoju tolerancji na te skutki uboczne. Z tego powodu z opioidami często przepisuje się środki zmiękczające stolec lub środki przeczyszczające (glikol polietylenowy, dokuzan i senes).
Mniej powszechne działania niepożądane obejmują: opóźnione opróżnianie żołądka, hiperalgezję , dysfunkcję immunologiczną i hormonalną, sztywność mięśni i mioklonie .
Stosowanie opiatów w leczeniu bólu jest powszechnie akceptowane w systemie opieki zdrowotnej. Jednak długotrwałe leczenie bólu przewlekłego jest bardzo kontrowersyjne, ponieważ istnieje wysokie ryzyko uzależnienia związanego z jego stosowaniem, co prowadzi do nadużyć i odwracania uwagi innych, nawet jeśli jest właściwie przyjmowane. Osoby uzależnione od opiatów będą stawiać nabycie tych leków przed innymi czynnościami w ich życiu, co negatywnie wpłynie na ich relacje zawodowe i osobiste.
Przewlekłe stosowanie opioidów może prowadzić do tolerancji . To często powoduje, że pacjent potrzebuje wyższych i/lub częstszych dawek leku, aby uzyskać pożądane efekty.
Działania niepożądane zależne od stężenia mogą się różnić w zależności od polimorfizmu genetycznego użytkownika, który może zmienić metabolizm leku. Cytochrom P450 (w szczególności CYP2D6 ) jest odpowiedzialny za metabolizm różnych opiatów do aktywnych metabolitów, a zmiany aktywności CYP450 prowadzą do różnych poziomów leku w surowicy.
Farmakologia w bólu
Ból to nieprzyjemne doświadczenie sensoryczne i emocjonalne związane z rzeczywistym lub potencjalnym uszkodzeniem tkanki. Jest to niezbędna funkcja obronna, w której ból działa jak alarm, aby uniknąć lub ograniczyć uszkodzenie tkanki. Opiaty działają na receptory opioidowe, które są sprzężone z receptorami sprzężonymi z białkiem G (GPCR). Receptory te dzielą się na 3 klasy: receptory μ (mu) , δ (delta) i κ (kappa) .
Ponad 70% receptorów opioidowych to receptory μ, zlokalizowane głównie w centralnych zakończeniach nocyceptorów rogu grzbietowego rdzenia kręgowego. Pozostałe 30% receptorów opioidowych jest zlokalizowanych postsynaptycznie na dendrytach neuronów spinothalamic i interneuronów drugiego rzędu .
Gdy opiat zwiąże się jako agonista z GPCR, nastąpi kaskada sygnalizacyjna skutkująca hamowaniem cyklazy adenylanowej i kanałów jonów wapniowych ze stymulacją kanałów jonów potasowych. Efektem netto tych zmian jest zmniejszenie wewnątrzkomórkowego cAMP i hiperpolaryzacja komórki neuronalnej zmniejszająca uwalnianie neuroprzekaźników. Dzięki tej ścieżce, gdy opiaty wiążą się z receptorem mu i aktywują go, następuje zmniejszenie transmisji sygnalizacji bólu. Ten szlak ukierunkowany jest na właściwości przeciwbólowe, z których znane są opiaty i do których są używane. Inne klinicznie ważne role mu obejmują jego udział w funkcjach układu oddechowego i sercowo-naczyniowego, perystaltyce przewodu pokarmowego , odżywianiu i nastroju. Te inne ścieżki są ważne, ponieważ wyjaśniają skutki uboczne używania opiatów, takie jak depresja oddechowa w dużych dawkach, zaparcia przy przewlekłym stosowaniu i właściwości uzależniające.
Bezwzględne przeciwwskazania
Osoby z następującymi schorzeniami nie powinny używać opioidów:
- ciężka niestabilność oddechowa
- ostra niestabilność psychiczna
- ryzyko niekontrolowanego samobójstwa
- zdiagnozowane nadużywanie substancji nienikotynowych
- Odstępy QTc dłuższe niż 500 milisekund, jeśli przepisano metadon
- ostre przekierowanie substancji kontrolowanych
- nietolerancja z poprzedniego próbnego stosowania z określonymi opioidami
- poważne działania niepożądane lub brak skuteczności.
Czynniki ryzyka nadużywania recept
Oto czynniki ryzyka nadużywania leków na receptę:
- przeszłość lub obecna historia nadużywania substancji
- zaburzenia psychiczne, które nie były leczone
- pacjenci w młodym wieku
- historia nadużywania substancji w rodzinie
- środowiska społeczne, które zachęcają do używania substancji
- długotrwałe stosowanie lub leczenie opioidami.
Statystycznie, pacjenci w średnim wieku z historią używania substancji i współistniejącymi chorobami psychicznymi mają większe ryzyko śmiertelności, takie jak samobójstwo.