Minimalne stężenie hamujące - Minimum inhibitory concentration
W mikrobiologii The minimalne stężenie hamujące ( MIC ) stanowi najniższe stężenie środka chemicznego, zazwyczaj leku, który zapobiega widocznego wzrostu z bakterii i bakterie. MIC zależy od mikroorganizmu, chorego człowieka (tylko in vivo) i samego antybiotyku. Często wyraża się ją w mikrogramach na mililitr (μg/ml) lub miligramach na litr (mg/l).
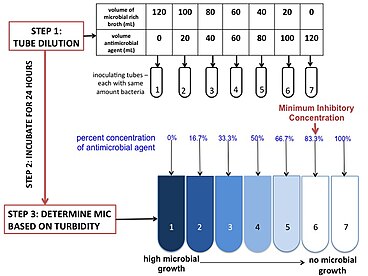
MIC określa się przygotowując roztwory substancji chemicznej in vitro w rosnących stężeniach, inkubując roztwory z oddzielnymi partiami hodowanych bakterii i mierząc wyniki przy użyciu rozcieńczenia agaru lub mikrorozcieńczenia bulionu . Wyniki zostały sklasyfikowane jako wrażliwe (często nazywane wrażliwymi), zwiększone narażenie lub oporne na konkretny środek przeciwdrobnoustrojowy za pomocą punktu przerwania. Punkty przerwania są ustalane na podstawie wartości, publikowanych w wytycznych organu referencyjnego, takiego jak amerykański Instytut Norm Klinicznych i Laboratoryjnych (CLSI), Brytyjskie Towarzystwo Chemioterapii Przeciwdrobnoustrojowej (BSAC) lub Europejski Komitet ds. Badania Wrażliwości na Przeciwdrobnoustroje (EUCAST). Na przestrzeni lat występowały poważne rozbieżności między wartościami granicznymi z różnych krajów europejskich oraz między wartościami ustalonymi przez Europejski Komitet ds. Badania Wrażliwości na Przeciwdrobnoustroje (EUCAST) i amerykański Instytut Norm Klinicznych i Laboratoryjnych (CLSI).
Podczas gdy MIC jest najniższym stężeniem środka przeciwbakteryjnego niezbędnym do zahamowania widocznego wzrostu, minimalne stężenie bakteriobójcze (MBC) jest minimalnym stężeniem środka przeciwbakteryjnego, które powoduje śmierć bakterii. Im bliżej MIC jest MBC, tym bardziej bakteriobójczy związek.
Pierwszym krokiem w odkrywaniu leku jest często badanie przesiewowe biblioteki kandydującej na lek pod kątem MIC wobec interesujących bakterii. W związku z tym wartości MIC są zwykle punktem wyjścia do szerszych ocen przedklinicznych nowych środków przeciwdrobnoustrojowych. Celem pomiaru minimalnego stężenia hamującego jest zapewnienie skutecznego doboru antybiotyków w celu zwiększenia skuteczności leczenia.
Tło
Historia
Po odkryciu i komercjalizacji antybiotyków mikrobiolog, farmakolog i lekarz Alexander Fleming opracował technikę rozcieńczania bulionu, wykorzystując do oceny zmętnienie bulionu. Powszechnie uważa się, że jest to punkt poczęcia minimalnych stężeń hamujących. Później, w latach 80. Instytut Standardów Klinicznych i Laboratoryjnych skonsolidował metody i standardy określania wartości MIC i zastosowania klinicznego. Po odkryciu nowych środków przeciwbakteryjnych, patogenów i ich ewolucji, protokoły CLSI są również stale aktualizowane, aby odzwierciedlić tę zmianę. Protokoły i parametry ustalone przez CLSI są uważane za „złoty standard” w Stanach Zjednoczonych i są wykorzystywane przez organy regulacyjne, takie jak FDA, do dokonywania ocen.
Zastosowanie kliniczne
Obecnie MIC stosuje się w badaniach wrażliwości na środki przeciwdrobnoustrojowe. Wartość MIC podaje się, umieszczając interpretację wrażliwości obok każdego antybiotyku. Różne interpretacje wrażliwości to: S (Sensitive), I (Intermediate) i R (Resistant). Interpretacje te zostały stworzone i wdrożone przez Instytut Norm Klinicznych i Laboratoryjnych (CLSI). W klinikach często dokładne patogeny nie mogą być łatwo określone na podstawie objawów pacjenta. Wtedy, nawet jeśli patogen zostanie określony, różne serotypy patogenów, takie jak Staphylococcus aureus, mają różne poziomy oporności na środki przeciwdrobnoustrojowe. W związku z tym trudno jest przepisać właściwe środki przeciwdrobnoustrojowe. W takich przypadkach MIC określa się przez hodowanie izolatu patogenu od pacjenta na płytce lub bulionie, który jest później używany w teście. Zatem znajomość MIC dostarczy lekarzowi cennych informacji do wypisania recepty. Dokładne i precyzyjne stosowanie środków przeciwdrobnoustrojowych jest również ważne w kontekście bakterii wielolekoopornych . Drobnoustroje, takie jak bakterie, zyskują oporność na środki przeciwdrobnoustrojowe, na które były wcześniej wrażliwe. Stosowanie niezgodnych poziomów środków przeciwdrobnoustrojowych zapewnia presję selekcyjną, która napędza kierunek i ewolucję oporności patogenów bakteryjnych. Zaobserwowano to przy poziomach antybiotyków poniżej MIC. W związku z tym coraz ważniejsze staje się określenie MIC, aby dokonać najlepszego wyboru przy przepisywaniu środków przeciwdrobnoustrojowych.
MIC jest stosowany klinicznie w porównaniu z MBC, ponieważ MIC jest łatwiej określić. Minimalne stężenie bakteriobójcze (MBC), które jest minimalnym stężeniem środka przeciwbakteryjnego powodującym śmierć drobnoustrojów, jest definiowane przez niezdolność do ponownej hodowli bakterii. Ponadto skuteczność leku jest ogólnie podobna, gdy jest przyjmowany zarówno w stężeniach MIC, jak i MBC, ponieważ układ odpornościowy gospodarza może wydalić patogen, gdy proliferacja bakterii jest zatrzymana. Gdy MBC jest znacznie wyższe niż MIC, toksyczność leku powoduje, że przyjmowanie MBC leku jest szkodliwe dla pacjenta. Toksyczność przeciwdrobnoustrojowa może przybierać różne formy, takie jak nadwrażliwość immunologiczna i toksyczność poza celem.
Metody
Test rozcieńczenia bulionu
Do przeprowadzenia tego testu potrzebne są trzy główne odczynniki : pożywka, środek przeciwdrobnoustrojowy i badany drobnoustrój. Najczęściej stosowanym podłożem jest Mueller Hinton Broth z dostosowaną kationami, ze względu na jego zdolność do wspomagania wzrostu większości patogenów i brak inhibitorów w stosunku do popularnych antybiotyków. W zależności od testowanego patogenu i antybiotyków, pożywki można zmieniać i/lub dostosowywać. Stężenie środka przeciwdrobnoustrojowego jest dostosowywane do prawidłowego stężenia poprzez zmieszanie podstawowego środka przeciwdrobnoustrojowego z pożywką. Dostosowany środek przeciwdrobnoustrojowy jest seryjnie rozcieńczany do wielu probówek (lub studzienek) w celu uzyskania gradientu. Szybkość rozcieńczania można regulować w zależności od punktu przerwania i potrzeb lekarza. Mikrob lub czynnik inokulujący musi pochodzić z tej samej jednostki tworzącej kolonie i musi mieć prawidłowe stężenie. Można to skorygować przez czas inkubacji i rozcieńczenie. W celu weryfikacji kontrolę dodatnią wysiewa się w stukrotnym rozcieńczeniu w celu zliczenia jednostek tworzących kolonie. Mikroby inokulują probówki (lub płytkę) i są inkubowane przez 16-20 godzin. MIC jest zazwyczaj określane przez zmętnienie.
Etest
Etesty mogą być również stosowane jako alternatywna metoda określania minimalnych wartości stężeń hamujących szerokiego zakresu środków przeciwdrobnoustrojowych przeciwko różnym grupom organizmów, która jest szeroko stosowana w laboratoriach mikrobiologicznych na całym świecie. Wyprodukowane przez bioMérieux , Etesty to gotowe do użycia, nieporowate plastikowe paski z odczynnikami z predefiniowanym gradientem antybiotyków, obejmującym ciągły zakres stężeń.