Kynurenina - Kynurenine
|
|

|
|
| Nazwy | |
|---|---|
|
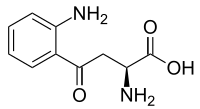
Preferowana nazwa IUPAC
Kwas ( 2S )-2-amino-4-(2-aminofenylo)-4-oksobutanowy |
|
| Inne nazwy
( S )-Kynurenina
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Siatka | Kynurenina |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
|
|
|
| Nieruchomości | |
| C 10 H 12 N 2 O 3 | |
| Masa cząsteczkowa | 208,217 g·mol -1 |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
l- Kynurenina jest metabolitem aminokwasu l - tryptofanu wykorzystywanego do produkcji niacyny .
Kynurenina jest syntetyzowana przez enzym dioksygenazę tryptofanu, która powstaje głównie, ale nie wyłącznie, w wątrobie, oraz 2,3-dioksygenazę indoloaminy , która powstaje w wielu tkankach w odpowiedzi na aktywację immunologiczną. Kynurenina i produkty jej dalszego rozpadu pełnią różne funkcje biologiczne, w tym rozszerzają naczynia krwionośne podczas stanu zapalnego i regulują odpowiedź immunologiczną. Niektóre nowotwory zwiększają produkcję kinureniny, co zwiększa wzrost guza.
Dowody sugerują, że zwiększona produkcja kinureniny może wywołać objawy depresji związane z interferonem leczenia wirusowego zapalenia wątroby typu C . Deficyty poznawcze w schizofrenii są związane z brakiem równowagi enzymów rozkładających kinureninę. Poziom kinureniny we krwi jest obniżony u osób z chorobą afektywną dwubiegunową . Produkcja kinureniny jest zwiększona w chorobie Alzheimera i chorobach układu krążenia, gdzie jej metabolity są związane z deficytami poznawczymi i objawami depresyjnymi. Kynurenina jest również związana z tikami .
Kynureninaza katabolizuje konwersję kinureniny do kwasu antranilowego, podczas gdy transaminaza oksoglutaranowa kinureniny katabolizuje jej konwersję do kwasu kinureninowego . 3-hydroksylaza kynureninowa przekształca kinureninę w 3-hydroksykinureninę .
Kynurenina została również zidentyfikowana jako jeden z dwóch związków, które tworzą pigment, który nadaje pająkowi nawłoci żółty kolor.
Dysfunkcja szlaku kinureninowego
Dysfunkcje stany różnych etapach szlak kinureninowy (takich jak kinureniny, kwasu kinureninowego , kwas chinolinowy , kwas antranilowy , 3-hydroksykinureniny) zostały opisane dla wielu zaburzeń, w tym:
- demencja HIV
- zespół Tourette'a
- Zaburzenia tikowe
- Zaburzenia psychiczne (takie jak schizofrenia , choroba afektywna dwubiegunowa , poważna depresja , zaburzenia lękowe )
- Stwardnienie rozsiane
- choroba Huntingtona
- Encefalopatie
- Metabolizm lipidów
- Metabolizm tłuszczu wątrobowego
- Toczeń rumieniowaty układowy
- Kwasuria glutarowa
- Witamina B 6 niedobór
- Zespół eozynofilii-mialgii
- Mialgiczne zapalenie mózgu i rdzenia / zespół przewlekłego zmęczenia
Regulacja w dół 3-monooksygenazy kinureniny (KMO) może być spowodowana polimorfizmami genetycznymi , cytokinami lub obydwoma. Niedobór KMO prowadzi do akumulacji kinureniny i przesunięcia szlaku metabolicznego tryptofanu w kierunku kwasu kinureninowego i antranilowego . Niedobór 3-monooksygenazy kinureniny jest związany z zaburzeniami mózgu (np. duża depresja, choroba afektywna dwubiegunowa, schizofrenia, zaburzenia tikowe) i wątroby.
