Erlotynib - Erlotinib
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Tarceva |
| Inne nazwy | Chlorowodorek erlotynibu |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a605008 |
| Dane licencyjne | |
Kategoria ciąży |
|
| Drogi administracji |
Tabletki doustnie |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | 59% |
| Wiązanie białek | 95% |
| Metabolizm | Wątroba (głównie CYP3A4 , mniej CYP1A2 ) |
| Okres półtrwania eliminacji | 36,2 godziny ( mediana ) |
| Wydalanie | >98% w postaci metabolitów, z czego >90% z kałem , 9% z moczem |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.216.020 |
| Dane chemiczne i fizyczne | |
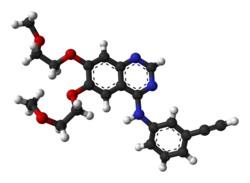
| Formuła | C 22 H 23 N 3 O 4 |
| Masa cząsteczkowa | 393,443 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Erlotynib , sprzedawany między innymi pod marką Tarceva , jest lekiem stosowanym w leczeniu niedrobnokomórkowego raka płuc (NSCLC) i raka trzustki . W szczególności stosuje się go w przypadku NSCLC z mutacjami w receptorze naskórkowego czynnika wzrostu (EGFR) — delecji eksonu 19 (del19) lub mutacji substytucji eksonu 21 (L858R) — który rozprzestrzenił się na inne części ciała . Jest przyjmowany doustnie.
Częste działania niepożądane to wysypka, biegunka, ból mięśni, ból stawów i kaszel. Poważne działania niepożądane mogą obejmować problemy z płucami, nerkami , niewydolność wątroby , perforację przewodu pokarmowego , udar i owrzodzenie rogówki . Stosowanie w ciąży może zaszkodzić dziecku. Jest inhibitorem receptorowej kinazy tyrozynowej , która działa na receptor naskórkowego czynnika wzrostu (EGFR).
Erlotynib został dopuszczony do użytku medycznego w Stanach Zjednoczonych w 2004 roku. Znajduje się na Liście Leków Podstawowych Światowej Organizacji Zdrowia .
Zastosowania medyczne
Rak płuc
Erlotynib w nieoperacyjnym niedrobnokomórkowym raku płuca dodany do chemioterapii poprawia przeżycie całkowite o 19% i przeżycie wolne od progresji (PFS) o 29% w porównaniu z samą chemioterapią. Amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła erlotynib do leczenia miejscowo zaawansowanego lub przerzutowego niedrobnokomórkowego raka płuca, u którego nie powiodła się co najmniej jedna wcześniejsza chemioterapia .
Wykazano, że w raku płuc erlotynib jest skuteczny u pacjentów z mutacjami EGFR lub bez, ale wydaje się być bardziej skuteczny u pacjentów z mutacjami EGFR. Przeżycie całkowite, przeżycie bez progresji i przeżycie roczne są podobne do standardowego leczenia drugiej linii (docetaksel lub pemetreksed). Całkowity odsetek odpowiedzi jest o około 50% lepszy niż standardowa chemioterapia drugiej linii. Pacjenci, którzy nie palą i byli palaczami lekkimi, z gruczolakorakiem lub podtypami takimi jak BAC, są bardziej narażeni na mutacje EGFR, ale mutacje mogą wystąpić u wszystkich typów pacjentów. Test na mutację EGFR został opracowany przez Genzyme .
Rak trzustki
W listopadzie 2005 roku FDA zatwierdziła erlotynib w połączeniu z gemcytabiną do leczenia miejscowo zaawansowanego, nieresekcyjnego lub przerzutowego raka trzustki .
Odporność na leczenie
Podobnie jak w przypadku innych konkurencyjnych wobec ATP drobnocząsteczkowych inhibitorów kinazy tyrozynowej, takich jak imatinib w CML , pacjenci szybko rozwijają oporność. W przypadku erlotynibu następuje to zwykle 8–12 miesięcy od rozpoczęcia leczenia. Ponad 50% oporności jest spowodowane mutacją w kieszeni wiążącej ATP domeny kinazy EGFR obejmującą podstawienie małej polarnej reszty treoniny dużą niepolarną resztą metioniny ( T790M ).
Około 20% lekooporności jest spowodowane przez amplifikację receptora czynnika wzrostu hepatocytów , który napędza aktywację PI3K zależną od ERBB3 .
Skutki uboczne
Pospolity
- Wysypka występuje u większości pacjentów. Przypomina to trądzik i dotyczy przede wszystkim twarzy i szyi. Jest samoograniczający się i ustępuje w większości przypadków, nawet przy ciągłym użytkowaniu. Niektóre badania kliniczne wykazały korelację między nasileniem reakcji skórnych a zwiększonym przeżyciem, chociaż nie zostało to ocenione ilościowo. Journal of Clinical Oncology odnotowano w 2004 roku, że „skórny [skóry] wysypki wydaje się być markerem zastępczym korzyści klinicznej, ale stwierdzenie to powinno zostać potwierdzone w badaniach trwających i przyszłych”. Biuletyn Lung Cancer Frontiers donosił w wydaniu z października 2003 r.: „Pacjenci z umiarkowanymi lub ciężkimi reakcjami skórnymi [wysypkami] mają znacznie lepsze przeżycie niż ci z łagodnymi reakcjami i znacznie lepiej niż ci, którzy nie mają skórnych objawów działania leków”.
- Biegunka
- Utrata apetytu
- Zmęczenie
- Częściowa utrata włosów (przez pasma, nie zwykle w kępkach)
Rzadki
- śródmiąższowe zapalenie płuc , które charakteryzuje się kaszlem i nasiloną dusznością . Może to być ciężkie i należy je brać pod uwagę u pacjentów z ostrym pogorszeniem oddychania.
- wrastające włoski , takie jak rzęsy
- toksyczność przewodu pokarmowego
- poważne lub śmiertelne perforacje przewodu pokarmowego
- toksyczność skórna
- pęcherzowe, pęcherze i złuszczające się stany skóry (niektóre śmiertelne)
- Zespół Stevensa-Johnsona / toksyczna nekroliza naskórka
- zaburzenia oczu
- uszkodzenia rogówki
- Toksyczność płucna
Interakcje
Erlotynib nie jest substratem żadnego z wątrobowych OATP (OATP1B1 lub OATP1B3). Ponadto erlotynib nie jest inhibitorem transportera OATP-1B1 ani OATP-1B3.
Erlotynib jest metabolizowany głównie przez enzym wątrobowy CYP3A4 . Związki, które indukują ten enzym (czyli stymulują jego produkcję), takie jak ziele dziurawca , mogą obniżać stężenie erlotynibu, podczas gdy inhibitory mogą zwiększać stężenie.
Mechanizm
Erlotynib jest inhibitorem receptora naskórkowego czynnika wzrostu ( inhibitorem EGFR ). Lek podąża za Iressa ( gefitynib ), który był pierwszym tego typu lekiem. Erlotynib jest ukierunkowany na kinazę tyrozynową receptora naskórkowego czynnika wzrostu (EGFR) , która jest silnie eksprymowana i czasami mutowana w różnych postaciach raka. Wiąże się w sposób odwracalny z miejscem wiązania adenozynotrifosforanu (ATP) receptora. Aby sygnał został przeniesiony, dwie cząsteczki EGFR muszą połączyć się, tworząc homodimer . Wykorzystują one następnie cząsteczkę ATP do wzajemnej transfosforylacji na resztach tyrozyny, co generuje reszty fosfotyrozyny, rekrutując białka wiążące fosfotyrozynę do EGFR w celu złożenia kompleksów białkowych, które przekazują kaskady sygnałów do jądra lub aktywują inne komórkowe procesy biochemiczne. Gdy erlotynib wiąże się z EGFR, tworzenie reszt fosfotyrozyny w EGFR nie jest możliwe i kaskady sygnałowe nie są inicjowane.
Społeczeństwo i kultura
Jest sprzedawany w Stanach Zjednoczonych przez Genentech i OSI Pharmaceuticals oraz przez Roche .
Amerykański patent na lek wygaśnie w 2020 r. W maju 2012 r. Sąd Okręgowy Stanów Zjednoczonych w Delaware wydał orzeczenie na korzyść OSI Pharmaceutical LLC przeciwko Mylan Pharmaceuticals, które podtrzymuje ważność patentu na Erlotinib. W Indiach generyczna firma farmaceutyczna Cipla walczy z Roche przeciwko indyjskiemu patentowi na ten lek.
Bibliografia
Zewnętrzne linki
- „Erlotynib” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Erlotynib” . Narodowy Instytut Raka .

