Cykl Carnota - Carnot cycle
| Termodynamika |
|---|

|
Cykl Carnota jest teoretyczna idealny termodynamiczny cykl zaproponowany przez francuskiego fizyka Sadi Carnot w 1824 i rozszerzone przez innych w 1830 i 1840 roku. Określa górną granicę sprawności, jaką każdy klasyczny silnik termodynamiczny może osiągnąć podczas konwersji ciepła na pracę , lub odwrotnie, sprawność układu chłodniczego w tworzeniu różnicy temperatur przez zastosowanie pracy do układu. Nie jest to rzeczywisty cykl termodynamiczny, ale konstrukt teoretyczny.
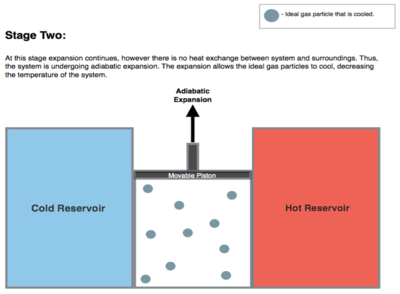
Każdy system termodynamiczny istnieje w określonym stanie . Kiedy układ przechodzi przez szereg różnych stanów i ostatecznie powraca do stanu początkowego, mówi się, że wystąpił cykl termodynamiczny. W trakcie przechodzenia przez ten cykl układ może wykonywać pracę na swoim otoczeniu, np. poruszając tłokiem, działając tym samym jak silnik cieplny . Układ przechodzący cykl Carnota nazywany jest silnikiem cieplnym Carnota , chociaż taki „doskonały” silnik jest tylko konstrukcją teoretyczną i nie można go zbudować w praktyce. Jednak zaprojektowano i uruchomiono mikroskopijny silnik cieplny Carnota.
Zasadniczo istnieją dwa „ zbiorniki ciepła ” stanowiące część silnika cieplnego w temperaturach i (odpowiednio na gorąco i zimno). Mają tak dużą pojemność cieplną, że na ich temperaturę praktycznie nie ma wpływu jeden cykl. Ponieważ cykl jest teoretycznie odwracalny , podczas cyklu nie występuje generacja entropii ; entropia jest zachowana. Podczas cyklu, dowolna ilość entropii jest pobierana z gorącego zbiornika i osadzana w zimnym zbiorniku. Ponieważ nie ma zmiany objętości w żadnym ze zbiorników, nie działają, a podczas cyklu pewna ilość energii jest pobierana z gorącego zbiornika, a mniejsza ilość energii jest odkładana w zimnym zbiorniku. Różnica w obu energiach jest równa pracy wykonanej przez silnik.
Gradacja
Cykl Carnota działający jako silnik cieplny składa się z następujących kroków:
-
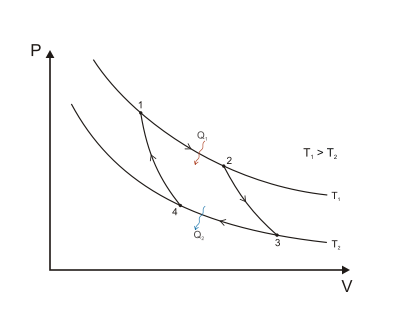
Ekspansja izotermiczna . Ciepło jest przekazywane odwracalnie ze zbiornika wysokotemperaturowego w stałej temperaturze T H (izotermiczne dodawanie lub pochłanianie ciepła). Podczas tego etapu (1 do 2 na Figurze 1 , A do B na Figurze 2 ) pozwala się na rozszerzenie gazu, wykonując pracę w otoczeniu poprzez wypychanie tłoka w górę (rysunek etapu 1, po prawej). Chociaż ciśnienie spada z punktów 1 do 2 (rysunek 1), temperatura gazu nie zmienia się podczas procesu, ponieważ jest on w kontakcie termicznym z gorącym zbiornikiem w T h , a zatem rozszerzanie jest izotermiczne. Energia cieplna Q 1 jest pobierana ze zbiornika wysokotemperaturowego, co powoduje wzrost entropii gazu o wielkość.
-
Izentropowa ( odwracalna adiabatyczna ) ekspansja gazu (izentropowa wydajność pracy). Na tym etapie (2 do 3 na Figurze 1 , B do C na Figurze 2 ) gaz w silniku jest izolowany termicznie zarówno od gorącego, jak i zimnego zbiornika. W ten sposób ani nie zyskują, ani nie tracą ciepła, jest toproces„ adiabatyczny ”. Gaz w dalszym ciągu rozpręża się poprzez redukcję ciśnienia, wykonując pracę nad otoczeniem (podnoszenie tłoka; rysunek drugiego stopnia, po prawej) i tracąc ilość energii wewnętrznej równą wykonanej pracy. Rozprężanie gazu bez dopływu ciepła powoduje jego schłodzenie do „zimnej” temperatury T c . Entropia pozostaje niezmieniona.
-
Kompresja izotermiczna. Odprowadzanie ciepła odwracalnie do zbiornika niskotemperaturowego przy stałej temperaturze T C . (izotermiczne odprowadzanie ciepła) (3 do 4 na rysunku 1 , C do D na rysunku 2 ) Teraz gaz w silniku jest w kontakcie termicznym z zimnym zbiornikiem w temperaturze T c . Otoczenie działa na gaz, popychając tłok w dół (rysunek 3, po prawej), powodując, że ilość energii cieplnej Q 2 opuszcza układ do zbiornika niskotemperaturowego i entropia układu zmniejsza się o wielkość . (Jest to ta sama ilość entropii pochłonięta w kroku 1, jak widać z nierówności Clausiusa ).
-
Odwracalna kompresja adiabatyczna. (4 do 1 na Figurze 1 , D do A na Figurze 2 ) Ponownie gaz w silniku jest izolowany termicznie od gorących i zimnych zbiorników i zakłada się, że silnik jest beztarciowy, a więc odwracalny. Podczas tego kroku otoczenie działa na gaz, popychając tłok dalej w dół (rysunek 4, po prawej), zwiększając jego energię wewnętrzną, sprężając go i powodując powrót jego temperatury do T h wyłącznie dzięki pracy dodanej do system, ale entropia pozostaje niezmieniona. W tym momencie gaz jest w tym samym stanie, co na początku kroku 1.
W tym przypadku,
- ,
lub,
- .
To prawda, jak i to zarówno niższe, a w rzeczywistości są w tym samym stosunku, jak .
Wykres ciśnienie-objętość
Kiedy cykl Carnota jest wykreślony na wykresie ciśnienie-objętość ( Rysunek 1 ), stopnie izotermiczne podążają za liniami izoterm dla płynu roboczego, stopnie adiabatyczne przemieszczają się między izotermami, a obszar ograniczony przez pełną ścieżkę cyklu reprezentuje całkowitą pracę, która można zrobić w jednym cyklu. Od punktu 1 do 2 i punktu 3 do 4 temperatura jest stała. Przenikanie ciepła z punktu 4 do 1 i punktu 2 do 3 są równe zeru.
Właściwości i znaczenie
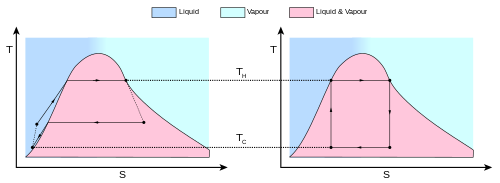
Wykres temperatura-entropia

Zachowanie silnika lub lodówki Carnota najlepiej zrozumieć za pomocą wykresu temperatura-entropia ( wykres T-S), w którym stan termodynamiczny jest określony przez punkt na wykresie z entropią (S) jako osią poziomą i temperaturą ( T) jako oś pionową ( Figura 2 ). W przypadku prostego układu zamkniętego (analiza masy kontrolnej) dowolny punkt na wykresie będzie reprezentował określony stan układu. Proces termodynamiczny będzie składał się z krzywej łączącej stan początkowy (A) i stan końcowy (B). Obszar pod krzywą będzie wynosił:
-
( 1 )
czyli ilość energii cieplnej przekazywanej w procesie. Jeśli proces przejdzie do większej entropii, obszar pod krzywą będzie ilością ciepła pochłoniętego przez system w tym procesie. Jeśli proces zmierza w kierunku mniejszej entropii, będzie to ilość usuniętego ciepła. Dla każdego procesu cyklicznego będzie część górna cyklu i część dolna. W cyklu zgodnym z ruchem wskazówek zegara obszar pod górną częścią będzie energią cieplną pochłoniętą podczas cyklu, podczas gdy obszar pod dolną częścią będzie energią cieplną usuniętą podczas cyklu. Obszar wewnątrz cyklu będzie wtedy różnicą między tymi dwoma, ale ponieważ energia wewnętrzna systemu musiała powrócić do swojej początkowej wartości, ta różnica musi być ilością pracy wykonanej przez system w cyklu. Odnosząc się do rysunku 1 , matematycznie, dla procesu odwracalnego możemy zapisać ilość pracy wykonanej w procesie cyklicznym jako:
-
( 2 )
Ponieważ dU jest różniczką dokładną , jej całka po dowolnej zamkniętej pętli wynosi zero i wynika z tego, że obszar wewnątrz pętli na diagramie T-S jest równy całkowitej pracy wykonanej, jeśli pętla jest przemierzana w kierunku zgodnym z ruchem wskazówek zegara, i jest równa do całkowitej pracy wykonanej w systemie, gdy pętla jest pokonywana w kierunku przeciwnym do ruchu wskazówek zegara.
Cykl Carnota
Ocena powyższej całki jest szczególnie prosta dla cyklu Carnota. Ilość energii przekazywanej podczas pracy wynosi
Całkowita ilość energii cieplnej przekazanej z gorącego zbiornika do systemu będzie
a całkowita ilość energii cieplnej przekazanej z systemu do zimnego zbiornika będzie
Wydajność definiuje się jako:
-
( 3 )
gdzie
- W to praca wykonana przez system (energia opuszczająca system jako praca),
- to ciepło pobrane z systemu (energia cieplna opuszczająca system),
- to ciepło wprowadzone do systemu (energia cieplna wchodząca do systemu),
- jest bezwzględną temperaturą zimnego zbiornika i
- to temperatura bezwzględna gorącego zbiornika.
- to maksymalna entropia systemu
- jest minimalną entropią systemu
Ta definicja sprawności ma sens dla silnika cieplnego , ponieważ jest to ułamek energii cieplnej pobranej z gorącego zbiornika i zamienionej na pracę mechaniczną. Cykl Rankine'a jest zwykle praktyczne przybliżenie.
Odwrócony cykl Carnota
Opisany cykl pracy silnika cieplnego Carnota jest cyklem całkowicie odwracalnym. To znaczy wszystkie procesy, które go tworzą, można odwrócić, w którym to przypadku staje się cyklem chłodniczym Carnota. Tym razem cykl pozostaje dokładnie taki sam, z wyjątkiem tego, że kierunki wszelkich interakcji ciepła i pracy są odwrócone. Ciepło jest pobierane ze zbiornika niskotemperaturowego, ciepło jest odprowadzane do zbiornika wysokotemperaturowego, a do osiągnięcia tego wszystkiego potrzebny jest wkład pracy. Wykres P–V odwróconego cyklu Carnota jest taki sam jak dla cyklu Carnota, z wyjątkiem tego, że kierunki procesów są odwrócone.
Twierdzenie Carnota
Z powyższego wykresu widać, że dla dowolnego cyklu działającego pomiędzy temperaturami a , żaden nie może przekroczyć wydajności cyklu Carnota.
Twierdzenie Carnota jest formalnym stwierdzeniem tego faktu: Żaden silnik pracujący pomiędzy dwoma zbiornikami ciepła nie może być bardziej wydajny niż silnik Carnota pracujący pomiędzy tymi samymi zbiornikami. Zatem równanie 3 daje maksymalną możliwą wydajność dla dowolnego silnika przy odpowiednich temperaturach. W następstwie twierdzenia Carnota stwierdza się, że: Wszystkie silniki odwracalne działające między tymi samymi zbiornikami ciepła są równie wydajne. Przekształcenie prawej strony równania daje bardziej zrozumiałą formę równania, a mianowicie, że teoretyczna maksymalna sprawność silnika cieplnego równa się różnicy temperatur pomiędzy gorącym i zimnym zbiornikiem podzielonej przez bezwzględną temperaturę zbiornika gorącego . Przyglądając się tej formule staje się ciekawy fakt: obniżenie temperatury zimnego zbiornika będzie miało większy wpływ na wydajność górną silnika cieplnego niż podniesienie temperatury gorącego zbiornika o taką samą wartość. W rzeczywistym świecie może to być trudne do osiągnięcia, ponieważ zimnym zbiornikiem jest często istniejąca temperatura otoczenia.
Innymi słowy, maksymalną wydajność osiąga się wtedy i tylko wtedy, gdy w cyklu nie powstaje nowa entropia, co miałoby miejsce np. gdyby tarcie prowadziło do rozproszenia pracy w ciepło. W takim przypadku cykl nie jest odwracalny, a twierdzenie Clausiusa staje się nierównością, a nie równością. W przeciwnym razie, ponieważ entropia jest funkcją stanu , wymagane odprowadzanie ciepła do środowiska w celu pozbycia się nadmiaru entropii prowadzi do (minimalnego) zmniejszenia wydajności. Tak więc równanie 3 podaje wydajność każdego odwracalnego silnika cieplnego .
W mezoskopowych silnikach cieplnych praca na cykl pracy na ogół waha się z powodu szumu termicznego. Jeśli cykl jest wykonywany quasi-statycznie, fluktuacje zanikają nawet w mezoskali. Jeśli jednak cykl jest wykonywany szybciej niż czas relaksacji czynnika roboczego, fluktuacje pracy są nieuniknione. Niemniej jednak, gdy liczone są fluktuacje pracy i ciepła, istnieje dokładna równość, która wiąże wykładniczą średnią pracy wykonanej przez dowolny silnik cieplny i przenoszenie ciepła z cieplejszej kąpieli.
Sprawność prawdziwych silników cieplnych
- Zobacz też: Sprawność silnika cieplnego i inne kryteria wydajności
Carnot zdał sobie sprawę, że w rzeczywistości nie jest możliwe zbudowanie termodynamicznie odwracalnego silnika, więc prawdziwe silniki cieplne są jeszcze mniej wydajne niż wskazuje równanie 3. Ponadto prawdziwe silniki, które działają w tym cyklu, są rzadkością. Niemniej jednak równanie 3 jest niezwykle przydatne do określenia maksymalnej wydajności, jakiej można oczekiwać dla danego zestawu zbiorników termicznych.
Chociaż cykl Carnota jest idealizacją, wyrażenie efektywności Carnota jest nadal użyteczne. Rozważ średnie temperatury,
przy którym ciepło jest odpowiednio wprowadzane i odprowadzane. Zastąp T H i T C w równaniu ( 3 ) odpowiednio przez ⟨ T H ⟩ i ⟨ T C ⟩.
Dla cyklu Carnota lub jego odpowiednika, średnia wartość ⟨ T H ⟩ będzie równa najwyższej dostępnej temperaturze, czyli T H , i ⟨ T C ⟩ najniższej, czyli T C . Dla innych mniej wydajnych cykli, ⟨ T H ⟩ będzie niższe niż T H , a ⟨ T C ⟩ będzie wyższe niż T C . Może to pomóc zilustrować, na przykład, dlaczego przegrzewacz lub regenerator może poprawić sprawność cieplną elektrowni parowych – i dlaczego sprawność cieplna elektrowni z cyklem skojarzonym (które zawierają turbiny gazowe pracujące w jeszcze wyższych temperaturach) przewyższa sprawność konwencjonalnych instalacje parowe. Pierwszy prototyp silnika wysokoprężnego oparty był na cyklu Carnota.
Zobacz też
Bibliografia
- Uwagi
- ^ Mikołaj Giordano (13 lutego 2009). Fizyka kolegium: rozumowanie i relacje . Nauka Cengage. P. 510. Numer ISBN 978-0-534-42471-8.
- ^ Ignacio A. Martínez; i in. (6 stycznia 2016). „Silnik Browniana Carnota” . Fizyka przyrody. s. 67-70.
- ^ Çengel, Yunus A. i Michael A. Boles. Termodynamika: podejście inżynierskie . 7 wyd. Nowy Jork: McGraw-Hill, 2011. s. 299. Drukuj.
- ^ Holubec Wiktor i Ryabov Artem (2018). „Jazda na rowerze oswaja wahania mocy w pobliżu optymalnej wydajności”. Fiz. Ks . 121 (12): 120601. arXiv : 1805.00848 . doi : 10.1103/PhysRevLett.121.120601 . PMID 30296120 . S2CID 52943273 .
- ^ NA Sinicyna (2011). „Relacja wahań dla silników cieplnych”. J. Fiz. O: Matematyka. Teoria . 44 (40): 405001. arXiv : 1111,7014 . Kod Bibcode : 2011JPhA...44N5001S . doi : 10.1088/1751-8113/44/40/405001 . S2CID 119261929 .
- Źródła
-
- Carnot, Sadi, Refleksje na temat motywującej mocy ognia
- Ewing, JA (1910) The Steam-Engine and Other Engines, wydanie 3, strona 62, za pośrednictwem archiwum internetowego
- Feynman, Richard P.; Leighton, Robert B.; Piaski Mateusza (1963). Wykłady Feynmana z fizyki . Wydawnictwo Addison-Wesley. s. Rozdział 44 . Numer ISBN 978-0-201-02116-5.
- Halliday, Dawidzie; Resnick, Robert (1978). Fizyka (3rd ed.). John Wiley & Synowie. s. 541–548 . Numer ISBN 978-0-471-02456-9.
- Kittel, Karol ; Kroemera, Herberta (1980). Fizyka Cieplna (wyd. 2). Firma WH Freemana. Numer ISBN 978-0-7167-1088-2.
- Kostic, M (2011). „Powrót do drugiego prawa degradacji energii i generowania entropii: od pomysłowego rozumowania Sadi Carnota do holistycznego uogólnienia”. Konf. AIP Proc . Materiały konferencyjne AIP. 1411 : 327–350. CiteSeerX 10.1.1.405.1945 . doi : 10.1063/1.3665247 .Amerykański Instytut Fizyki, 2011. ISBN 978-0-7354-0985-9 . Streszczenie: [1] . Pełny artykuł (24 strony [2] ), również w [3] .
Zewnętrzne linki
- Artykuł o hiperfizyce na temat cyklu Carnota.
- Interaktywny aplet Java pokazujący zachowanie silnika Carnota.
- SM Blinder Carnot Cycle na gazie idealnym zasilanym przez Wolfram Mathematica