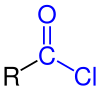
Chlorek acylu - Acyl chloride
W chemii organicznej An chlorek acylu (lub chlorek kwasowy ) jest związek organiczny z grupą funkcyjną, - CO Cl . Ich wzór jest zwykle zapisywany jako RCOCl, gdzie R jest łańcuchem bocznym . Są reaktywnymi pochodnymi kwasów karboksylowych . A Przykład specyficzna chlorkiem acylowym jest chlorek acetylu , CH 3 COCl. Chlorki acylowe są najważniejszym podzbiorem halogenków acylowych .
Nomenklatura
Gdzie ugrupowanie chlorku acylu ma priorytet, chlorkami acylowymi są nazywane poprzez nazwę kwasu karboksylowego macierzystego i zastępując chlorek -ilo do kwasu -ic . Zatem:
- chlorek acetylu CH 3 COCl
- chlorek benzoilu C 6 H 5 COCl
Gdy inne grupy funkcyjne mają pierwszeństwo, chlorki acylu są uważane za przedrostki — chlorokarbonyl- :
- kwas (chlorokarbonylo)octowy ClOCCH 2 COOH
Nieruchomości
Ze względu na brak zdolności do tworzenia wiązań wodorowych chlorki acylu mają niższe temperatury wrzenia i topnienia niż podobne kwasy karboksylowe . Na przykład kwas octowy wrze w 118°C, podczas gdy chlorek acetylu wrze w 51°C. Jak większość związków karbonylowych , spektroskopia w podczerwieni ujawnia pasmo w pobliżu 1750 cm- 1 .
Najprostszym stabilnym chlorkiem acylu jest chlorek acetylu; chlorek formylu nie jest stabilny w temperaturze pokojowej, chociaż można go wytwarzać w temperaturze –60 °C lub niższej. Chlorek acylu hydrolizuje (reaguje z wodą).
Synteza
Szlaki przemysłowe
Przemysłowa droga do chlorku acetylu obejmuje reakcję bezwodnika octowego z chlorowodorem :
- (CH 3 CO) 2 O + HCl → CH 3 COCl + CH 3 CO 2 H
Propionylu wytwarza się przez chlorowanie kwasu propionowego z fosgenem :
- CH 3 CH 2 CO 2 H + COCl 2 → CH 3 CH 2 COCl + HCl + CO 2
Chlorek benzoilu jest wytwarzany przez częściową hydrolizę benzotrichlorku :
- C 6 H 5 Cl 3 + H 2 O → C 6 H 5 C (O) Cl + 2 HCI
Metody laboratoryjne: chlorek tionylu
W laboratorium, chlorkami acylowymi są zazwyczaj wytwarza się przez traktowanie kwasów karboksylowych z chlorkiem tionylu (SOCh 2 ). Reakcja jest katalizowana przez dimetyloformamid i inne dodatki.
Tionylu chloride jest dobrze nadaje się reagent jako produktów ubocznych (HCI, SO 2 ) są gazy i pozostały chlorek tionylu można łatwo usunąć w wyniku niskiej temperaturze wrzenia (76 ° C). Reakcja z chlorkiem tionylu jest katalizowana przez dimetyloformamid .
Metody laboratoryjne: chlorki fosforu
Popularny jest również trójchlorek fosforu (PCl 3 ), pentachlorek fosforu (PCl 5 ). chociaż wymagany jest nadmiar odczynnika. Pentachlorek fosforu jest również skuteczny, ale tylko jeden chlorek jest przenoszony:
- RCO 2 H + PCl 5 → RCOCl + POCl 3 + HCl
Metody laboratoryjne: chlorek oksalilu
Inna metoda polega na zastosowaniu chlorku oksalilu :
- RCO 2 H + ClCOCOCl → RCOCl + CO + CO 2 + HCl
Reakcja jest katalizowana przez dimetyloformamid (DMF), który reaguje z chlorkiem oksalilu w pierwszym etapie, dając iminowy związek pośredni, który reaguje z kwasem karboksylowym, odrywając tlenek i regenerując katalizator DMF. W porównaniu z chlorkiem tionylu chlorek oksalilu jest droższy, ale także łagodniejszy i dlatego bardziej selektywny.
Inne metody laboratoryjne
Jako źródło chlorków można stosować chlorki kwasowe. W ten sposób chlorek acetylu można destylować z mieszaniny chlorku benzoilu i kwasu octowego:
- CH 3 CO 2 H + C 6 H 5 COCl → CH 3 COCl + C 6 H 5 CO 2 H
Inne metody, które nie tworzą HCl, obejmują reakcję Appela :
- RCO 2 H + Ph 3 P + CCl 4 → RCOCl + Ph 3 PO + HCl 3
Innym jest użycie chlorku cyjanurowego :
- RCO 2 H + C 3 N 3 Cl 3 → RCOCl + C 3 N 3 Cl 2 OH
Reakcje
Chlorek acylu to reaktywne, wszechstronne odczynniki. Chlorki acylu mają większą reaktywność niż inne pochodne kwasów karboksylowych, takie jak bezwodniki kwasowe , estry lub amidy :
Reakcje nukleofilowe
Chlorki kwasowe są przydatne do wytwarzania amidów, estrów, bezwodników. W wyniku tych reakcji powstają chlorki, które mogą być niepożądane. Chlorki acylu hydrolizują dając kwas karboksylowy:
Ta hydroliza jest zwykle raczej uciążliwa niż zamierzona. Chlorki acylu stosuje się do wytwarzania bezwodników kwasowych , amidów i estrów , poprzez reakcję chlorków kwasowych odpowiednio z: solą kwasu karboksylowego , aminą lub alkoholem .
Mechanizm
Uważa się, że alkoholiza halogenków acylu (alkoksy-dehalogenacja) przebiega zgodnie z mechanizmem S N 2 (Schemat 10). Jednak mechanizm może być również czworościenny lub S N 1 w silnie polarnych rozpuszczalnikach (podczas gdy S N 2 reakcja obejmuje skoordynowaną reakcję, tetraedryczny szlak addycji-eliminacji obejmuje dostrzegalny związek pośredni).
Zasada, np. pirydyna lub N,N- dimetyloformamid, katalizuje acylowanie. Odczynniki te aktywują chlorek acylu poprzez mechanizm katalizy nukleofilowej. Amina atakuje wiązanie karbonylowe i przypuszczalnie tworzy najpierw przejściowy tetraedryczny związek pośredni, a następnie, przez podstawienie grupy opuszczającej, czwartorzędową sól acyloamoniową. Ta czwartorzędowa sól acyloamoniowa jest bardziej podatna na atak alkoholi lub innych nukleofilów.
Zastosowanie dwóch faz (wodnej dla aminy, organicznej dla chlorku acylu) nazywa się reakcją Schotten-Baumanna . To podejście jest stosowane w przygotowaniu nylonu za pomocą tak zwanej sztuczki z nylonową liną ( ).
Konwersja do ketonów
Węglowe nukleofile, takie jak odczynniki Grignarda , przekształcają chlorki acylu w ketony , które z kolei są podatne na atak drugiego równoważnika, dając trzeciorzędowy alkohol . Reakcja halogenków acylowych z niektórymi odczynnikami organokadmowymi zatrzymuje się na etapie ketonowym. Reakcja z odczynnikami Gilmana daje również ketony, odzwierciedlając niską nukleofilowość tych związków diorganomiedzi litu.
Zmniejszenie
Chlorki acylu są redukowane przez wodorek litowo-glinowy i wodorek diizobutyloglinowy do pierwszorzędowych alkoholi. Wodorek tri-tert-butoksyglinu litu , obszerny donor wodorku, redukuje chlorki acylu do aldehydów, podobnie jak redukcja Rosenmunda za pomocą gazowego wodoru nad zatrutym katalizatorem palladowym.
Acylacja aren
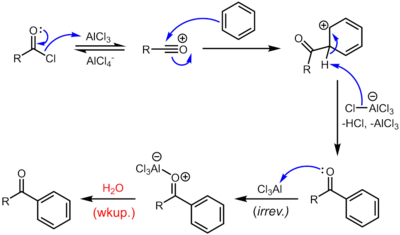
W przypadku katalizatorów kwasowych Lewisa, takich jak chlorek żelazowy lub chlorek glinu, chlorki acylu uczestniczą w acylacji Friedela-Craftsa , dając ketony arylowe:
Ze względu na trudne warunki i reaktywność półproduktów, ta skądinąd całkiem użyteczna reakcja bywa niechlujna, a także nieprzyjazna dla środowiska.
Dodatek utleniający
Chlorki acylu reagują z centrami metali o niskiej wartościowości. Ilustrację jest dodanie utleniającego z chlorkiem acetylu do kompleksu Vaska użytkownika , konwersja kwadratowy płaskich Ir (I) oktaedrycznej Ir (III):
- IrCl(CO)(PPh 3 ) 2 + CH 3 COCl → CH 3 COIrCl 2 (CO)(PPh 3 ) 2
Zagrożenia
Chlorki acylu o niskiej masie cząsteczkowej są często lachrymatorami i gwałtownie reagują z wodą, alkoholami i aminami.
Bibliografia
- ^ Nomenklatura chemii organicznej , R-5.7.6 Halogenki kwasowe
- ^ Sih, John C. (2001-04-15), "Chlorek Formylu", w John Wiley & Sons, Ltd (red.), Encyklopedia odczynników do syntezy organicznej , John Wiley & Sons, Ltd, doi : 10.1002/047084289x .rf026 , ISBN 9780471936237
- ^ Richard OC Norman; James M. Coxon (16 września 1993). Zasady syntezy organicznej, wydanie III . CRC Prasa. P. 371. Numer ISBN 978-0-7487-6162-3.
- ^ Wang, Hong-Yong; Xie, Min-Hao; Luo, Szi-Neng; Zou, Pei; Liu, Ya-Ling (2009). „Chlorek 3,5-dinitrobenzoilu” . Acta Crystallographica Sekcja E . 65 (10): o2460. doi : 10.1107/S1600536809036228 . PMC 2970283 . PMID 21577915 .
- ^ Patent USA 5672749 , Phillip R. DeVrou, W. Bryan Waites, Robert E. Young, „Proces przygotowania chlorku acetylu”
- ^ Samel, Ulf-Rainer; Kohlera, Waltera; Gracz, Armin Otto; Keuser, Ullrich (2005). „Kwas propionowy i pochodne”. Encyklopedia Chemii Przemysłowej Ullmanna . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a22_223 .
- ^ Maki, Takao; Takeda, Kazuo (2002). „Kwas benzoesowy i pochodne”. Encyklopedia Chemii Przemysłowej Ullmanna . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a03_555 .
- ^ Helferich, B.; Schäfer, W. (1929). „Chlorek n-butylu”. Syntezy organiczne . 9 : 32. doi : 10.15227/orgsyn.009.0032 .
- ^ B c Martin Ansell (1972). „Przygotowanie halogenków acylowych”. W Saul Patai (red.). Halogenki acylowe . Chemia grup funkcjonalnych PATAI. s. 35-68. doi : 10.1002/9780470771273.ch2 . Numer ISBN 9780470771273.
- ^ JS Pizey, Odczynniki syntetyczne, tom. 1, Halsted Press, Nowy Jork, 1974.
- ^ B c Clayden Jonathan (2001). Chemia organiczna . Oksford: Oxford University Press. s. 276–296 . Numer ISBN 0-19-850346-6.
- ^ B Allen CFH; Barker, WE (1932). „Dezoksybenzoina”. Syntezy organiczne . 12 : 16. doi : 10.15227/orgsyn.012.0016 .
- ^ Adams, Roger (1923). „Chlorek p-nitrobenzoilu”. Syntezy organiczne . 3 : 75. doi : 10.15227/orgsyn.003.0075 .
- ^ a b c d Boyd, Robert W.; Morrisona, Roberta (1992). Chemia organiczna . Englewood Cliffs, NJ: Prentice Hall. s. 666–762. Numer ISBN 0-13-643669-2.
- ^ LP Kyrides (1940). „Chlorek fumarylu”. Syntezy organiczne . 20 : 51. doi : 10.15227/orgsyn.020.0051 .
- ^ „ Trifenylofosfina czterochlorek węgla Taschner, Michael J. e-EROS: Encyklopedia odczynników do syntezy organicznej , 2001
- ^ K. Venkataraman; DR Wagle (1979). „Chlorek cyjanurowy: przydatny odczynnik do przekształcania kwasów karboksylowych w chlorki, estry, amidy i peptydy”. Czworościan Lett. 20 (32): 3037-3040. doi : 10.1016/S0040-4039(00)71006-9 .
- ^ Sonntag, Norman OV (1953-04-01). „Reakcje chlorków kwasów alifatycznych”. Recenzje chemiczne . 52 (2): 237–416. doi : 10.1021/cr60162a001 . ISSN 0009-2665 .
- ^ Bentley, T. William; Llewellyn, Gareth; McAlister, J. Anthony (styczeń 1996). „Mechanizm SN2 do alkoholizy, aminolizy i hydrolizy chlorku acetylu” . Czasopismo Chemii Organicznej . 61 (22): 7927-7932. doi : 10.1021/jo9609844 . ISSN 0022-3263 . PMID 11667754 .
- ^ CH Bamford i CFH Tipper, Kompleksowa kinetyka chemiczna: tworzenie estrów i hydroliza oraz reakcje pokrewne, Elsevier, Amsterdam, 1972.
- ^ Lis, Józef M.; Dmitrenko, Olga; Liao, Lian-an; Bach, Robert D. (październik 2004). „Badania obliczeniowe substytucji nukleofilowej w węglu karbonylowym: mechanizm SN 2 w porównaniu z tetraedrycznym półproduktem w syntezie organicznej” . Czasopismo Chemii Organicznej . 69 (21): 7317-7328. doi : 10.1021/jo049494z . ISSN 0022-3263 . PMID 15471486 .
- ^ Hubbard, Patricia; Brittain, William J. (luty 1998). „Mechanizm tworzenia estrów katalizowanych aminami z kwaśnego chlorku i alkoholu” . Czasopismo Chemii Organicznej . 63 (3): 677–683. doi : 10.1021/jo9716643 . ISSN 0022-3263 . PMID 11672060 .
- ^ Morgan, Paweł W.; Kwolek, Stephanie L. (kwiecień 1959). „Sztuczka z liny nylonowej: Demonstracja polimeryzacji kondensacyjnej” . Dziennik Edukacji Chemicznej . 36 (4): 182. Kod Bib : 1959JChEd..36..182M . doi : 10.1021/ed036p182 . ISSN 0021-9584 .
- ^ David A. Shirley (2011). „Synteza ketonów z halogenków kwasowych i związków metaloorganicznych magnezu, cynku i kadmu”. Organizacja Reakcje : 28-58. doi : 10.1002/0471264180.lub008.02 . Numer ISBN 978-0471264187.
- ^ William Reusch. „Pochodne kwasu karboksylowego” . VirtualText Chemii Organicznej . Uniwersytet Stanowy Michigan . Zarchiwizowane od oryginału w dniu 2016-05-16 . Źródło 19.02.2009 .
- ^ Hartwig, Jan (2010). Chemia metali organotransmisji: od wiązania do katalizy . Nowy Jork: Uniwersyteckie książki naukowe. P. 1160. Numer ISBN 978-1-938787-15-7.