Biodruk 3D - 3D bioprinting
Biodrukowanie trójwymiarowe ( 3D ) to wykorzystanie technik podobnych do drukowania 3D do łączenia komórek, czynników wzrostu i/lub biomateriałów w celu wytwarzania części biomedycznych, często w celu naśladowania naturalnych cech tkanki. Ogólnie rzecz biorąc, biodrukowanie 3D może wykorzystywać metodę warstwa po warstwie do osadzania materiałów znanych jako biotusz w celu tworzenia struktur tkankowych, które są później wykorzystywane w różnych dziedzinach medycyny i inżynierii tkankowej. Biodrukowanie 3D obejmuje szeroki zakres technik biodrukowania i biomateriałów .
Obecnie biodrukowanie może być wykorzystywane do drukowania tkanek i narządów, aby pomóc w badaniach leków i pigułek. Jednak innowacje rozciągają się od biodrukowania macierzy zewnątrzkomórkowej do mieszania komórek z hydrożelami osadzanymi warstwa po warstwie w celu wytworzenia pożądanej tkanki. Ponadto biodrukowanie 3D zaczęło obejmować drukowanie rusztowań. Rusztowania te mogą służyć do regeneracji stawów i więzadeł.
Proces
Biodrukowanie 3D zazwyczaj składa się z trzech etapów: przed biodrukowaniem, biodrukowaniem i biodrukowaniem po biodruku.
Wstępne biodrukowanie
Pre-biodrukowanie to proces tworzenia modelu, który później stworzy drukarz i doboru materiałów, które zostaną użyte. Jednym z pierwszych kroków jest wykonanie biopsji narządu. Powszechnie stosowane technologie biodrukowania to tomografia komputerowa (CT) i rezonans magnetyczny (MRI). Aby drukować metodą warstwa po warstwie, na obrazach wykonywana jest rekonstrukcja tomograficzna . Obrazy teraz 2D są następnie przesyłane do drukarki w celu wykonania. Po utworzeniu obrazu pewne komórki są izolowane i mnożone. Komórki te są następnie mieszane ze specjalnym upłynnionym materiałem, który dostarcza tlen i inne składniki odżywcze, aby utrzymać je przy życiu. W niektórych procesach komórki są otoczone sferoidami komórkowymi o średnicy 500 μm. Ta agregacja komórek nie wymaga rusztowania i jest wymagana do umieszczenia w rurkowatej fuzji tkanek w procesach takich jak wytłaczanie.
Biodruk
W drugim etapie płynna mieszanina komórek, matrycy i składników odżywczych, znana jako biotusz, jest umieszczana we wkładzie drukarki i deponowana za pomocą skanów medycznych pacjentów. Kiedy biodrukowana tkanka wstępna jest przenoszona do inkubatora, ta tkanka wstępna oparta na komórkach dojrzewa w tkankę.
Biodrukowanie 3D do wytwarzania konstrukcji biologicznych zazwyczaj obejmuje umieszczanie komórek na biokompatybilnym rusztowaniu przy użyciu kolejnego podejścia warstwa po warstwie, aby wygenerować trójwymiarowe struktury przypominające tkankę. Wykazano, że sztuczne narządy, takie jak wątroba i nerki, wykonane za pomocą biodruku 3D, nie mają kluczowych elementów wpływających na organizm, takich jak działające naczynia krwionośne, kanaliki do zbierania moczu oraz wzrost miliardów komórek wymaganych dla tych organów. Bez tych składników organizm nie ma możliwości dostania się w głąb swojego wnętrza niezbędnych składników odżywczych i tlenu. Biorąc pod uwagę, że każda tkanka w ciele składa się naturalnie z różnych typów komórek, wiele technologii drukowania tych komórek różni się pod względem zdolności do zapewnienia stabilności i żywotności komórek podczas procesu produkcyjnego. Niektóre z metod wykorzystywanych do biodrukowania 3D komórek to fotolitografia , magnetyczny biodruk 3D , stereolitografia i bezpośrednia ekstruzja komórek.
Post-biodrukowanie
Proces post-biodrukowania jest niezbędny do stworzenia stabilnej struktury z materiału biologicznego. Jeśli ten proces nie jest dobrze utrzymany, zagrożona jest mechaniczna integralność i funkcja drukowanego obiektu 3D. Do utrzymania obiektu potrzebne są zarówno stymulacje mechaniczne, jak i chemiczne. Te stymulacje wysyłają sygnały do komórek, aby kontrolować przebudowę i wzrost tkanek. Ponadto, w ostatnim rozwoju, technologie bioreaktorów umożliwiły szybkie dojrzewanie tkanek, unaczynienie tkanek i zdolność do przetrwania przeszczepów.
Bioreaktory zapewniają konwekcyjny transport składników odżywczych, tworzą środowiska mikrograwitacyjne, zmieniają ciśnienie powodujące przepływ roztworu przez komórki lub dodają kompresję w celu obciążenia dynamicznego lub statycznego. Każdy rodzaj bioreaktora jest idealny dla różnych typów tkanek, na przykład bioreaktory kompresyjne są idealne dla tkanki chrzęstnej.
Podejście do biodruku
Badacze w tej dziedzinie opracowali metody wytwarzania żywych narządów, które są skonstruowane z odpowiednimi właściwościami biologicznymi i mechanicznymi. Biodrukowanie 3D opiera się na trzech głównych podejściach: biomimice, autonomicznym samoporządkowaniu i mini-tkankach budulcowych.
Biomimikra
Pierwsze podejście do biodrukowania nazywa się biomimikra. Głównym celem tego podejścia jest stworzenie wytworzonych struktur, które są identyczne z naturalną strukturą, która znajduje się w tkankach i narządach ludzkiego ciała. Biomimikra wymaga powielania kształtu, struktury i mikrośrodowiska narządów i tkanek. Zastosowanie biomimikry w biodrukowaniu polega na tworzeniu zarówno identycznych komórkowych, jak i zewnątrzkomórkowych części narządów. Aby to podejście było skuteczne, tkanki muszą być replikowane w mikroskali. Dlatego konieczne jest zrozumienie mikrośrodowiska, charakteru sił biologicznych w tym mikrośrodowisku, dokładnej organizacji funkcjonalnych i wspierających typów komórek, czynników rozpuszczalności oraz składu macierzy zewnątrzkomórkowej.
Autonomiczny samodzielny montaż
Drugim podejściem biodrukowania jest autonomiczny samomontaż. Podejście to opiera się na fizycznym procesie rozwoju narządów embrionalnych jako modelu do replikacji tkanek będących przedmiotem zainteresowania. Kiedy komórki są we wczesnym stadium rozwoju, tworzą własny blok budulcowy macierzy zewnątrzkomórkowej, właściwą sygnalizację komórkową oraz niezależne rozmieszczenie i wzorcowanie, aby zapewnić wymagane funkcje biologiczne i mikroarchitekturę. Autonomiczna samoorganizacja wymaga konkretnych informacji o technikach rozwojowych tkanek i narządów zarodka. Istnieje model „bez rusztowania”, który wykorzystuje samoorganizujące się sferoidy, które podlegają fuzji i układowi komórek, aby przypominały ewoluujące tkanki. Autonomiczna samoorganizacja zależy od komórki jako podstawowego czynnika histogenezy, kierującego budulcem, właściwościami strukturalnymi i funkcjonalnymi tych tkanek. Wymaga to głębszego zrozumienia, w jaki sposób rozwijają się mechanizmy tkanek embrionalnych, a także mikrośrodowiska, w którym powstają biodrukowane tkanki.
Mini-tkanka
Trzecie podejście do biodrukowania to połączenie podejścia biomimikry i samodzielnego składania, które nazywa się mini tkankami. Organy i tkanki zbudowane są z bardzo małych elementów funkcjonalnych. Podejście mini-tissue bierze te małe kawałki i produkuje je i układa je w większe ramy.
Drukarki
Podobnie jak zwykłe drukarki atramentowe, biodrukarki składają się z trzech głównych elementów. Są to sprzęt, rodzaj bio-tuszu i materiał, na którym jest drukowany (biomateriały). „Bio-tusz to materiał wykonany z żywych komórek, który zachowuje się jak ciecz, umożliwiając ludziom „drukowanie” go w celu uzyskania pożądanego kształtu. Aby wytworzyć bio-tusz, naukowcy tworzą zawiesinę komórek, którą można wkład i wkładany do specjalnie zaprojektowanej drukarki, wraz z innym wkładem zawierającym żel znany jako bio-papier." W biodrukowaniu stosuje się trzy główne typy drukarek. Są to drukarki atramentowe, laserowe i wytłaczające. Drukarki atramentowe są wykorzystywane głównie w biodrukowaniu do szybkich i wielkoskalowych produktów. Jeden typ drukarki atramentowej, zwany drukarką atramentową typu drop-on-demand, drukuje materiały w dokładnych ilościach, minimalizując koszty i straty. Drukarki wykorzystujące lasery zapewniają drukowanie w wysokiej rozdzielczości; jednak drukarki te są często drogie. Drukarki do wytłaczania drukują komórki warstwa po warstwie, podobnie jak drukowanie 3D w celu tworzenia konstrukcji 3D. Oprócz samych komórek drukarki ekstruzyjne mogą również wykorzystywać hydrożele nasycone komórkami.
Oparte na wytłaczaniu
Druk ekstruzyjny jest bardzo powszechną techniką w dziedzinie druku 3D, która polega na wytłaczaniu lub wyciskaniu ciągłego strumienia stopionego materiału stałego lub lepkiej cieczy przez rodzaj otworu, często dyszę lub strzykawkę. Jeśli chodzi o biodrukowanie oparte na ekstruzji, istnieją trzy główne typy ekstruzji. Są to napędy pneumatyczne, tłokowe i śrubowe. Każda metoda wytłaczania ma swoje zalety i wady. Wytłaczanie pneumatyczne wykorzystywało sprężone powietrze do przetłaczania płynnego biotuszu przez środek osadzający. Powietrze używane do przemieszczania biotuszu musi być wolne od zanieczyszczeń. Filtry powietrza są powszechnie używane do sterylizacji powietrza przed jego użyciem. Tłok napędzany tłokiem wykorzystuje tłok połączony ze śrubą prowadzącą. Ruch liniowy tłoka wyciska materiał z dyszy. Wytłaczarka napędzana ślimakiem wykorzystuje ślimak ślimakowy do wytłaczania materiału. Ruch obrotowy wymusza opuszczanie materiału i wysuwanie go z dyszy. Urządzenia napędzane śrubą pozwalają na stosowanie materiałów o wyższej lepkości i zapewniają większą kontrolę objętości.
Aplikacje
Przeszczepialne narządy i organy do badań
Istnieje kilka zastosowań biodruku 3D w medycynie. Niemowlęcemu pacjentowi z rzadką chorobą układu oddechowego znaną jako tracheobronchomalacja (TBM) podano szynę tchawicy utworzoną za pomocą drukowania 3D. Biodrukowanie 3D może być wykorzystywane do rekonstrukcji tkanek z różnych obszarów ciała. Pacjenci ze schyłkową chorobą pęcherza mogą być leczeni za pomocą zmodyfikowanych tkanek pęcherza moczowego do odbudowy uszkodzonego narządu. Ta technologia może być również potencjalnie zastosowana do kości, skóry, chrząstki i tkanki mięśniowej. Chociaż jednym z długoterminowych celów technologii biodrukowania 3D jest rekonstrukcja całego narządu, drukowanie w pełni funkcjonalnych organów jest niewielkie. W przeciwieństwie do stentów wszczepialnych narządy mają złożone kształty i są znacznie trudniejsze do wydrukowania biologicznego. Na przykład biodrukowane serce musi spełniać nie tylko wymagania strukturalne, ale także wymagania dotyczące unaczynienia, obciążenia mechanicznego i propagacji sygnału elektrycznego. W 2019 roku izraelscy naukowcy skonstruowali z ludzkich komórek serce wielkości królika.
Mięso hodowlane
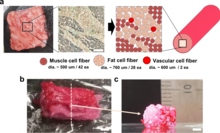
Biodrukowanie może być również stosowane w przypadku mięsa hodowlanego . W 2021 roku wyprodukowano mięso hodowlane przypominające stek, składające się z trzech rodzajów włókien komórek bydlęcych. W Wagyu -Jak wołowina ma strukturę podobną do oryginalnej mięsa.
Uderzenie
Biodrukowanie 3D przyczynia się do znaczących postępów w dziedzinie medycznej inżynierii tkankowej , umożliwiając prowadzenie badań nad innowacyjnymi materiałami zwanymi biomateriałami . Biomateriały to materiały przystosowane i wykorzystywane do drukowania obiektów trójwymiarowych. Niektóre z najbardziej godnych uwagi substancji bioinżynieryjnych są zwykle silniejsze niż przeciętne materiały ustrojowe, w tym tkanki miękkie i kości. Te składniki mogą działać jako przyszłe substytuty, a nawet ulepszenia oryginalnych materiałów korpusu. Na przykład alginian jest polimerem anionowym o wielu implikacjach biomedycznych, w tym wykonalności, silnej biokompatybilności, niskiej toksyczności i silniejszych zdolnościach strukturalnych w porównaniu z niektórymi materiałami strukturalnymi organizmu. Powszechne są również hydrożele syntetyczne, w tym żele na bazie PV. Połączenie kwasu z inicjowanym przez promieniowanie UV środkiem sieciującym na bazie PV zostało ocenione przez Wake Forest Institute of Medicine i uznane za odpowiedni biomateriał. Inżynierowie badają również inne opcje, takie jak drukowanie mikrokanalików, które mogą zmaksymalizować dyfuzję składników odżywczych i tlenu z sąsiednich tkanek. Ponadto Agencja Redukcji Zagrożeń Obronnych ma na celu wydrukowanie mininarządów, takich jak serca, wątroby i płuca, jako możliwości dokładniejszego testowania nowych leków i być może wyeliminowania potrzeby testowania na zwierzętach.
Zobacz też
Bibliografia
Dalsza lektura
- Tran J (2015). „Do biodruku czy nie do biodruku” . North Carolina Journal of Law and Technology . 17 : 123-78. SSRN 2562952 . Zarchiwizowane od oryginału w dniu 2019-03-10 . Źródło 2019-01-12 .
- Tran J (7 maja 2015). „Patentowanie biodruku”. Harvard Journal of Law and Technology Digest . 29 . SSRN 2603693 .
- Wiśwakarma A (27.11.2014). Biologia komórek macierzystych i inżynieria tkankowa w naukach dentystycznych . Elsevier, 2014. ISBN 9780123971579.


